
- •1. Основные положения статистической термодинамики
- •1.1. Понятия и начала феноменологической термодинамики.
- •1.2. Микроскопическое (механическое) описание классических систем.
- •1.3. Особенности представления квантовых систем
- •1.4. Вероятность нахождения системы в элементе фазового пространства. Метод ансамблей Гиббса.
- •1.5. Макроскопические величины как фазовые средние
- •1.6. Распределение в системах с постоянным числом частиц
- •1.6.2. Распределения Гиббса.
- •1.6.3. Квазиклассическое приближение.
- •1.7. Свойства распределения Гиббса
- •1.8. Большое каноническое распределение Гиббса
- •2. Статистика идеального газа
- •2.1. Идеальный газ как модель статистической системы
- •2.2. Распределение Максвелла
- •2.3. Столкновения молекул со стенкой сосуда. Давление
- •2.4. Характерные величины идеального газа
- •2.5. Столкновение молекул между собой
- •2.6. Длина свободного пробега
- •2.7. Идеальный газ во внешнем поле
- •2.8. Число и функция состояний идеального газа
- •2.9. Классическая теория теплоемкости газа двухатомных молекул
- •2.10. Квантовая теория теплоемкости газа двухатомных молекул
- •2.11. Распределения в квантовых системах
- •3. Законы термодинамики
- •3.1. Статистическое обоснование первого начала термодинамики
- •3.2. Второе начало термодинамики
- •3.3. Вечный двигатель второго рода. Максимальная работа процессов
- •3.4. Полезная работа тепловых машин
- •3.5. Метод термодинамических потенциалов
- •3.6. Термодинамические коэффициенты. Критерии устойчивости равновесия
- •3.7. Статистическое вычисление термодинамических величин
- •3.8. Третье начало термодинамики (теорема Нернста)
- •3.9. Применения термодинамики
- •4. Статистика сложных систем.
- •4.1. Модель кристаллического твердого тела. Уравнение движения атомов
- •4.2. Дисперсионное уравнение нормальных колебаний кристалла
- •4.3. Кристалл как система линейных гармонических осцилляторов
- •4.4. Статистическая сумма и энергия кристалла (в гармоническом приближении)
- •4.5. Теория теплоемкости Дебая
- •4.6. Электронный газ в металлах
- •4.7. Зависимость энергии электрона от волнового вектора. Эффективная масса
- •4.8. Теория парамагнетизма. Природа и характеристики магнетизма.
- •4.9. Равновесное излучение.
- •4.10. Системы с кулоновским взаимодействием частиц.
- •5. Теория малых флуктуаций
- •5.1. Определение и значение флуктуаций
- •5.2. Мера вероятности и масштаб флуктуаций
- •5.3. Флуктуации термодинамических величин в однородной среде
- •5.4. Предельная чувствительность измерительных приборов
- •5.5. Рассеяния света флуктуациями
- •6. Элементы теории физической кинетики
- •6.1. Определения и характеристики необратимых процессов
- •6.2. Теория стационарных процессов в газе свободных электронов
- •6.3. Газокинетическое уравнение Больцмана
- •6.4. Приближение времени релаксации
- •Раздел 2
- •Раздел 2
- •Раздел 3
- •Раздел 4
- •Раздел 5
- •Раздел 6
- •Список Литературы
1.8. Большое каноническое распределение Гиббса
Взаимодействие подсистемы с окружением в общем случае осуществляется взаимным обменом не только энергией, но и частицами. В процессе взаимодействия частицы уходят из подсистемы или приходят в нее, унося или принося при этом соответствующее количество энергии. Обмен энергией и частицами происходит одновременно. В такой ситуации переменной является не только энергия, но и число частиц в ней. При этом выделенная подсистема может побывать во всех квантовых состояниях, отличающихся числом частиц.
Примером систем
с переменным числом частиц могут быть
капля или кристалл (лед), находящийся в
равновесии с паром или расплавом (водой),
соответственно. Последние играют роль
окружения (термостата). Молекулы с
поверхности жидкости переходят в пар,
а молекулы из пара конденсируются на
поверхности жидкости. Тоже происходит
с молекулами на поверхности кристалла.
Если систематического перехода частиц
из пара в жидкость или обратно не
происходит, то в системе установится
состояние равновесия, при котором число
частиц, переходящих в обоих направлениях,
уравнивается. Подобная ситуация имеет
место и в равновесной химической реакции.
В выделенной подсистеме (например,
молекулах соединения
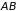 )
число частиц изменяется: уменьшается
за счет реакции распада
)
число частиц изменяется: уменьшается
за счет реакции распада
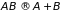 и увеличивается за счет синтеза
и увеличивается за счет синтеза
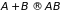 .
.
Для характеристики
состояния таких систем необходимо
указать не только ее полную энергию, но
и число частиц, которое в ней содержится.
Задача заключается в нахождении
распределения вероятностей
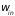 того, что подсистема находится в
-ом
состоянии и содержит при этом
частиц. Ее решение проведем по алгоритму,
изложенному в разделе 1.6.2. Отличие
состоит в том, что число состояний
системы с данной энергией
следует заменить на
того, что подсистема находится в
-ом
состоянии и содержит при этом
частиц. Ее решение проведем по алгоритму,
изложенному в разделе 1.6.2. Отличие
состоит в том, что число состояний
системы с данной энергией
следует заменить на
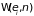 ,
где учитывается число частиц, а число
состояний термостата – на
,
где учитывается число частиц, а число
состояний термостата – на
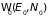 .
Поскольку сумма числа частиц в подсистеме
и термостате остается постоянной
.
Поскольку сумма числа частиц в подсистеме
и термостате остается постоянной
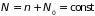 ,
вместо формул (1.51) и (1.53) получаем
,
вместо формул (1.51) и (1.53) получаем
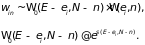 (1.68)
(1.68)
Так
как размеры термостата, его энергия и
число содержащихся в нем частиц велики,
то для всей замкнутой системы
(подсистема + термостат) справедливы
неравенства
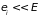 и
и
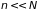 .
Поэтому, как и в разделе 1.6.2, можно
разложить функцию
.
Поэтому, как и в разделе 1.6.2, можно
разложить функцию
 в ряд по степеням
и
и ограничиться линейными членами
разложения
в ряд по степеням
и
и ограничиться линейными членами
разложения
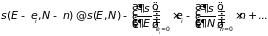 .
.
И для вероятности имеем
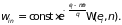 (1.69)
(1.69)
Статистическая
температура по-прежнему вычисляется
по формуле (1.55)
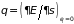 .
Коэффициент
называется химическим (парциальным)
потенциалом и определяется выражением
.
Коэффициент
называется химическим (парциальным)
потенциалом и определяется выражением
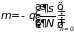 , (1.70)
, (1.70)
где производная
берется при постоянном значении энергии
и внешних параметров. Из условия
нормировки
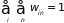 находится постоянная величина
находится постоянная величина
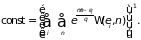
Искомое распределение вероятностей состояний системы с переменным числом частиц принимает вид
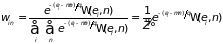 . (1.71)
. (1.71)
Здесь через
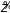 обозначена функция состояний, которая
при постоянном числе частиц в системе
обозначена функция состояний, которая
при постоянном числе частиц в системе
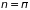 совпадает с (1.60). Полученная формула
называется большим каноническим
распределением Гиббса. Оно позволяет
находить средние значения любой величины
совпадает с (1.60). Полученная формула
называется большим каноническим
распределением Гиббса. Оно позволяет
находить средние значения любой величины
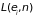 ,
зависящей от состояния системы и числа
частиц:
,
зависящей от состояния системы и числа
частиц:
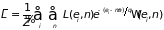 . (1.72)
. (1.72)
В частности, среднее число частиц при произвольном значении энергии системы равно
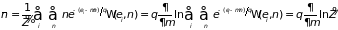 .
.
(1.73)
Это по существу первый и далеко не единственный пример определения физических параметров через функцию состояний.
Рассмотрим равновесную систему, состоящую из двух подсистем, также находящихся в состоянии статистического равновесия и слабо взаимодействующие между собой (обмениваются частицами и энергией). Для каждой из них можно записать
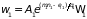 ,
,
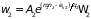 .
.
Поскольку подсистемы слабо взаимодействуют, то, согласно теореме умножения вероятностей, для вероятности одновременного нахождения первой системы в -ом, а второй – в -ом состояниях находим
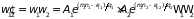 .
.
Две подсистемы
образуют одну равновесную систему с
суммарной энергией
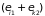 и числом частиц
и числом частиц
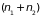 ,
для которой также справедливо большое
каноническое распределение
,
для которой также справедливо большое
каноническое распределение
 .
.
Если подсистемы
находятся в состоянии равновесия, то
при установлении взаимодействия между
ними их состояние не должно изменяться.
Поэтому необходимо, чтобы вероятности
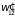 и
и
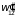 ,
определенные последними двумя равенствами,
были тождественно равны друг другу
,
определенные последними двумя равенствами,
были тождественно равны друг другу
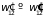 .
Отсюда следуют равенства
.
Отсюда следуют равенства
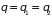 ,
,
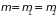 . (1.74)
. (1.74)
С физической точки зрения, это означает равенство температур и парциальных потенциалов во всех квазинезависимых подсистемах, входящих в состав равновесной системы. Согласно молекулярным представлениям, равенство температур выражает требование, чтобы количества энергии, отдаваемое и получаемое подсистемой, были равны друг другу. В равновесном состоянии при обмене частицами не только совпадает числа приходящих и уходящих из подсистемы частиц, но равны и средние энергии, переносимые этими частицами – об этом свидетельствует равенство парциальных потенциалов. Если бы это было не так, например, уходили только быстрые, а приходили только медленные частицы, то состояние равновесия было бы нарушено.
Статистические температура и парциальный потенциал определяют состояние термостата. Только в том случае, когда выделенная подсистема является макроскопической, условия равновесия позволяют относить и к самой подсистеме. Не имеет смысла говорить о температуре и парциальном потенциале микроскопической подсистемы, например, молекулы.
В
квазиклассическом приближении
число состояний системы
,
как и в разделе 1.6.3, можно выразить через
объем фазового пространства
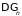
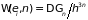 . (1.74)
. (1.74)
Здесь величина
объема фазового пространства в отличие
от систем с постоянным числом частиц
изменяется с изменением числа частиц
(степеней свободы
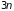 )
)
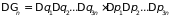 .
.
И большое каноническое распределение принимает вид
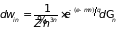 , (1.75)
, (1.75)
где функция состояния выражается следующим образом
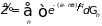 .
.
Приведенные положения статистической физики и распределения в равновесных системах относятся к широкому классу веществ. Конкретизации найденных закономерностей посвящены следующие разделы книги, где будут рассмотрены различные физические системы с учетом характера движения молекул, квазичастиц, типов взаимодействия. Общность законов статистической физики позволила не ограничивать круг ее рассмотрения чисто тепловыми процессами, но включить в нее самые разнообразные макроскопические свойства тел – оптические, электрические, магнитные, химические и т.п.
