
- •Литейные сплавы и плавка предисловие
- •Литейные свойства сплавов
- •1.1. Технологические свойства сплавов и важность их определения для практики
- •1.2. Номенклатура литейных свойств сплавов
- •1.3. Жидкотекучесть. Технологические пробы
- •Взаимосвязь толщин стенок отливок и площади их поверхности при литье в кокиль
- •Взаимосвязь толщины стенок отливки и площади их поверхности при литье под давлением
- •1.4. Склонность отливок к образованию усадочных раковин и пористости
- •V1, v2, v3 и v0 - объемы сплава при соответствующих температурных условиях
- •Температурные коэффициенты объемного сжатия (ткос) в жидком состоянии (индекс «ж») и объемная усадка затвердевания (индекс «з»)
- •1.5. Линейная усадка сплавов и отливок
- •1.6. Усадочные напряжения в отливках
- •1.7. Склонность сплавов и отливок к горячим трещинам
- •1.8. Склонность сплавов и отливок к холодным трещинам
- •3.9. Склонность сплавов к насыщению газами и образованию газовой пористости
- •Растворимость водорода в металлах
- •1.10. Неметаллические включения и плены в сплавах
- •1.11. Склонность компонентов сплавов к ликвации
- •1.12. Зависимость механических свойств сплавов от толщины стенок отливок
- •Механические свойства и рекомендуемый химический состав серого чугуна по гост 1412-85
- •Механические свойства серых чугунов, не предусмотренные гост 1412-85
- •Физические свойства чугунов
- •5.3. Высокопрочный чугун
- •Механические свойства*1 и рекомендуемый химический состав высокопрочного чугуна с шаровидным графитом по гост 7283—85
- •5.4. Чугун с вермикулярным графитом
- •Зависимость механических свойств и объема усадочных раковин в чвг от содержания шаровидного графита (шг)
- •5.5. Ковкий чугун
- •Содержание с и Si в отливках из ковкого чугуна в зависимости от толщины стенок
- •Механические свойства и рекомендуемый химический состав ковкого чугуна по гост 7293-79 (изм. В 1991 г.)
- •Марки, содержание углерода и механические свойства литейных углеродистых сталей по гост 977-88
- •Средний химический состав легированных сталей, мае. %
- •Механические свойства легированных сталей
- •Литейные сплавы цветных металлов
- •6.1. Алюминиевые сплавы
- •Химический состав и механические свойства алюминиевых литейных сплавов по гост 1583—93
- •* В данной таблице обозначения способов литья те же, что в табл. 6.1; то — термическая обработка; ств — временное сопротивление разрыву; стт — предел текучести; 5 — относительное удлинение.
- •Химический состав литейных титановых сплавов, мае. %
- •Линейная усадка 8/ и объем ву.Р усадочных раковин в отливках титановых сплавов
- •Механические свойства бронз
- •Механические свойства латуней
- •Средний химический состав и прочностные свойства никелевых литейных сплавов при температурах 800 и 900 °с
- •Основные понятия и определения
- •Классификация огнеупорных материалов
- •Типовые операции и процессы плавки литейных сплавов Горение топлива
- •Шлакообразование. Строение шлаковых расплавов
- •8.3. Окислительное рафинирование
- •8.4. Закономерности угара элементов в кислых и основных печах
- •Удаление вредных примесей из железоуглеродистых сплавов
- •8.7. Раскисление металла
- •Науглероживание расплавов железа
- •Взаимодействие футеровки с расплавами шлакаи металла
- •Исходные материалы для плавки литейных сплавов Первичные металлические материалы
- •Соотношение содержаний с и Si в литейных чугунах
- •9.2. Вторичные металлические материалы
- •Вторичные черные металлы
- •Физические характеристики* важнейших шихтовых материалов
- •Топливо
- •Важнейшие характеристики каменноугольного кокса
- •9.4. Флюсы
- •Состав известняка, мае. %
- •9.5. Расчет шихты
- •Список компонентов шихты и ограничений по их содержанию
- •Угар (пригар) химических элементов при плавке чугуна
- •Угар элементов при выплавке цветных сплавов, отн. %
- •Примечание. В числителе — угар при плотной шихте, в знаменателе — угар при некомпактной шихте.
- •Примечание. Минимальное значение функции равно 2720,49 руб./т.
- •10.1. Принцип действия и разновидности конструкций коксовых вагранок
- •Особенности горения кокса в вагранках
- •Изменение температуры и химического состава газовой фазы по высоте вагранки
- •Влияние высоты холостой колоши на процесс плавки в вагранке
- •Влияние размеров рабочих колош на процесс плавления шихты в вагранке
- •Влияние качества кокса на тепловые процессы в вагранке
- •Влияние подготовки шихты на ход ваграночной плавки
- •Влияние величины удельного расхода кокса и воздуха на ход ваграночной плавки
- •Способы интенсификации ваграночного процесса
- •Металлургические процессы плавки в коксовой вагранке
- •Расчет требуемого расхода известняка
- •Данные о характере газовой фазы в зонах вагранки
- •Значение коэфициента к науглероживания в холостой колоше
- •Зависимость концентрации серы в чугуне от содержания ее в коксе
- •Особенности плавки в вагранках с основной футеровкой
- •Особенности плавки в металлургических вагранках
- •Особенности плавки чугуна в коксогазовых вагранках
- •Плавка чугуна в бескоксовых вагранках
- •Стабилизация химического состава чугуна, выплавляемого в вагранках
- •Плавка чугуна в дуговых печах
- •11.2. Технология плавки
- •Особенности конструкции и технологии плавки чугуна в дуговых печах постоянного тока
- •Плавка чугуна в индукционных печах
- •Выбор частоты тока для питания индукционных тигельных печей
- •Электромагнитное перемешивание металла в тигле
- •12.4. Основные элементы конструкции печей промышленной частоты
- •Изготовление футеровки печи
- •Технология плавки чугуна в индукционных тигельных печах промышленной частоты
- •12.7. Особенности плавки чугуна в индукционных тигельных печах средней частоты
- •Индукционные канальные печи в чугунолитейном производстве
- •Преимущества и недостатки индукционных канальных печей.
- •12.9. Сравнительный анализ процессов плавки чугуна в современных чугуноплавильных печах
- •Технологические особенности плавки различных сортов чугуна
- •13.1. Технология получения высококачественного серого чугуна с пластинчатым графитом
- •13.2, Технология получения высокопрочного чугуна с шаровидным графитом
- •13.3. Производство чугуна с вермикулярным графитом
- •13.4. Производство ковкого чугуна
- •Рекомендации по введению легирующих элементов при плавке легированных чугунов
- •Плавка стали
- •14.1. Плавка стали в мартеновских печах
- •Плавка стали в мартеновской печи с основной футеровкой.
- •Плавка стали в основной дуговой печи с окислением примесей.
- •14.4. Плавка стали в индукционных тигельных печах Общая характеристика особенностей плавки стали в индукционных тигельных печах.
- •Плавка в печи с кислой футеровкой.
- •Особенности плавки в индукционных тигельных печах с основной футеровкой.
- •14.6. Электрошлаковый переплав стали
- •Плавка сплавов цветных металлов
- •15.1. Плавка сплавов на основе алюминия
- •Характеристики двойных алюминиевых лигатур
- •Состав модификаторов и параметры процесса модифицирования алюминиевых сплавов
- •15.2. Плавка сплавов на основе магния
- •Режимы модифицирования магниевых сплавов
- •15.3. Плавка сплавов на основе цинка
- •Составы лигатур для плавки медных сплавов
- •Список литературы к разделу 1
- •К разделу II
Шлакообразование. Строение шлаковых расплавов
Источники шлакообразования. Источниками образования шлаков при плавке литейных сплавов в различных плавильных печах могут быть вещества различного происхождения. В зависимости от этого их можно подразделить на несколько групп.
Первую группу составляют химические соединения, находившиеся на поверхности кусков шихты до их загрузки в печь. Это частицы земли, глины, песка, оксидов основного металла и легирующих элементов компонентов шихты.
Ко второй группе относятся вещества, образовавшиеся в результате взаимодействия с атмосферой печи (угара) основного металла, легирующих элементов и примесей.
Частицы оплавившейся футеровки в большинстве случаев также оказываются в шлаке, образуя третью группу.
Для печей, работающих на твердом топливе, источником шлакообразования может быть зола топлива (четвертая группа).
Эти четыре группы веществ образуют первичный (так называемый самородный) шлак. Свойства такого шлака далеко не всегда удовлетворяют требованиям литейщиков. Так, например, первичный шлак, образующийся в чугуноплавильной печи непрерывного действия (вагранке), имеет высокую вязкость, которая является препятствием при удалении шлака через шлаковую летку. Для снижения вязкости шлака, т.е. для увеличения его жидкотекучести в печь добавляют вещество (флюс), снижающее температуру плавления шлака. Этим веществом является и з в е с - т н я к. (В старину вещества, улучшающие плавкость шлака, называли плавнями.)
При плавке стали на шихте, содержащей повышенное количество серы и фосфора, в печь вводят вещества (флюсы), которые, вступая в химические реакции с этими вредными примесями, переводят их в шлак.
На этих примерах показана роль флюса в плавке. В первом случае добавляемые к первичному шлаку вещества изменяли его физическое свойство - температуру плавления, во втором - химическое свойство, в частности способность вступать в реакцию с вредными веществами. Таким образом, для придания шлаку требуемых физико-химических свойств в печь добавляют вещества, называющиеся флюсами.
Роль шлаков в процессе плавки может быть различной в зависимости от природы литейного сплава, типа плавильной печи и шихтовых материалов, используемых для плавки. Наиболее сложные и многообразные функции шлак выполняет в условиях плавки стали в мартеновских и дуговых печах на шихте, загрязненной серой и фосфором. Не вдаваясь в детали этих функций, которые будут раскрыты по ходу дальнейшего изложения, ограничимся их простым перечислением задач, которые возложены на шлак.
Обеспечить быструю передачу тепла от газовой фазы к металлу.
Обеспечить питание жидкой ванны расплава кислородом в окислительный период плавки.
Служить защитным покровом, затрудняющим растворение азота и водорода в металле.
Создать условия, обеспечивающие минимальное содержание в металле серы и фосфора.
Обеспечить возможность проведения процесса раскисления стали, в частности, диффузионного раскисления и др.
По сравнению с металлургическими процессами плавку стали в литейных цехах обычно ведут более простыми технологическими процессами, в которых используется только какая-то (большая или меньшая) часть отмеченных функций шлака.
При выплавке цветных сплавов используют так называемые покровные флюсы, роль которых сводится к защите металла от газовой фазы печи. Составы и свойства этих шлаков будут рассмотрены при изложении технологии плавки конкретных цветных сплавов.
В данном разделе рассматриваются строение и свойства шлаков, используемых при плавке железоуглеродистых сплавов.
Наибольшее распространение получили две теории строения шлаковых расплавов — ионная и молекулярная.
Ионная теория. Данная теория предполагает, что различные химические соединения в шлаковых расплавах находятся в состоянии частичной диссоциации по следующим схемам:
Me О <=> Ме2+ +02";
MeS+±Me2+ +S2;
Me F2 <=>Me2+ + 2F";
3 (Me О) • P205 <=> 3Me2+ + 2PO^";
2 (Me O) • Si02 <=> 2Me2+ + SiO^;
2(MeO) • Si02 <=> 2Me2+ + Si20;|-;
3 (MeO) • 2(Si02) <=> 3Men + Si20^.
Из существующих многочисленных подтверждений справедливости ионной природы строения шлаковых расплавов можно привести такое явление, как электролиз жидких шлаков. Тем не менее, применение ионной теории на практике затруднено, так как в шлаках наряду с простыми ионами могут находиться в состоянии метастабильного или стабильного равновесия сложные анионы. Оперировать с такими сложными частицами при проведении обычных химических расчетов затруднительно, поэтому на практике обычно руководствуются более простой молекулярной теорией.
Молекулярная теория. Получившая широкое распространение молекулярная теория основана на предположении о том, что шлак состоит из электрически нейтральных молекул оксидов, которые можно расположить по химическим свойствам в следующий ряд:
Увеличение основных свойств оксидов
Si02, Р205, А1203, ТЮ2, FeO, MgO, MnO, CaO
Увеличение кислотных свойств оксидов
Каждый из оксидов в приведенном ряду является кислотным по отношению к оксиду, расположенному справа, и основным по отношению к соседу слева. Кислотные и основные оксиды в шлаке могут реагировать между собой, образуя соли.
Активность оксида в шлаке определяется не общим его содержанием, а концентрацией свободного оксида, которая вычисляется по балансовому уравнению типа:
СаОсвободн = СаОобщ + СаО$ю2 - СаОр2о5,
где СаОсвободн — концентрация оксида кальция химически не связанного; СаОобщ — суммарная концентрация оксида кальция в шлаке; CaOSi02 — концентрация оксида кальция, связанного с кремнеземом; СаОр2о5 — концентрация оксида кальция, связанного в фосфорнокислое соединение.
Если в результате взаимодействия кислотных и основных оксидов в шлаке свободными остаются основные оксиды, то шлак считается основным и, наоборот, наличие свободных кислотных оксидов делает шлак кислым.
На практике свойства шлака определяют по степени его основности, которая в простейшем случае двухкомпонентного шлака, состоящего из оксида кремния и оксида кальция, равна:
В = Ca0/Si02,
где В — основность шлака; СаО — концентрация в шлаке основного оксида кальция; мае. %; Si02 — концентрация в шлаке кислотного оксида кремния, мае. %.
В общем случае основность вычисляют по формуле
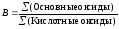
где ∑ (основные оксиды) — суммарное содержание основных оксидов, мае. %; ∑ (кислотные оксиды) — суммарное содержание кислотных оксидов, мае. %.
В зависимости от основности шлак принято считать кислым (В меньше 0,8), нейтральным (В = 0,8... 1,2) и основным (В больше 1,2). В свою очередь, основные шлаки подразделяются на:
шлаки пониженной основности, В= 1,3... 1,5,
шлаки средней основности, В= 1,6...2,5,
шлаки повышенной основности, В выше 2,5.
Величина, обратная основности, называется степенью кислотности:
А = 1/В.
Молекулярная теория позволяет описывать важнейшие химические реакции между шлакообразующими оксидами. Результаты расчетов, проведенных на основе молекулярной теории, хорошо согласуются с практическими данными, однако это совпадение можно рассматривать как чисто формальное, не выявляющее истинной физико-химической природы процессов. В металлургии и литейном производстве молекулярные представления о строении шлаков имеют широкое распространение, так как они были применены ранее ионных и позволили качественно объяснить ряд явлений, происходящих в плавильных печах.
На практике в большинстве случаев три вещества — Si02, СаО и А1203 — составляют 90...95% массы шлака и определяют его
1710°С
Рис. 2. Диаграмма
состояния системы СаО—Si02—
А1203
важнейшие свойства. Поэтому зависимость важнейших физических свойств шлаков (температуры плавления, вязкости и др.) от их состава изображают в основном в виде двойных или тройных диаграмм состояния.
На рис.2 приведена диаграмма состояния трехкомпонентных шлаков, содержащих Si02, СаО и А1203.
Шлаки, как и другие многокомпонентные системы, плавятся в интервале температур. Поэтому температура плавления шлаков является условной величиной. За температуру плавления шлаков принимают температуру ликвидуса, т. е. температуру полного исчезновения твердой фазы при нагреве.
На диаграмме штриховыми и тонкими сплошными линиями показаны изотермы, т. е. линии одинаковых температур плавления, а более толстыми линиями обозначены границы между областями кристаллизации отдельных химических соединений.
Из данной диаграммы следует, что шлаки с высокой основностью имеют и максимальную температуру плавления.
С помощью диаграммы состояния можно определить количество флюса, необходимого для получения шлака с минимальной температурой плавления.
Численный пример. Пусть при плавке на данной шихте при данных режимах образуется первичный шлак, состоящий из 80 % Si02 и 20 % А1203. Из диаграммы (см. рис. 8.2) следует, что температура плавления такого шлака находится в пределах 1700... 1800 °С. Требуется определить количество флюса — извести (СаО), — позволяющее существенно снизить температуру плавления шлака.
Добавление флюса увеличит общее количество шлака в печи, но соотношение между Si02 и А1203, равное 4 (80 %/20 %), при этом не изменится. Составы шлаков, для которых соотношение содержаний Si02 и А1203 равно 4, по совокупности соответствуют линии, соединяющей вершину треугольника (100 % СаО) и точку 20 % А1203 на стороне треугольника Si02 — А1203. Находим точку пересечения этой линии с изотермой плавления, равной 1300 °С. Из точки пересечения проводим прямую, параллельную стороне треугольника Si02—А1203. На пересечении этой прямой со шкалой содержания СаО находим, что содержание этого компонента (извести) в шлаке равно 17,5 %. Аналогично находится содержание Si02 и А1203 в трехкомпонентном шлаке (равно соответственно Si02 66 % и А1203 16,5 %).
Однако для выбора состава шлака знания только температуры его плавления недостаточно, так как некоторые из шлаков становятся хорошо подвижными при температуре, значительно превышающей температуру плавления. Например, самый легкоплавкий шлак, содержащий примерно 62 % Si02, 24 % СаО и 14 % А1203, температура плавления которого равна 1170°С, приобретает хорошую текучесть лишь при температуре 1600 °С. Поэтому
25,9%А1203
. 30
Рис. 8.3. Зависимость
вязкости (толстые линии) и температуры
плавления (тонкие линии) шлака от
его состава и температуры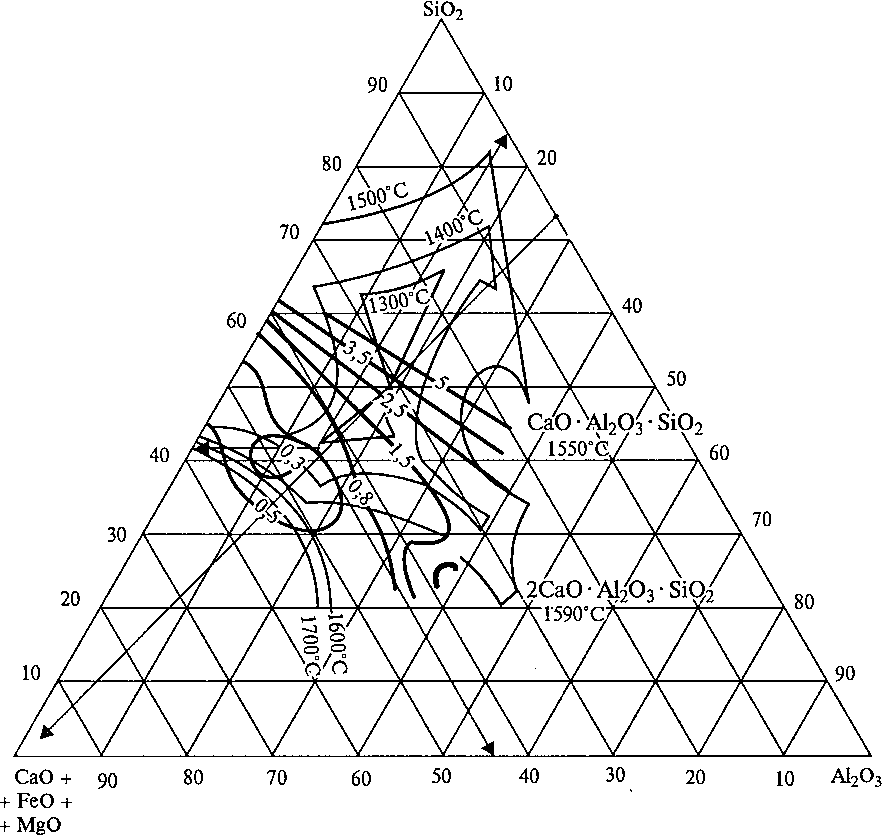
выбор состава шлака обычно проводят по диаграмме, представленной на рис. 8.3, которая отражает влияние состава шлака и на его вязкость, и на температуру плавления. На диаграмме толстыми линиями нанесены линии одинаковой вязкости (Па-с), а тонкими — линии одинаковых температур плавления (°С). Из диаграммы следует, что область минимальных значений вязкости шлака не совпадает с областью минимальной температуры плавления.
Методика расчета количества флюса, необходимого для получения требуемой вязкости шлака, аналогична методике расчета по требуемой температуре плавления шлака. Численный пример такого расчета применительно к шлаку ваграночной плавки приведен на с. 235.
На практике вязкость трехкомпонентных шлаков снижают добавками CaF2 и MgF2.
