
- •Глава 1. Основы теоретических представлений в органической химии
- •1.1. Учение а.М. Бутлерова
- •1.2. Теория гибридизации атомных орбиталей
- •1.3. Ковалентная связь
- •1.3.3. Водородные связи
- •1.4. Теория электронных смещений
- •1.5. Классификация и номенклатура органических соединений
- •1.5.1. Заместительная номенклатура
- •1.5.2. Радикало-функциональная номенклатура
- •1.5.4. Рациональная Номенклатура
- •1.6. Представление о Кислотно-оснÓвных свойствах органических соединений
- •1.7. Основы стереохимии
- •1.7.1. Оптическая изомерия
- •1.7.2. Геометрическая изомерия
- •1.7.3. Конформационная изомерия
- •1.8. Классификация органических реакций. Понятие о механизме реакций. Растворители и катализаторы
- •1.9. Методы идентификации органических соединений. Основные физические константы
- •1.10. Методы разделения и очистки органических веществ
- •1.10.1. Разделение твёрдых смесей и очистка твёрдых веществ
- •1.10.2. Разделение жидких смесей и очистка жидкостей
- •1.11. Представление о биологическом действии и метаболизме органических соединений
- •Глава 2. Алканы
- •2.1. Номенклатура. Изомерия
- •2.2. Строение
- •2.3. Физические свойства
- •2.4. Химические свойства
- •2.4.1. Реакции радикального замещения
- •2.4.2. Реакции дегидрирования и разложения
- •2.4.3. Реакции изомеризации
- •Способы получения и природные источники
- •2.6. Применение и физиологическая роль
- •Глава 3. Функциональные производные алканов
- •3.1. ОбщноСть Химических свойств
- •3.1.1. Реакции нуклеофильного замещения
- •3.1.2. Реакции отщепления (элиминирования)
- •3.2. Галогеналканы
- •3.2.1. Классификация, номенклатура, изомерия
- •3.2.2. Строение и свойства
- •3.2.3. Способы получения
- •3.2.4. Полигалогеналканы
- •3.2.5. Физиологическая роль и Важнейшие представители
- •3.3. Насыщенные спирты
- •3.3.1. Классификация, номенклатура, изомерия
- •3.3.2. Строение и физические свойства
- •3.3.3. Химические свойства
- •3.3.4. Способы получения
- •3.3.5. Многоатомные спирты
- •3.3.6. Физиологическое действие
- •3.3.7. Важнейшие представители
- •3.4. Простые насыщенные эфиры
- •3.4.1. Номенклатура и изомерия
- •3.4.2. Физические и химические свойства
- •3.4.3. Способы получения
- •3.4.4. Циклические простые эфиры
- •3.4.5. Физиологическая роль и Важнейшие представители
- •3.5. Эфиры минеральных кислот
- •3.5.1. Эфиры серной кислоты
- •3.5.2. Эфиры фосфорной кислоты
- •3.6. Тиоспирты и тиоэфиры
- •3.7. Насыщенные амины
- •3.7.1. Классификация, номенклатура, изомерия
- •3.7.2. Физические свойства
- •3.7.3. Строение и химические свойства
- •3.7.4. Способы получения
- •3.7.5. Физиологическая роль и Важнейшие представители
- •3.8. Нитроалканы
- •3.8.1. Строение
- •3.8.2. Свойства
- •3.8.3. Способы получения
- •3.8.4. Физиологическое действие и Важнейшие представители
- •3.9. Кремний-, фосфор- и мышьякорганические соединения
- •3.9.1. Кремнийорганические соединения
- •3.9.2. Фосфорорганические соединения
- •3.9.3. Мышьякорганические соединения
- •Глава 4. Непредельные углеводороды
- •4.1. ОБщность строения и химических свойств
- •4.1.1. Реакции электрофильного присоединения
- •4.1.2. Реакции радикального присоединения
- •4.1.3. Реакции радикального замещения
- •4.1.4. Другие реакции
- •4.2. Этиленовые углеводороды
- •4.2.1. Номенклатура, изомерия
- •4.2.2. Физические свойства
- •4.2.3. Химические свойства
- •4.2.4. Способы получения
- •4.2.5. Физиологическое действие и Важнейшие представители
- •4.3. Диеновые (и полиеновые) углеводороды
- •4.3.1. Классификация, номенклатура
- •4.3.5. Способы получения
- •4.3.6. Важнейшие представители
- •4.4. Ацетиленовые углеводороды
- •4.4.1. Номенклатура, изомерия
- •4.4.2. Особенности строения и свойств
- •4.4.3. Способы получения
- •4.4.4. Физиологическое действие и Важнейшие представители
- •Глава 5. Функциональные производные непредельнЫх углеводороДов
- •5.1. ОБщность строения и химических свойств
- •5.1.1. Классификация
- •5.1.2. Субстраты винильного типа
- •5.1.3. Субстраты аллильного типа
- •5.2. Галогеналкены
- •5.2.1. Винилгалогениды
- •5.2.2. Аллилгалогениды
- •5.2.3. Способы получения
- •5.2.4. Важнейшие представители
- •5.3. Непредельные спирты и эфиры
- •5.3.1. Виниловый спирт и его эфиры
- •5.3.2. Аллиловый и пропаргиловый спирты
- •5.3.3. Способы получения
- •5.3.4. Важнейшие представители
- •Глава 6. Алифатические альдегиды, кетоны и карбоновые кислоты
- •6.1. Насыщенные альдегиды и кетоны
- •6.1.1. Изомерия, номенклатура
- •6.1.2. Строение карбонильной группы
- •6.1.3. Физические свойства
- •6.1.4. Химические свойства
- •6.1.5. Способы получения
- •6.1.6. Физиологическая роль
- •6.1.7. Важнейшие представители
- •6.2. Непредельные альдегиды и кетоны
- •6.2.1. Кетен
- •6.2.2. Непредельные карбонильные соединения
- •Примерами соединений с сопряжёнными -связями являются
- •6.2.3. Важнейшие представители
- •6.3. Дикарбонильные соединения
- •6.3.3. Важнейшие представители
- •6.4. Насыщенные монокарбоновые кислоты и их производные
- •6.4.1. Номенклатура
- •6.4.2. Строение функциональной группы
- •6.4.3. Физические свойства
- •6.4.4. Химические свойства
- •6.4.5. Способы получения
- •6.4.6. Пероксикарбоновые кислоты и ацилпероксиды
- •6.4.7. Физиологическая роль и Важнейшие представители
- •6.5. Непредельные монокарбоновые кислоты
- •6.5.1. Номенклатура, изомерия
- •6.5.2. Строение
- •6.5.3. Химические свойства
- •6.5.4. Способы получения
- •6.5.5. Физиологическая роль и Важнейшие представители
- •6.5.6. Омыляемые липиды
- •6.6. Дикарбоновые кислоты и их производные
- •6.6.1. Особенности химического поведения
- •6.6.2. Малоновый эфир и синтезы на его основе
- •2 H5c2ooc-ch2-cooc2h5
- •2 H5c2ooc-ch2-cooc2h5
- •6.6.3. Способы получения
- •2 Rooc-(ch2)n-сoo¯ 2 rooc-(ch2)n-сoo rooc-(ch2)2n-coor hooc-(ch2)2n-cooh
- •6.6.4. Важнейшие представители
- •6.7. Гидроксикислоты
- •6.7.1. Классификация, номенклатура, изомерия
- •6.7.2. Химические свойства
- •6.7.3. Способы получения
- •6.7.4. Физиологическая роль и Важнейшие представители
- •6.8. Оксокислоты
- •6.8.1. Особенности химического поведения
- •6.8.2. Ацетоуксусный эфир и синтезы на его основе
- •6.8.3. Способы получения
- •6.8.4. Важнейшие представители
- •6.9. Аминокарбоновые кислоты. Пептиды
- •6.9.1. Классификация, номенклатура, изомерия аминокислот
- •6.9.2. Строение, физические и Химические свойства
- •6.9.3. Способы получения аминокислот
- •6.9.4. Важнейшие представители аминокислот
- •6.9.5. Пептиды
- •Глава 7. Углеводы
- •7.1. Моносахариды
- •7.1.1. Изомерия, номенклатура
- •7.1.2. Химические свойства
- •7.1.3. Важнейшие представители моносахаридов и их производных
- •7.2. Олигосахариды
- •7.2.1. Классификация и номенклатура дисахаридов
- •7.2.2. Химические свойства дисахаридов
- •7.2.3. Важнейшие представители дисахаридов
- •7.3. Полисахариды
- •7.3.1. Целлюлоза
- •7.3.2. Амилоза и амилопектин
- •7.3.3. Гликоген
- •7.3.4. Декстраны
- •7.3.5. Хитин
- •7.3.6. Пектовая кислота
- •7.3.7. Гетерополисахариды
- •Глава 8. Алициклические углеводороды и их производные
- •8.1. Номенклатура моно- и бициклических соединений
- •8.2. Пространственное строение и изомерия циклоалканов
- •8.2.1. Циклопропан
- •8.2.2. Циклобутан
- •8.2.3. Циклопентан
- •8.2.4. Циклогексан
- •8.3. Химические свойства
- •8.3.1. Реакции циклопропана, циклопропена и их производных
- •8.3.2. Реакции циклобутана и его производных
- •8.3.3. Реакции средних циклов
- •8.3.4. Реакции изомеризации цикла
- •8.4. Способы получения циклоалканов
- •8.5. Терпены и терпеноиды. Каротиноиды
- •8.5.1. Ациклические терпены и терпеноиды
- •8.5.2. Моноциклические терпены и терпеноиды
- •8.5.3. Бициклические терпены и терпеноиды
- •8.5.4. Каротиноиды
- •8.6. Физиологическая роль и важнейшие представители
- •8.7. Стероиды
- •Глава 9. Бензол. Ароматичность. Углеводороды ряда бензола
- •9.1. Строение бензола
- •Тепловой эффект реакции гидрирования бензола составляет
- •9.2. Номенклатура и изомерия аренов
- •9.3. Строение аренов
- •9.3.1. Строение толуола
- •9.3.2. Строение винилбензола
- •9.4. Физические свойства
- •9.5. Химические Свойства
- •9.5.1. Химические свойства бензола
- •9.5.2. Химические свойства аренов
- •9.6. Способы получения
- •9.7. Физиологическое действие и важнейшие представители аренов
- •9.8. Небензоидные ароматические системы
- •Глава 10. Функциональные производные углеводородов ряда бензола
- •10.1. Общность строения и свойств монозамещённых бензолов
- •10.1.1. Электронные эффекты заместителей
- •10.1.2. Реакции электрофильного замещения
- •10.1.3. Реакции нуклеофильного замещения
- •10.2. Галогенарены
- •10.2.1. Классификация, номенклатура
- •10.2.2. Строение арилгалогенидов
- •10.2.3. Физические свойства
- •10.2.4. Химические свойства
- •10.2.5. Способы получения
- •10.2.6. Важнейшие представители
- •10.3. Ароматические сульфокислоты
- •10.3.1. Номенклатура
- •10.3.2. Строение
- •10.3.3. Физические и химические свойства
- •10.3.4. Способы получения
- •10.3.5. Производные сульфокислот
- •10.3.6. Медико-биологическое значение и Важнейшие представители
- •10.4. Ароматические нитросоединения
- •10.4.1. Строение нитробензола
- •10.4.2. Физические свойства
- •10.4.3. Химические свойства
- •10.4.4. Способы получения
- •10.4.5. Физиологическое действие и Важнейшие представители
- •10.5. Фенолы. Ароматические спирты. Хиноны
- •10.5.1. Классификация, номенклатура, изомерия фенолов и ароматических спиртов
- •10.5.2. Строение фенола и бензилового спирта
- •Ароматические амины и продукты неполного восстановления нитросоединений
- •10.6.1. Классификация, номенклатура, изомерия ароматических аминов
- •10.6.2. Строение анилина
- •10.6.3. Физические и химические свойства ароматических аминов
- •10.6.4. Способы получения ароматических аминов
- •10.6.5. Важнейшие представители ароматических аминов
- •10.6.6. Продукты неполного восстановления нитросоединений
- •10.7. Ароматические диазосоединения
- •10.7.2. Механизм образования солей арендиазония и строение катиона бензолдиазония
- •10.7.3. Амфотерность диазосоединений
- •10.7.4. Реакции солей арендиазония
- •10.8. Ароматические альдегиды и кетоны
- •10.9. Ароматические карбоновые кислоты и их производные
- •10.10. Физиологическая роль функциональных производных бензола
- •Глава 11. Полициклические ароматические углеводороды и их производные
- •11.1. Классификация углеводородов с конденсированными циклами
- •11.2. Нафталин
- •11.2.1. Строение, изомерия, номенклатура
- •11.2.2. Свойства
- •11.2.3. Способы получения
- •11.2.4. Важнейшие представители
- •11.3. Антрацен
- •11.3.1. Строение, изомерия, номенклатура
- •11.3.2. Свойства
- •Продукт исчерпывающего гидрирования (пергидроантрацен) можно получить, проводя реакцию в жёстких условиях с применением металлических катализаторов.
- •11.3.3. Способы получения
- •11.3.4. Важнейшие представители
- •11.4. Фенантрен
- •11.4.1. Строение, изомерия, номенклатура
- •11.4.2. Свойства
- •11.4.3. Способы получения
- •11.5. Физиологическое действие полициклических углеводородов
- •Глава 12. Гетероциклические соединения
- •12.1. Классификация и номенклатура
- •12.2. Пятичленные гетероциклические
- •12.2.1. Номенклатура пиррола, фурана и тиофена и их производных
- •12.2.2. Строение пиррола, фурана и тиофена
- •12.2.3. Физические и химические свойства пиррола, фурана и тиофена
- •12.2.4. Особенности индола
- •12.2.5. Способы получения пиррола, фурана, тиофена, индола
- •12.2.6. Важнейшие представители и медико-биологическое значение
- •12.3. Пятичленные гетероциклические
- •12.3.1. Номенклатура имидазола и пиразола
- •12.3.2. Строение имидазола и пиразола
- •12.3.3. Физические и химические свойства имидазола и пиразола
- •12.3.4. Способы получения
- •12.3.5. Важнейшие представители и медико-биологическое значение
- •12.4. Шестичленные гетероциклические
- •12.4.1. Номенклатура пиридина и его производных
- •12.4.2. Строение пиридина
- •12.4.3. Химические свойства пиридина
- •Но если оба -положения заняты, то замещается водород в-положении. При нагревании с избытком амида натрия можно получить 2,6-диаминопиридин.
- •12.4.4. Особенности химического поведения пиколинов и функциональных производных пиридина
- •12.4.5. Хинолин и изохинолин
- •12.4.7. Способы получения
- •Реакция аналогична получению бензола, протекает при высоких температурах, но представляет только теоретический интерес.
- •12.4.8. Важнейшие представители и медико-биологическое значение
- •12.5. Шестичленные гетероциклические
- •12.5.1. Строение и свойства диазинов
- •12.5.2. Пурин
- •12.5.3. Способы получения
- •12.5.4. Важнейшие представители и медико-биологическое значение
- •12.5.5. Нуклеозиды, нуклеотиды и нуклеиновые кислоты
- •12.6. Алкалоиды
10.6.3. Физические и химические свойства ароматических аминов
Ароматические амины — бесцветные жидкости или кристаллические вещества со специфическим запахом, темнеющие на воздухе. Низшие амины плохо растворимы в воде, высшие — в воде нерастворимы. Плотности большинства соединений близки к 1 г/мл.
Химические свойства ароматических аминов определяются наличием аминогруппы и бензольного кольца, причём высокая эффективность взаимодействия этих структурных составляющих приводит к значительному изменению активности аминов в реакциях как с участием аминогруппы, так и ароматического кольца.
10.6.3.1. Электрофильное замещение
Как и многие ароматические соединения, ароматические амины могут вступать в реакции электрофильного замещения (SE) по бензольному кольцу. Аминогруппа является одним из самых сильных электронодоноров в ароматическом кольце за счёт большого+М-эффекта. В результате электронная плотность на кольце повышена, и это повышение наблюдается, главным образом, во-ип-положениях. Таким образом, реакции ароматических аминов с электрофильными реагентами протекают значительно легче, чем для бензола и аренов. Механизм взаимодействия анилина с электрофильной частицей можно представить следующим образом:

Вступление электрофила в о- и п-положения бензольного кольца может быть объяснено также динамическим подходом.
Однако помимо высокой реакционной способности ароматических аминов по отношению к электрофилам замещение в бензольном кольце аминов имеет ряд существенных особенностей. Эти особенности связаны прежде всего с тем, что большинство электрофильных реакций протекает в кислой среде.
Галогенирование протекает легко. При этом наиболее гладко протекает бромирование. Так, обработка анилина бромной водой сразу приводит к образованию 2,4,6-триброманилина:

Электрофильной частицей здесь является бромоний-катион Br+, который образуется при диспропорционировании молекулы брома в водной среде. Для получения монобромпроизводных ароматические амины предварительно ацилируют и затем бромированию подвергаютN-ацильное производное:

Ацильная группа за счёт сопряжения уменьшает электронодонорную активность аминогруппы, и реакционная способность ароматического кольца уменьшается. После проведения бромирования ацильную защиту снимают, проводя гидролиз в кислой среде.
Хлорирование в водной среде сопровождается образованием продуктов окисления, например образованием хлоранила — см. гл. 10.5.7.
Нитрование ароматических аминов в бензольное кольцо можно проводить нитрующей смесью с образованиемм-нитроанилина в качестве основного продукта, так как в кислой среде амины превращаются в соли замещённого аммония, а аммонийная группа в кольце является сильным акцептором. Поэтому для проведения нитрования требуются жёсткие условия, и преимущественная ориентация замещения — вмета-положение:

Такое направление замещения в катионе замещённого аммония объясняется динамическим подходом. Для этого требуется сравнить устойчивость -комплексов. Несмотря на то, что число граничных структур-комплексов при вступлении электрофила ворто-,мета- ипара-положения одинаково,-комплексы с электрофильной частицей ворто- ипара-положениях по отношению к аммонийной группе менее устойчивы, так как одна из трёх граничных структур в этих случаях сильно дестабилизирована за счёт локализации положительного заряда на атоме углерода, связанном с аммонийным атомом азота. Эти граничные структуры изображены последними в соответствующих рядах.

Нитрование ароматических аминов нельзя проводить концентрированной азотной кислотой, так как это требует нагревания, а при повышенных температурах усиливаются окислительные свойства азотной кислоты. Поэтому при применении концентрированной азотной кислоты происходит не нитрование, а окисление амина. Использование других нитрующих агентов, например тетрафторобората нитрония [NO2]+BF4¯при низких температурах, может привести к продуктам нитрования по атому азота (N-нитроариламинам).
Для получения продуктов нитрования в орто- ипара-положения ароматического кольца необходимо предварительно ввестиацильную защиту, которая заключается в предварительном ацилировании аминогруппы (см. также гл. 10.6.3.3). Продукты ацилирования,N-ацилариламины, не обладают оснóвными свойствами, и поэтому в кислой среде электронодонорная активность атома азота сохраняется, хотя величина +М-эффекта будет значительно меньше, чем у исходного амина, так как ацильная группа также вступает в сопряжение с аминогруппой. В связи с этим уменьшается реакционная способность ароматического кольца.

При нитровании нитрующей смесью N-ацилариламинов получается смесьо- ип-изомеров. После проведения нитрования ацильную защиту снимают.

Сульфирование. Взаимодействие анилина с концентрированной серной кислотой при нагревании до 450—460Кприводит к образованию сульфаниловой кислоты (метод «запекания»):

Образование исключительно п-изомера объясняется уменьшением электронодонорной активности аминогруппы в промежуточнойN-сульфокислоте (аналогично применению ацильной защиты при бромировании и нитровании) и большим пространственным эффектом заместителя в этом соединении.
Взаимодействие со слабыми электрофилами. Повышение активности бензольного кольца ароматических аминов делает возможным взаимодействие с такими слабыми электрофилами, как альдегиды, соли диазония и некоторыми другими. Реакция с формальдегидом может рассматриваться как типичная реакцияSEпо отношению к амину или как реакцияAdNпо отношению к альдегиду:

Образующийся продукт присоединения, являющийся ароматическим спиртом, также может проявлять электрофильные свойства и вступать во взаимодействие со следующей молекулой амина. По отношению к ароматическому спирту это уже будет нуклеофильное замещение (механизм реакции, скорее всего, SN1):

п,п-бис-(диметиламино)-дифенилметан
Взаимодействие ароматических аминов с солями диазония будет рассмотрено далее, в свойствах диазосоединений.
10.6.3.2. Кислотно-оснόвные свойства
Для аминов в целом (и ароматических, и алифатических) характерны слабые кислотные свойства. Это NH-кислоты, и поэтому отщепление катиона водорода происходит труднее, чем в случае OH-кислот, из-за меньшей электроотрицательности атома азота по сравнению с кислородом.
В
молекулах ароматических аминов по
причине р--сопряжения
и сильного смещения электронной плотности
с атома азота на бензольное к ольцоN–H-связь
более полярна, чем в алифатических
аминах. Поэтому кислотность ароматических
аминов несколько выше, однако она
остаётся достаточно низкой, и кислотные
свойства проявляются только по отношению
к таким реагентам, как активные металлы,
металлорганические соединения или же
металлические производные аммиака и
алифатических аминов. Например:
ольцоN–H-связь
более полярна, чем в алифатических
аминах. Поэтому кислотность ароматических
аминов несколько выше, однако она
остаётся достаточно низкой, и кислотные
свойства проявляются только по отношению
к таким реагентам, как активные металлы,
металлорганические соединения или же
металлические производные аммиака и
алифатических аминов. Например:
![]()
![]()
Бóльшую кислотность ароматических аминов по сравнению с алифатическими можно объяснить также устойчивостью образующегося аниона, в котором отрицательный заряд делокализован с участием -электронной системы бензольного кольца:

Оснóвные свойства у ароматических аминов, наоборот, слабее выражены, чем у алифатических аналогов. Причина этого та же, что и в случае кислотных свойств: участие неподелённой электронной пары атома азота в сопряжении с -электронной системой бензольного кольца и, как следствие, пониженная электронная плотность на атоме азота по сравнению с аммиаком и алифатическими аминами. Так, значение константы основности для метиламина CH3NH2 примерно в 107 раз выше константы основности анилина: рКb метиламина равно 2.3, анилина — 9.4 (для сравнения: рКb аммиака равно 4.8).
Таким образом, ароматические амины дают соли только с сильными кислотами, например:
Ar-NH2
+ H2SO4
![]() [Ar-NH3]+
HSO4¯
[Ar-NH3]+
HSO4¯
Однако такие соли, являющиеся солями сильных кислот и слабых оснований, легко гидролизуются.
Введение заместителей в ароматическое кольцо влияет на оснóвные свойства ароматических аминов. Электроноакцепторные заместители за счёт более полной делокализации неподелённой электронной пары атома азота ещё сильнее уменьшают оснóвные свойства, а электронодонорные заместители, наоборот, повышают основность ароматических аминов, так как в этом случае их электронный эффект препятствует делокализации неподелённой пары электронов азота. Особенно сильно такое влияние проявляется в о- и п-положениях бензольного кольца.

10.6.3.3. Нуклеофильные свойства
Ароматические амины могут проявлять нуклеофильные свойства за счёт атома азота. Однако по сравнению с алифатическими аминами в данном случае нуклеофильность будет понижена вследствие сопряжения, так же как и понижены оснóвные свойства. Тем не менее аналогично алифатическим аминам (гл. 3.7.3) анилин и его производные вступают в реакции алкилирования, ацилирования, взаимодействия с азотистой кислотой, в изонитрильную реакцию, а также в реакции арилирования и образования оснований Шиффа*.
Алкилирование. В данной реакции субстратами могут являться галогеналканы, диалкилсульфаты,п-толуолсульфонаты, реже — спирты. Во всех случаях это типичная реакция нуклеофильного замещения у насыщенного атома углерода, механизм которой приведён в главе 3.1.1. Различия наблюдаются только в природе уходящей группы. Например, для метилирования можно использовать метилйодид, диметилсульфат или метил-п-толуолсульфонат в щелочной среде, как показано в этих некоторых схемах:


Алкилирование обычно идёт дальше с образованием смеси вторичных, третичных аминов и солей четвертичного аммония.
В случаях алкилирования спиртами реакцию проводят в газовой фазе в присутствии кислот. При этом обычно получаются третичные амины:
![]()
Арилирование. Эти реакции должны протекать в более жёстких условиях, чем реакции алкилирования, так как предполагается замещение галогена в ароматическом кольце, а это означает протекание реакции по ариновому механизму (или механизму SN2аром, если субстрат активирован). Однако достаточно легко реакции могут протекать в тех случаях, когда в ароматическом кольце амина имеются электронодонорные заместители (в орто- и пара-положениях), повышающие его нуклеофильность, а в молекуле арилгалогенида (также в орто- и пара-положениях) — электроноакцепторные группы. Например:


При нагревании до 500 К анилина с его солянокислой солью получают дифениламин. Эта реакция становится возможной за счёт наличия в субстрате очень сильного электроноакцептора аммонийной группы:
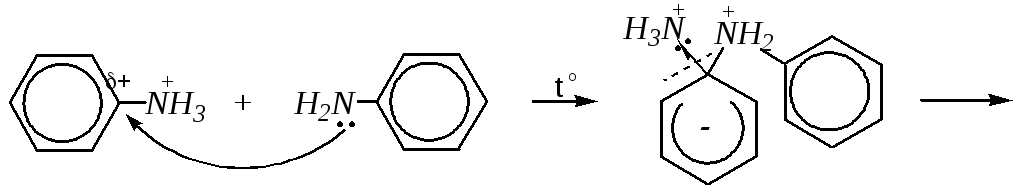

Ацилирование. Реакции ацилирования ароматических аминов — это реакции взаимодействия этих соединений с карбоновыми кислотами и их производными, являющимися ацильными агентами. Такие реакции производных карбоновых кислот рассматривались в главе 6.4.4.2. В данном случае ацилирование проводят ангидридами, хлорангидридами кислот и самими карбоновыми кислотами, продуктами при этом являются N-ариламиды:

В целом ацилирование ариламинов протекает медленнее, чем ацилирование алифатических аминов.
Взаимодействие аминов с хлорангидридами аренсульфокислот — реакции, аналогичные ацилированию. Действие арилсульфохлоридов на первичные, вторичные и третичные амины приводит к разным продуктам. Так, первичные и вторичные амины легко образуют сульфамиды, третичные — в реакцию не вступают:


При этом аренсульфамид, полученный из первичного амина, обладает ярко выраженной NH-кислотностью и потому растворяется в водных растворах щелочей:

А сульфамид, образованный из вторичного амина и не содержащий атомов водорода в амидной группе, в щелочах не растворяется. Такое различное отношение первичных, вторичных и третичных ароматических аминов к аренсульфохлоридам лежит в основе разделения смеси аминов.
Образование оснований Шиффа. Первичные ароматические амины при взаимодействии с ароматическими альдегидами образуют основания Шиффа (называемые также анилами, или шиффовыми основаниями):

Механизм реакции нуклеофильного присоединения аминов к карбонильным соединениям рассмотрен в главе 6.1.4.1. Образующиеся в общем случае при таком присоединении азометины малоустойчивы и могут гидролизоваться с образованием исходных веществ, в данном случае шиффовы основания стабилизированы сопряжением -электронных систем двух ароматических колец и -связи между этими кольцами (---сопряжение). Поэтому такие соединения устойчивы к щелочам, но могут гидролизоваться в кислой среде.
В биохимических процессах образование оснований Шиффа играет существенную роль. Например, через их образование осуществляется биосинтез аминокислоты триптофана, осуществляется связывание ретиналя с белком опсином — механизм зрения, а также и другие процессы.
Взаимодействие с азотистой кислотой. Как и для алифатических аминов, взаимодействие ариламинов с азотистой кислотой приводит к разным продуктам для первичных, вторичных и третичных аминов, поэтому данную реакцию можно использовать для различия этих аминов. Механизм нитрозирования аминов с участием азотистой кислоты подробно рассмотрен в главах 3.7.3.5 и 10.7.2. При этом из первичных аминов образуются соли арендиазония:
 ,
,
из вторичных аминов — N-нитрозоамины:
 ,
,
а из третичных аминов — п-нитрозосоединения:
 .
.
Однако реакция нитрозирования третичных аминов — это проявление нуклеофильных свойств за счёт ароматического кольца, и по отношению к амину данная реакция является электрофильным замещением атома водорода в ароматическом кольце.
Изонитрильная реакция. Как и алифатические амины, первичные ароматические амины дают изонитрильную реакцию (гл. 3.7.3.6), заключающуюся во взаимодействии аминов с хлороформом в присутствии щёлочи:

Протекание реакции сопровождается неприятным запахом образующегося карбиламина (арилизоцианида), поэтому первичные амины могут быть обнаружены с помощью этой реакции.
10.6.3.4. Окисление
При взаимодействии ариламинов с сильными окислителями (например, NaOCl, CrO3) происходит отрыв электрона и образование катион-радикалов, которые далее превращаются в красители:
![]()
Аминогруппу также можно окислить до нитрозогруппы, применяя пероксисерную кислоту (кислоту Каро) H2SO5, и до нитрогруппы — трифторпероксиуксусной кислотой CF3COOOH, азотной кислотой или перманганатом калия:
![]()
Данную реакцию можно использовать как способ получения нитрозо- или нитросоединений соответственно.
