
- •Глава 1. Основы теоретических представлений в органической химии
- •1.1. Учение а.М. Бутлерова
- •1.2. Теория гибридизации атомных орбиталей
- •1.3. Ковалентная связь
- •1.3.3. Водородные связи
- •1.4. Теория электронных смещений
- •1.5. Классификация и номенклатура органических соединений
- •1.5.1. Заместительная номенклатура
- •1.5.2. Радикало-функциональная номенклатура
- •1.5.4. Рациональная Номенклатура
- •1.6. Представление о Кислотно-оснÓвных свойствах органических соединений
- •1.7. Основы стереохимии
- •1.7.1. Оптическая изомерия
- •1.7.2. Геометрическая изомерия
- •1.7.3. Конформационная изомерия
- •1.8. Классификация органических реакций. Понятие о механизме реакций. Растворители и катализаторы
- •1.9. Методы идентификации органических соединений. Основные физические константы
- •1.10. Методы разделения и очистки органических веществ
- •1.10.1. Разделение твёрдых смесей и очистка твёрдых веществ
- •1.10.2. Разделение жидких смесей и очистка жидкостей
- •1.11. Представление о биологическом действии и метаболизме органических соединений
- •Глава 2. Алканы
- •2.1. Номенклатура. Изомерия
- •2.2. Строение
- •2.3. Физические свойства
- •2.4. Химические свойства
- •2.4.1. Реакции радикального замещения
- •2.4.2. Реакции дегидрирования и разложения
- •2.4.3. Реакции изомеризации
- •Способы получения и природные источники
- •2.6. Применение и физиологическая роль
- •Глава 3. Функциональные производные алканов
- •3.1. ОбщноСть Химических свойств
- •3.1.1. Реакции нуклеофильного замещения
- •3.1.2. Реакции отщепления (элиминирования)
- •3.2. Галогеналканы
- •3.2.1. Классификация, номенклатура, изомерия
- •3.2.2. Строение и свойства
- •3.2.3. Способы получения
- •3.2.4. Полигалогеналканы
- •3.2.5. Физиологическая роль и Важнейшие представители
- •3.3. Насыщенные спирты
- •3.3.1. Классификация, номенклатура, изомерия
- •3.3.2. Строение и физические свойства
- •3.3.3. Химические свойства
- •3.3.4. Способы получения
- •3.3.5. Многоатомные спирты
- •3.3.6. Физиологическое действие
- •3.3.7. Важнейшие представители
- •3.4. Простые насыщенные эфиры
- •3.4.1. Номенклатура и изомерия
- •3.4.2. Физические и химические свойства
- •3.4.3. Способы получения
- •3.4.4. Циклические простые эфиры
- •3.4.5. Физиологическая роль и Важнейшие представители
- •3.5. Эфиры минеральных кислот
- •3.5.1. Эфиры серной кислоты
- •3.5.2. Эфиры фосфорной кислоты
- •3.6. Тиоспирты и тиоэфиры
- •3.7. Насыщенные амины
- •3.7.1. Классификация, номенклатура, изомерия
- •3.7.2. Физические свойства
- •3.7.3. Строение и химические свойства
- •3.7.4. Способы получения
- •3.7.5. Физиологическая роль и Важнейшие представители
- •3.8. Нитроалканы
- •3.8.1. Строение
- •3.8.2. Свойства
- •3.8.3. Способы получения
- •3.8.4. Физиологическое действие и Важнейшие представители
- •3.9. Кремний-, фосфор- и мышьякорганические соединения
- •3.9.1. Кремнийорганические соединения
- •3.9.2. Фосфорорганические соединения
- •3.9.3. Мышьякорганические соединения
- •Глава 4. Непредельные углеводороды
- •4.1. ОБщность строения и химических свойств
- •4.1.1. Реакции электрофильного присоединения
- •4.1.2. Реакции радикального присоединения
- •4.1.3. Реакции радикального замещения
- •4.1.4. Другие реакции
- •4.2. Этиленовые углеводороды
- •4.2.1. Номенклатура, изомерия
- •4.2.2. Физические свойства
- •4.2.3. Химические свойства
- •4.2.4. Способы получения
- •4.2.5. Физиологическое действие и Важнейшие представители
- •4.3. Диеновые (и полиеновые) углеводороды
- •4.3.1. Классификация, номенклатура
- •4.3.5. Способы получения
- •4.3.6. Важнейшие представители
- •4.4. Ацетиленовые углеводороды
- •4.4.1. Номенклатура, изомерия
- •4.4.2. Особенности строения и свойств
- •4.4.3. Способы получения
- •4.4.4. Физиологическое действие и Важнейшие представители
- •Глава 5. Функциональные производные непредельнЫх углеводороДов
- •5.1. ОБщность строения и химических свойств
- •5.1.1. Классификация
- •5.1.2. Субстраты винильного типа
- •5.1.3. Субстраты аллильного типа
- •5.2. Галогеналкены
- •5.2.1. Винилгалогениды
- •5.2.2. Аллилгалогениды
- •5.2.3. Способы получения
- •5.2.4. Важнейшие представители
- •5.3. Непредельные спирты и эфиры
- •5.3.1. Виниловый спирт и его эфиры
- •5.3.2. Аллиловый и пропаргиловый спирты
- •5.3.3. Способы получения
- •5.3.4. Важнейшие представители
- •Глава 6. Алифатические альдегиды, кетоны и карбоновые кислоты
- •6.1. Насыщенные альдегиды и кетоны
- •6.1.1. Изомерия, номенклатура
- •6.1.2. Строение карбонильной группы
- •6.1.3. Физические свойства
- •6.1.4. Химические свойства
- •6.1.5. Способы получения
- •6.1.6. Физиологическая роль
- •6.1.7. Важнейшие представители
- •6.2. Непредельные альдегиды и кетоны
- •6.2.1. Кетен
- •6.2.2. Непредельные карбонильные соединения
- •Примерами соединений с сопряжёнными -связями являются
- •6.2.3. Важнейшие представители
- •6.3. Дикарбонильные соединения
- •6.3.3. Важнейшие представители
- •6.4. Насыщенные монокарбоновые кислоты и их производные
- •6.4.1. Номенклатура
- •6.4.2. Строение функциональной группы
- •6.4.3. Физические свойства
- •6.4.4. Химические свойства
- •6.4.5. Способы получения
- •6.4.6. Пероксикарбоновые кислоты и ацилпероксиды
- •6.4.7. Физиологическая роль и Важнейшие представители
- •6.5. Непредельные монокарбоновые кислоты
- •6.5.1. Номенклатура, изомерия
- •6.5.2. Строение
- •6.5.3. Химические свойства
- •6.5.4. Способы получения
- •6.5.5. Физиологическая роль и Важнейшие представители
- •6.5.6. Омыляемые липиды
- •6.6. Дикарбоновые кислоты и их производные
- •6.6.1. Особенности химического поведения
- •6.6.2. Малоновый эфир и синтезы на его основе
- •2 H5c2ooc-ch2-cooc2h5
- •2 H5c2ooc-ch2-cooc2h5
- •6.6.3. Способы получения
- •2 Rooc-(ch2)n-сoo¯ 2 rooc-(ch2)n-сoo rooc-(ch2)2n-coor hooc-(ch2)2n-cooh
- •6.6.4. Важнейшие представители
- •6.7. Гидроксикислоты
- •6.7.1. Классификация, номенклатура, изомерия
- •6.7.2. Химические свойства
- •6.7.3. Способы получения
- •6.7.4. Физиологическая роль и Важнейшие представители
- •6.8. Оксокислоты
- •6.8.1. Особенности химического поведения
- •6.8.2. Ацетоуксусный эфир и синтезы на его основе
- •6.8.3. Способы получения
- •6.8.4. Важнейшие представители
- •6.9. Аминокарбоновые кислоты. Пептиды
- •6.9.1. Классификация, номенклатура, изомерия аминокислот
- •6.9.2. Строение, физические и Химические свойства
- •6.9.3. Способы получения аминокислот
- •6.9.4. Важнейшие представители аминокислот
- •6.9.5. Пептиды
- •Глава 7. Углеводы
- •7.1. Моносахариды
- •7.1.1. Изомерия, номенклатура
- •7.1.2. Химические свойства
- •7.1.3. Важнейшие представители моносахаридов и их производных
- •7.2. Олигосахариды
- •7.2.1. Классификация и номенклатура дисахаридов
- •7.2.2. Химические свойства дисахаридов
- •7.2.3. Важнейшие представители дисахаридов
- •7.3. Полисахариды
- •7.3.1. Целлюлоза
- •7.3.2. Амилоза и амилопектин
- •7.3.3. Гликоген
- •7.3.4. Декстраны
- •7.3.5. Хитин
- •7.3.6. Пектовая кислота
- •7.3.7. Гетерополисахариды
- •Глава 8. Алициклические углеводороды и их производные
- •8.1. Номенклатура моно- и бициклических соединений
- •8.2. Пространственное строение и изомерия циклоалканов
- •8.2.1. Циклопропан
- •8.2.2. Циклобутан
- •8.2.3. Циклопентан
- •8.2.4. Циклогексан
- •8.3. Химические свойства
- •8.3.1. Реакции циклопропана, циклопропена и их производных
- •8.3.2. Реакции циклобутана и его производных
- •8.3.3. Реакции средних циклов
- •8.3.4. Реакции изомеризации цикла
- •8.4. Способы получения циклоалканов
- •8.5. Терпены и терпеноиды. Каротиноиды
- •8.5.1. Ациклические терпены и терпеноиды
- •8.5.2. Моноциклические терпены и терпеноиды
- •8.5.3. Бициклические терпены и терпеноиды
- •8.5.4. Каротиноиды
- •8.6. Физиологическая роль и важнейшие представители
- •8.7. Стероиды
- •Глава 9. Бензол. Ароматичность. Углеводороды ряда бензола
- •9.1. Строение бензола
- •Тепловой эффект реакции гидрирования бензола составляет
- •9.2. Номенклатура и изомерия аренов
- •9.3. Строение аренов
- •9.3.1. Строение толуола
- •9.3.2. Строение винилбензола
- •9.4. Физические свойства
- •9.5. Химические Свойства
- •9.5.1. Химические свойства бензола
- •9.5.2. Химические свойства аренов
- •9.6. Способы получения
- •9.7. Физиологическое действие и важнейшие представители аренов
- •9.8. Небензоидные ароматические системы
- •Глава 10. Функциональные производные углеводородов ряда бензола
- •10.1. Общность строения и свойств монозамещённых бензолов
- •10.1.1. Электронные эффекты заместителей
- •10.1.2. Реакции электрофильного замещения
- •10.1.3. Реакции нуклеофильного замещения
- •10.2. Галогенарены
- •10.2.1. Классификация, номенклатура
- •10.2.2. Строение арилгалогенидов
- •10.2.3. Физические свойства
- •10.2.4. Химические свойства
- •10.2.5. Способы получения
- •10.2.6. Важнейшие представители
- •10.3. Ароматические сульфокислоты
- •10.3.1. Номенклатура
- •10.3.2. Строение
- •10.3.3. Физические и химические свойства
- •10.3.4. Способы получения
- •10.3.5. Производные сульфокислот
- •10.3.6. Медико-биологическое значение и Важнейшие представители
- •10.4. Ароматические нитросоединения
- •10.4.1. Строение нитробензола
- •10.4.2. Физические свойства
- •10.4.3. Химические свойства
- •10.4.4. Способы получения
- •10.4.5. Физиологическое действие и Важнейшие представители
- •10.5. Фенолы. Ароматические спирты. Хиноны
- •10.5.1. Классификация, номенклатура, изомерия фенолов и ароматических спиртов
- •10.5.2. Строение фенола и бензилового спирта
- •Ароматические амины и продукты неполного восстановления нитросоединений
- •10.6.1. Классификация, номенклатура, изомерия ароматических аминов
- •10.6.2. Строение анилина
- •10.6.3. Физические и химические свойства ароматических аминов
- •10.6.4. Способы получения ароматических аминов
- •10.6.5. Важнейшие представители ароматических аминов
- •10.6.6. Продукты неполного восстановления нитросоединений
- •10.7. Ароматические диазосоединения
- •10.7.2. Механизм образования солей арендиазония и строение катиона бензолдиазония
- •10.7.3. Амфотерность диазосоединений
- •10.7.4. Реакции солей арендиазония
- •10.8. Ароматические альдегиды и кетоны
- •10.9. Ароматические карбоновые кислоты и их производные
- •10.10. Физиологическая роль функциональных производных бензола
- •Глава 11. Полициклические ароматические углеводороды и их производные
- •11.1. Классификация углеводородов с конденсированными циклами
- •11.2. Нафталин
- •11.2.1. Строение, изомерия, номенклатура
- •11.2.2. Свойства
- •11.2.3. Способы получения
- •11.2.4. Важнейшие представители
- •11.3. Антрацен
- •11.3.1. Строение, изомерия, номенклатура
- •11.3.2. Свойства
- •Продукт исчерпывающего гидрирования (пергидроантрацен) можно получить, проводя реакцию в жёстких условиях с применением металлических катализаторов.
- •11.3.3. Способы получения
- •11.3.4. Важнейшие представители
- •11.4. Фенантрен
- •11.4.1. Строение, изомерия, номенклатура
- •11.4.2. Свойства
- •11.4.3. Способы получения
- •11.5. Физиологическое действие полициклических углеводородов
- •Глава 12. Гетероциклические соединения
- •12.1. Классификация и номенклатура
- •12.2. Пятичленные гетероциклические
- •12.2.1. Номенклатура пиррола, фурана и тиофена и их производных
- •12.2.2. Строение пиррола, фурана и тиофена
- •12.2.3. Физические и химические свойства пиррола, фурана и тиофена
- •12.2.4. Особенности индола
- •12.2.5. Способы получения пиррола, фурана, тиофена, индола
- •12.2.6. Важнейшие представители и медико-биологическое значение
- •12.3. Пятичленные гетероциклические
- •12.3.1. Номенклатура имидазола и пиразола
- •12.3.2. Строение имидазола и пиразола
- •12.3.3. Физические и химические свойства имидазола и пиразола
- •12.3.4. Способы получения
- •12.3.5. Важнейшие представители и медико-биологическое значение
- •12.4. Шестичленные гетероциклические
- •12.4.1. Номенклатура пиридина и его производных
- •12.4.2. Строение пиридина
- •12.4.3. Химические свойства пиридина
- •Но если оба -положения заняты, то замещается водород в-положении. При нагревании с избытком амида натрия можно получить 2,6-диаминопиридин.
- •12.4.4. Особенности химического поведения пиколинов и функциональных производных пиридина
- •12.4.5. Хинолин и изохинолин
- •12.4.7. Способы получения
- •Реакция аналогична получению бензола, протекает при высоких температурах, но представляет только теоретический интерес.
- •12.4.8. Важнейшие представители и медико-биологическое значение
- •12.5. Шестичленные гетероциклические
- •12.5.1. Строение и свойства диазинов
- •12.5.2. Пурин
- •12.5.3. Способы получения
- •12.5.4. Важнейшие представители и медико-биологическое значение
- •12.5.5. Нуклеозиды, нуклеотиды и нуклеиновые кислоты
- •12.6. Алкалоиды
7.1.2. Химические свойства
Ввиду того, что находящиеся в таутомерном равновесии разные формы моносахаридов содержат сильно отличающиеся по характеру функциональные группы, химические свойства этих веществ будут определяться наличием этих таутомерных форм с присущими им функциональными группами. Оксоформы углеводов содержат оксогруппу (альдегидную или кетонную), поэтому моносахариды могут вступать в реакции с участием оксогруппы именно в открыто-цепной форме (оксоформе). Наоборот, циклические формы, являясь полуацеталями, проявляют свойства этого класса соединений, вступая в реакции с участием полуацетальной гидроксильной группы. А так как в молекулах углеводов имеются и гидроксогруппы многоатомных спиртов (как в оксоформах, так и в циклических формах), то свойства этого класса соединений моносахариды проявляют, находясь в любой таутомерной форме.
7.1.2.1. Реакции открыто-цепных форм
Моносахариды, являясь полигидроксикарбонильными соединениями, вступают в реакции с участием карбонильной группы, прежде всего это реакции нуклеофильного присоединения. Примерами могут служить реакции с гидроксиламином, с гидросульфитом натрия.
-

D-рибоза

оксим D-рибозы

бисульфитное производное D-рибозы
Аналогично реакция протекает с эквимолекулярным количеством фенилгидразина. Однако с избытком этого реагента реакция протекает иначе. С первой молекулой образуются обычные для карбонильных соединений фенилгидразоны:
![]() ,
,
которые при нагревании вступают в SN-реакцию со второй молекулой фенилгидразина, а в последующем дегидрировании принимает участие третья молекула реагента. При этом образуются озазоны. Нетрудно видеть, что эпимерные манноза и глюкоза образуют одинаковые продукты:
|
|
|
|
фенилгидразон D-маннозы
| |
|
фенилгидразон D-глюкозы |

Озазоны — жёлтые кристаллические вещества, структура их молекул стабилизирована длинной цепью сопряжения и внутримолекулярной водородной связью.
Образование озазонов используют для идентификации углеводов. Для каждого углевода характерна определённая скорость образования озазона, например: озазон фруктозы выделяется из раствора за 2 мин., озазон глюкозы — за 4—5 мин., озазон ксилозы — за 7 мин. и т. д. Впервые озазоны синтезированы Э. Фишером в 1887 г.
При нагревании со щёлочью происходит изомеризация альдоз в кетозы (и обратно) и в эпимерные альдозы через енольную форму. Например, превращения D-глюкозы, D-фруктозы и D-маннозы:
|
| ||
|
D-глюкоза |
D-фруктоза |
D-манноза |
Реакции восстановления оксогруппы также возможны только в оксоформе, и они приводят к соответствующим многоатомным спиртам. Восстановление проводят водородом на металлических катализаторах. При этом из кетоз образуется смесь эпимерных спиртов. Например:

D-рибозаD-рибит

D-глюкозаD-глюцит

D-фруктозаD-глюцитD-маннит
Данные многоатомные спирты называют с использованием суффикса -ит.
Альдозы легко подвергаются окислению по свободной альдегидной группе. Так, под действием мягких окислителей, например бромной воды, образуются альдоновые кислоты, которые обычно существуют в виде - или -лактонов.

D-глюконовая кислота и её-лактон
Кроме бромной воды для получения альдоновых кислот могут использоваться реактив Толленса (реакция серебряного зеркала), свежеосаждённый гидроксид меди (II) (или гидроксид меди в виде реактива Фелинга) (гл. 4.4.2 и 6.1.4.3). Окисление альдоз до альдоновых кислот протекает обычно в кислой или нейтральной среде. Однако при использовании для этих целей разбавленной азотной кислоты окисление может пойти дальше (в зависимости от концентрации кислоты) и образуются «аровые» (полное общее название гликаровые) кислоты, в молекулах которых окислены оба концевых атома углерода. Например:
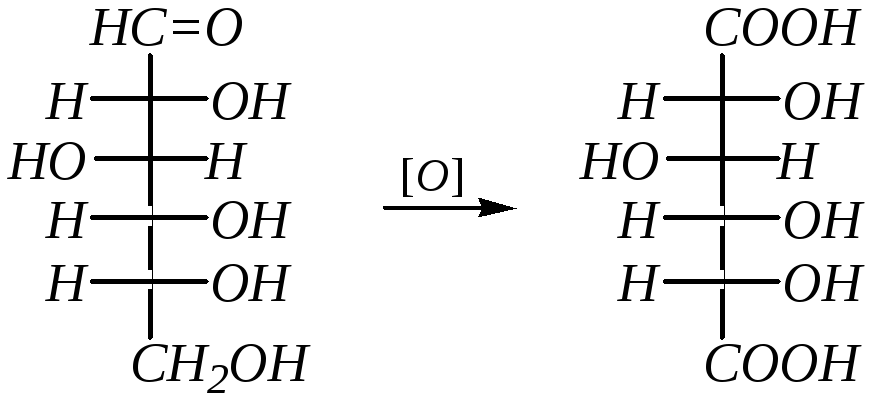
D-глюкаровая кислота
А при окислении только первичноспиртовой группы могут быть получены альдегидокарбоновые кислоты, так называемые уроновые кислоты. Но такое окисление обычно возможно только для циклических форм моносахаридов с защищённой полуацетальной группой, поэтому будет рассмотрено несколько позже.
Окисление в щелочной среде сопровождается изомеризацией альдоз в кетозы и обратно, и в том числе эпимеризацией, например, глюкозы в маннозу и обратно (см. выше). Поэтому в этих условиях могут окисляться и кетозы, предварительно изомеризуясь, образуя альдоновые кислоты. Например, использование реактива Толленса для окисления D-глюкозы (или D-фруктозы) приводит к получению не только D-глюконовой кислоты, а смеси продуктов, содержащей в том числе и D-манноновую кислоту.

7.1.2.2. Реакции циклических форм
Как уже было показано выше, полуацетальные (гликозидные) гидроксильные группы присутствуют в циклических (полуацетальных) формах молекул моносахаридов. Поэтому превращения циклических форм связаны со свойствами полуацеталей вообще и с особенностями поведения таких гидроксогрупп в частности, так как помимо полуацетального гидроксила в молекулах моносахаридов присутствует несколько спиртовых гидроксильных групп.
Полуацетальная гидроксильная группа обладает повышенной реакционной способностью: легко реагирует, например, со спиртами в условиях кислотного катализа с образованием полных ацеталей, называемых также в химии углеводов гликозидами. Это превращение находит отражение и в названии продукта: суффикс с окончанием -оза заменяется суффиксом -озид.

(),D-глюкопираноза алкил-(),D-глюкопиранозид
(В данном случае в реакцию вступает либо смесь - и -аномеров, либо одна из этих циклических форм, неважно какая. Образуется при этом смесь аномеров).
Несахарный фрагмент гликозида называют агликоном. Если агликон связан с остатком моносахарида через атом кислорода, то такой гликозид называют О-гликозидом, если через атом азота — N-гликозидом. (Например, при реакциях с аминами образуются N-гликозидные связи.)
Для получения О-алкилгликозидов обычно используют спирты, насыщенные сухим хлороводородом. Механизм реакции здесь, скорее всего, SN1 так же, как и при образовании полных ацеталей из простых альдегидов и кетонов (гл. 6.1.4.1), так как промежуточный карбокатион стабилизирован р-р-сопряжением с участием неподелённой пары электронов атома кислорода пиранозного кольца:

(),D-глюкопираноза


алкил-,D-глюкопиранозид алкил-,D-глюкопиранозид
Образующиеся гликозиды, являясь полными ацеталями, гидролизуются в кислой среде, но устойчивы при действии разбавленных щелочей:

В условиях реакции алкилирования спиртов при обработке их щелочными растворами диметилсульфата (CH3)2SO4 (метилирование) или йодалканов образуются простые эфиры с участием всех спиртовых гидроксогрупп и гликозидного гидроксила тоже. Эта реакция типичное нуклеофильное замещение, в котором субстратами являются диметилсульфат или галогеналканы, протекающее, видимо, по механизму, близкому к SN2. Например:

(),D-глюкопираноза метил-2,3,4,6-тетра-О-метил-,D-глюкопиранозид
и метил-2,3,4,6-тетра-О-метил-,D-глюкопиранозид
Образующиеся простые эфиры гидролизу не подвергаются, а гликозидная группа легко гидролизуется в кислой среде, аналогично рассмотренному выше.

2,3,4,6-тетра-О-метил-,D-глюкопираноза
и 2,3,4,6-тетра-О-метил-,D-глюкопираноза
Реакции ацилирования моносахаридов протекают с участием ангидридов или галогенангидридов карбоновых кислот. При этом также образуется смесь - и -аномеров. Образующиеся сложные эфиры полностью гидролизуются как в кислой, так и в щелочной среде. Например:
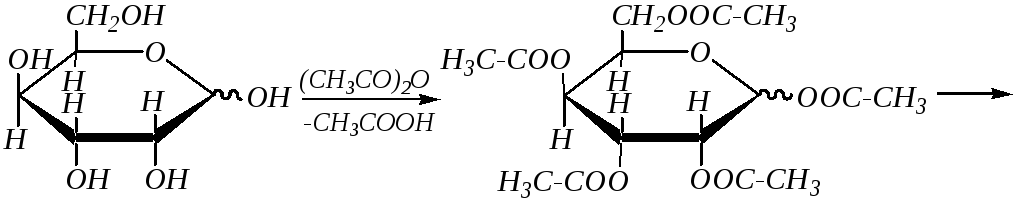
(),D-гулопираноза ацетил-2,3,4,6-тетра-О-ацетил-(),D-гулопиранозид
или (),D-гулопираноза пентаацетат

,D-гулопираноза и ,D-гулопираноза
Окисление первичноспиртовой группы (без участия альдегидной группы альдоз), протекающее в фиксированных циклических формах, т.е. для гликозидов моносахаридов, приводит к образованию уроновых кислот. Например:

этил-(),D-глюкопиранозид

(),D-глюкуроновая кислота
7.1.2.3. Реакции дегидратации
При нагревании моносахаридов с минеральными кислотами может происходить внутримолекулярная дегидратация. В частности, ксилоза в водных растворах серной кислоты теряет три молекулы воды, и в результате образуется фурфурол (2-фуранкарбальдегид).

D-ксилоза фурфурол
Подобные превращения с образованием гидроксиметилфурфурола могут происходить с некоторыми альдо- и кетогексозами.
7.1.2.4. Реакции удлинения и укорочения углеродной цепи
Реакции постепенного наращивания углеродной цепи и, наоборот, постепенного укорочения её (т.е. переходы триоза тетроза пентоза гексоза гептоза и обратно) имеют большое значение для установления строения моносахаридов.
Углеродная цепь наращивается циангидринным методом. Например, при превращении альдопентозы в альдогексозу химизм можно представить в следующем виде:
|
|
|
|
D-арабиноза | |
|
|
нитрилы D-глюконовой и D-манноновой кислот |

лактоны D-глюконовой иD-манноновой кислот

D-глюкозаD-манноза
Укорочение углеродной цепи альдоз происходит в результате окисления альдегидной группы и последующего окислительного декарбоксилирования образовавшейся альдоновой кислоты с помощью специфического реагента. Например:

D-глюкозаD-глюконовая кислотаD-арабиноза







