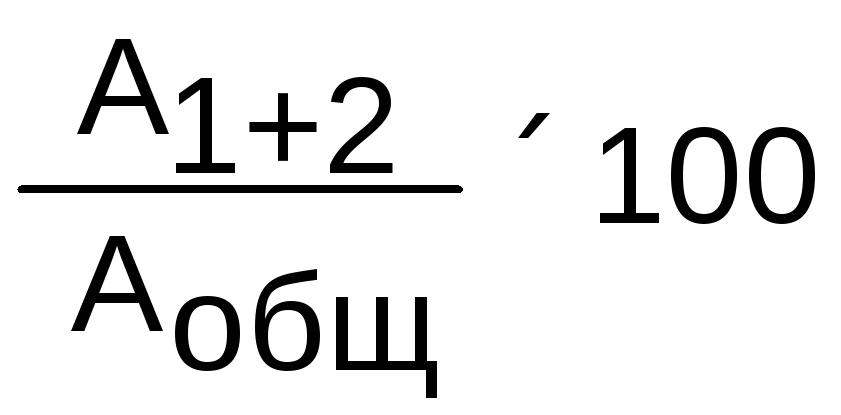- •Для студентов лечебного и педиатрического факультетов
- •Оглавление
- •Раздел 1. Строение, свойства и функции белков
- •Лабораторная работа 1
- •Лабораторная работа 2
- •Оформление работы
- •Практическое значение
- •Тема 1.2. Структура и физико-химические свойства белков Актуальность
- •Вопросы для самоподготовки
- •Темы для реферативных сообщений
- •Клинико-диагностическое значение
- •Практическое значение
- •Оформление работы
- •Исследование денатурации белков при нагревании в условиях различной рН Проведение анализа
- •Оформление работы
- •Тема 1.3. Классификация белков. Строение и функции белков в организме. Сложные белки Актуальность
- •Вопросы для самоподготовки
- •Темы для реферативных сообщений
- •Анализ химического состава гликопротеинов Материал исследования
- •Проведение анализа
- •Оформление работы
- •Тестовые задания
- •Ситуационные задачи
- •Раздел 2. Строение, классификация и роль витаминов Тема 2.1. Жирорастворимые витамины Актуальность
- •Вопросы для самоподготовки
- •Темы для реферативных сообщений
- •Тема 2.2. Водорастворимые витамины Актуальность
- •Вопросы для самоподготовки
- •Темы для реферативных сообщений
- •Качественные реакции на аскорбиновую кислоту
- •Оформление работы
- •Тестовые задания
- •Ситуационные задачи
- •Раздел 3. Энзимология Тема 3.1. Строение и свойства ферментов. Регуляция активности ферментов Актуальность
- •Вопросы для самоподготовки
- •Темы для реферативных сообщений
- •Проведение реакции.
- •Оформление работы
- •Оформление работы
- •Оформление работы
- •Обнаружение специфичности действия амилазы слюны Принцип
- •Проведение реакции
- •Оформление работы
- •Лабораторная работа 4 Влияние активаторов и инактиваторов на активность амилазы Принцип
- •Реактивы
- •Материал исследования
- •Проведение реакции
- •Оформление работы
- •Темы для реферативных сообщений
- •Нормальные величины
- •Клинико-диагностическое значение
- •Оформление работы
- •Тестовые задания
- •Ситуационные задачи
- •Контрольные вопросы к итоговому занятию
- •Вопросы для самоподготовки
- •Тестовые задания
- •Ситуационные задачи
- •Раздел 5. Обмен аминокислот и белков Тема 5.1. Внешний обмен белков Актуальность
- •Вопросы для самоподготовки
- •Темы для реферативных сообщений
- •Реактивы
- •Материал исследования
- •Проведение анализа
- •Оформление работы
- •Лабораторная работа 3
- •Оформление работы
- •Темы для реферативных сообщений
- •Лабораторная работа 1 Определение активности аминотрансфераз сыворотки крови Принцип
- •Реактивы
- •Материал исследования
- •Проведение анализа
- •Нормальные величины
- •Клинико-диагностическое значение
- •Оформление работы
- •Темы для реферативных сообщений
- •Нормальные величины
- •Клинико-диагностическое значение
- •Оформление работы
- •Нормальные величины
- •Клинико‑диагностическое значение
- •Оформление работы
- •Темы для реферативных сообщений
- •Лабораторная работа 1 Определение аминокислот методом распределительной хроматографии на бумаге
- •Принцип
- •Реактивы
- •Материал исследования
- •Проведение анализа
- •Практическое значение
- •Оформление работы
- •Оформление работы
- •Тестовые задания
- •Ситуационные задачи
- •Раздел 6. Строение и обмен пуриновых и пиримидиновых нуклеотидов Тема 6.1. Строение и метаболизм пуриновых и пиримидиновых нуклеотидов Актуальность
- •Вопросы для самоподготовки
- •Темы для реферативных сообщений
- •Нормальные величины
- •Клинико-диагностическое значение
- •Титрометрическое определение мочевой кислоты в моче
- •Ситуационные задачи
- •Темы для реферативных сообщений
- •Оформление работы
- •Темы для реферативных сообщений
- •Нормальные величины
- •Клинико-диагностическое значение
- •Оформление работы
- •Оформление работы
- •Тестовые задания
- •Ситуационные задачи
- •Контрольные вопросы к итоговому занятию
- •Раздел 8. Строение и обмен углеводов Тема 8.1. Строение и внешний обмен углеводов. Обмен гликогена Актуальность
- •Вопросы для самоподготовки
- •ТЕмы для реферативных сообщений
- •Нормальные значения
- •Клинико-диагностическое значение
- •Оформление работы
- •Оформление работы
- •Тема 8.2. Окисление глюкозы в анаэробных условиях. Глюконеогенез Актуальность
- •Вопросы для самоподготовки
- •Темы для реферативных сообщений
- •Нормальные величины
- •Клинико-диагностическое значение
- •Оформление работы
- •Нормальные величины
- •Клинико-диагностическое значение
- •Оформление работы
- •Практическое значение
- •Оформление работы
- •Тема 8.3. Аэробное окисление глюкозы. Пентозофосфатный путь Актуальность
- •Вопросы для самоподготовки
- •Темы для реферативных сообщений
- •Материал исследования
- •Реактивы
- •Определение концентрации глюкозы
- •Нормальные величины
- •Оценка гликемической кривой
- •Клинико-диагностическое значение
- •Оформление работы
- •Тестовые задания
- •Ситуационные задачи
- •Контрольные вопросы к итоговому занятию
- •Раздел 9. Строение и обмен липидов
- •Темы для реферативных сообщений
- •Лабораторная работа 1
- •Оформление работы
- •Темы для реферативных сообщений
- •Оформление работы
- •Лабораторная работа 2 Определение концентрации триацилглицеролов в сыворотке крови Принцип
- •Материал исследования
- •Оформление работы
- •Нормальные величины
- •Качественная проба Либена на ацетон Принцип
- •Проведение анализа
- •Нормальные величины
- •Клинико-диагностическое значение
- •Оформление работы
- •Тема 9.3. Внутриклеточный обмен фосфолипидов и холестерола. Транспорт липидов в крови Актуальность
- •Вопросы для самоподготовки
- •Темы для реферативных сообщений
- •Оформление работы
- •Тестовые задания
- •Ситуационные задачи
- •Контрольные вопросы к итоговому занятию
- •Раздел 10. Гормональная регуляция обмена веществ и функций организма Тема 10.1. Механизмы передачи гормонального сигнала. Классификация гормонов. Гормоны гипофиза. (семинар) Актуальность
- •Вопросы для самоподготовки
- •Темы для реферативных сообщений
- •Тема 10.2. Гормоны гипоталамуса, гипофиза, щитовидной поджелудочной и паращитовидной желез Актуальность
- •Вопросы для самоподготовки
- •Темы для реферативных сообщений
- •Лабораторная работа 1
- •Оформление работы
- •Тема 10.3. Гормоны гипофиза, надпочечников и половых желез Актуальность
- •Вопросы для самоподготовки
- •Темы для реферативных сообщений
- •Лабораторная работа 1
- •Ситуационные задачи
- •Раздел 11. Биохимия крови
- •Темы для реферативных сообщений
- •Клинико‑диагностическое значение
- •Оформление работы
- •Нормальные величины
- •Клинико-диагностическое значение
- •Оформление работы
- •Нормальные величины
- •Оформление работы
- •Лабораторная работа 4 (теоретически) Электрофорез белков на бумаге и ацетатцеллюлозных пленках Принцип
- •Материал исследования
- •Оборудование
- •Проведение анализа (основные положения)
- •Клинико-диагностическое значение
- •Тема 11.2. Обмен железа. Гемопротеины. Синтез и распад гема Актуальность
- •Вопросы для самоподготовки
- •Темы для реферативных сообщений
- •Нормальные величины
- •Клинико-диагностическое значение
- •Оформление работы
- •Тема 11.3. Неорганические вещества крови. Кислотно-основное состояние Актуальность
- •Вопросы для самоподготовки
- •Темы для реферативных сообщений
- •Нормальные величины
- •Клинико-диагностическое значение
- •Виды нарушений кислотно-основного состояния
- •Оформление работы
- •Нормальные величины
- •Практическое значение
- •Оформление работы
- •Оформление работы
- •Оформление работы
- •Тестовые задания
- •Ситуационные задачи
- •Раздел 12. Биохимия почек и печени Тема 12.1. Водно-солевой обмен. Нормальные и патологические компоненты мочи Актуальность
- •Вопросы для самоподготовки
- •Темы для реферативных сообщений
- •Нормальные величины
- •Лабораторная работа 2
- •Определение кетоновых тел тест-полосками "Кетофан"
- •Определение билирубина и уробилиногена тест-полосками "Иктофан" Принцип
- •Нормальные величины
- •Клинико-диагностическое значение
- •Определение гемоглобина и эритроцитов тест-полосками "Гемофан"
- •Принцип
- •Нормальные величины
- •Нормальные величины
- •Оформление работы
- •Лабораторная работа 3 (теоретически) Проба Реберга – определение клиренса креатинина Материал исследования
- •Принцип
- •Проведение анализа
- •Темы для реферативных сообщений
- •Клинико‑диагностическое значение
- •Тестовые задания
- •Ситуационные задачи
- •Контрольные вопросы к итоговому занятию
- •Приложение 1 Классификация и номенклатура ферментов
- •I класс. Оксидоредуктазы
- •II класс. Трансферазы
- •III класс. Гидролазы
- •IV класс. Лиазы
- •V класс. Изомеразы
- •VI класс. Лигазы
- •Приложение 2 Индивидуальные белки плазмы крови
- •Характеристика некоторых белков плазмы крови
- •Нормальные величины
- •Клинико‑диагностическое значение
- •Нормальные величины
- •Нормальные величины
- •Клинико-диагностическое значение
- •Нормальные величины
- •Клинико-диагностическое значение
- •Церулоплазмин
- •Нормальные величины
- •Клинико‑диагностическое значение
- •‑Глобулины
- •Желудочный сок
- •Клиренс эндогенного креатинина
- •Приложение 4
- •Строение, классификация и роль витаминов
- •Энзимология
- •Биологическое окисление
- •Обмен аминокислот и белков
- •Строение и обмен пуриновых и пиримидиновых нуклеотидов
- •Матричные биосинтезы
- •Строение и обмен углеводов
- •Строение и обмен липидов
- •Гормональная регуляция обмена веществ и функций организма
- •Биохимия крови
- •Биохимия почек и печени
Темы для реферативных сообщений
Усиление токсичных свойств соединений в результате биотрансформации. Химический канцерогенез.
Афлатоксины. Нитраты, нитриты и нитрозамины. Анилиновые красители. Их характеристика, токсичность и возможность обезвреживания в организме.
Метаболизм этанола. Механизмы токсического действия этанола. Современные представления о ферментативных путях метаболизма этанола: алкогольокисляющие ферментные системы.
Лабораторная работа 1
Исследование обезвреживающей системы печени
Исследование биотрансформации веществ с помощью амидопириновой пробы
Биотрансформация амидопирина (2,3-диметил-1-фенил-4-диметиламинопиразолон-5, пирамидон) осуществляется микросомальной и конъюгационной системами печени. Первый этап процесса, N‑деметилирование, осуществляется ферментами печени с образованием 4‑аминоантипирина. На втором этапе 4‑аминоантипирин подвергается ацетилированию с участием ацетил‑SКоА с образованием N‑ацетил-4-аминоантипирина.
|
|
Принцип
Исследование связано с определением концентрации 4‑аминоантипирина в моче. При взаимодействии с фенолом в щелочной среде и присутствии гексацианоферрата калия (III) (K3[Fe(CN)6], красная кровяная соль) 4‑аминоантипирин образует соединение типа индофенола, имеющего розовую окраску.
Материал исследования
Моча.
Реактивы
1) Аммиачный буфер, рН 10,5-10,6 (20 г хлорида аммония растворяют в 100 мл 25% раствора аммиака); 2) 0,02% раствор фенола перекристаллизованного; 3) 12,5% раствор трихлоруксусной кислоты (ТХУ); 4) 36% раствор соляной кислоты; 5) 1% раствор гексацианоферрата (III) калия K3[Fe(CN)]6.
Стандартный раствор 4‑аминоантипирина 1 г/л для построения калибровочного графика.
Проведение анализа
Обследуемый принимает утром натощак амидопирин из расчета 6 мг/кг веса (Aобщ). Собирается 4 порции мочи в интервале соответственно от 1 до 6 часов, 6-12, 12-24 и 45-48 часов. Объем мочи измеряется. Не позже чем через 24 часа, моча центрифугируется или фильтруется.
Далее исследуется концентрация 4‑аминоантипирина (опыт 1) и N‑ацетил-4-аминоантипирина (опыт 2):
|
|
Опыт 1, мл |
Опыт 2, мл |
|
Моча Аммиачный буфер Соляная кислота |
1,5 0,3 0,3 |
1,5 –– 0,3 |
|
|
Выдержать 15 минут при комнатной температуре |
Закрыть пробкой. Выдержать 15 минут при 100С |
|
|
Пробирки охлаждают и центрифугируют при 1500 об/мин | |
|
Аммиачный буфер |
–– |
0,6 |
|
Вновь центрифугируют при 1500 об/мин | ||
|
Надосадок Дистилл. вода ТХУ Раствор фенола Р-р K3[Fe(CN)6] |
0,6 –– 0,5 2,0 0,1 |
0,8 0,2 –– 2,0 0,1 |
|
|
Инкубируют 10 минут при 20-25°С. Не позднее чем через 60 минут измеряют оптическую плотность проб против воды при 510 нм (зеленый светофильтр) | |
Расчет
Концентрацию продуктов биотрансформации амидопирина в моче (мг/л) определяют по калибровочному графику, построенному с использованием калибровочных растворов антипирина в диапазоне от 3 до 20 мг/л.
Количество 4-аминоантипирина (A1, мг в порции мочи) находят, умножая его концентрацию (опыт 1) на соответствующий объем мочи (л).
Общее количество 4-аминоантипирина и N‑ацетил-4-аминоантипирина (A1+2, мг в порции мочи) находят, умножая их концентрацию (опыт 2) на соответствующий объем мочи (л).
Количество N-ацетил-4-аминоантипирина (A2), выделенного с мочой за сутки, находят по разности содержания в опыте 1 и опыте 2.
Монооксигеназную активность печени оценивают по формуле:
Активность монооксигеназ (%) =
 , где
, где
A1 – количество 4-аминоантипирина в порции мочи,Aобщ– количество введенного амидопирина.
Ацетилирующую активность ферментных систем печени находят по формуле:
Активность трансфераз (%) =
![]() , где
, где
A2 – количествоN-ацетил-4-аминоантипирина в порции мочи,A1– количество 4-аминоантипирина в порции мочи.
Общую обезвреживающую способность ферментных систем печени оценивают по формуле:
Общая активность (%) =