
- •О.И.Москвич общая физика Молекулярная физика
- •Предисловие
- •I. Основы молекулярной статистики
- •1.1. Предмет молекулярной физики
- •1.2. Масштабы физических величин в молекулярном мире
- •1.3. Теоретические и экспериментальные методы молекулярной физики
- •1.4. Эволюция молекулярных систем. Порядок и хаос
- •1.5. Принципы организации статистического и термодинамического методов изучения макросистем
- •Статистический метод
- •Термодинамический метод
- •2.1. Классификация моделей молекулярных систем
- •2.2. Идеальные статистические системы
- •Модели идеальных систем
- •2.3. Элементарные сведения из теории вероятностей
- •Случайные события
- •Определения вероятности событий
- •Статистическое или частотное определение вероятности.
- •Теоремы теории вероятностей
- •Условие нормировки вероятности
- •Случайная величина
- •Плотность вероятности
- •2.4. Основные понятия молекулярной статистики
- •Вероятность микроскопического состояния. Статистический ансамбль
- •Статистические постулаты
- •Комментарий к постулату равновероятности
- •Эргодическая гипотеза:
- •Постулат равновероятности доступных микроскопических состояний изолированной системы в состоянии термодинамического
- •Комментарий к эргодической гипотезе
- •Вероятность макроскопического состояния
- •3.1. Вывод закона распределения вероятностей Описание системы
- •Актуальные свойства модели системы
- •Постановка задачи
- •Вывод закона
- •Математические преобразования больших чисел. Введение общепринятых обозначений
- •Формула для вероятности макросостояния. Закон Бернулли, или биномиальное распределение.
- •3.2. Графическое представление биномиального распределения.
- •Основные характеристики биномиального распределении.
- •3.3. Предельные случаи биномиального распределения
- •4.1. Распределение энергии в статической системе
- •Вывод распределения Гиббса
- •4.2. Вывод распределения Максвелла
- •4.3. Плотность вероятности и характерные скорости распределения Максвелла
- •4.4. Распределение Максвелла по компонентам скорости
- •4.5. Экспериментальная проверка распределения Максвелла
- •5.1. Вывод формулы для давления идеального газа
- •5.2. Основное уравнение молекулярно-кинетической теории. Газовые законы
- •5.3. Уравнение эффузии
- •5.4. Измерение давления
- •5.5. Определение и измерение температуры
- •5.6. Построение эмпирической шкалы на основе газового термометра
- •Преимущества газовой шкалы температур
- •Построение газовой шкалы температур
- •Термодинамическая шкала температур
- •6.1. Распределение молекул по энергиям во внешнем потенциальном поле
- •6.2. Формула Больцмана для концентрации молекул в потенциальном поле
- •6.3. Зависимость концентрации молекул газа от координат в однородном гравитационном поле и поле центробежных сил
- •Графическое представление зависимости концентрации молекул от координат
- •6.4. Экспериментальное подтверждение распределения Больцмана: опыты Перрена
- •Получение макромолекул
- •Выделение частиц одинакового размера
- •Измерение диаметра макромолекулы
- •Подсчёт количества частиц на определённой высоте
- •6.5. Барометрическая формула
- •6.6. Закон распределения Максвелла – Больцмана
- •7.1. Формулировка теоремы и её доказательство Формулировка теоремы
- •Актуальные свойства модели статистической системы
- •Доказательство теоремы
- •7.2. Статистические степени свободы
- •7.3. Броуновское движение и его статистическое описание
- •Поступательное броуновское движение
- •Вращательное броуновское движение
- •7.4. Броуновский критерий точности физических измерений
- •7.5. Классическая теория теплоёмкости многоатомных газов. Область её применимости
- •7.6. Классическая теория теплоёмкости твёрдых тел.
- •7.7. Применение квантовых моделей в теории теплоёмкости твёрдых тел
- •Модель Эйнштейна
- •Модель Дебая
- •II. Основы термодинамики
- •8.1. Четыре постулата термодинамики
- •8.2. Нулевое (общее) начало термодинамики
- •Формулировка постулата
- •Свойство транзитивности термодинамического равновесия
- •Информационное содержание постулата
- •Фундаментальное и прикладное значение постулата
- •8.3. Макроскопические процессы
- •8.4. Функция состояния
- •Математические свойства функции состояния
- •8.5. Внутренняя энергия системы. Работа и теплота Внутренняя энергия
- •Макроскопическая работа и теплота
- •8.6. Калорическое и термическое уравнения состояния
- •9.1. Первое начало термодинамики
- •Формулировка постулата
- •Математическая запись постулата
- •Информационное содержание постулата
- •Фундаментальное и прикладное значение постулата
- •9.2. Теплоёмкость
- •Связь между теплоёмкостями и(общий случай)
- •Уравнение Роберта Майера
- •9.3. Политропические процессы в идеальном газе
- •Вывод уравнения политропического процесса в идеальном газе
- •9.4. Тепловые машины и их эффективность.
- •Принципиальная схема работы тепловой машины
- •Показатели эффективности тепловых машин
- •10.1. Цикл Карно
- •Расчёт кпд машины Карно
- •10.2. Теоремы Карно
- •Термодинамическая шкала температур
- •10.3. Метод циклов
- •Задача о нахождении зависимости внутренней энергии макроскопического тела от его объема
- •10.4. Неравенство Клаузиуса. Определение энтропии
- •10.5. Оценка эффективности тепловых машин сверху
- •Примеры оценок эффективности тепловых машин сверху кпд бензинового двигателя внутреннего сгорания
- •Кпд паровой турбины
- •Киэ бытового холодильника
- •Киэ кондиционера воздуха
- •Киэ теплового насоса
- •Тепловое загрязнение окружающей среды
- •11.1. Формулировки второго начала термодинамики
- •Энтропийная формулировка второго начала термодинамики Часть первая
- •Часть вторая
- •Информационное содержание постулата
- •11.2. Закон возрастания энтропии в изолированных системах
- •Демон Максвелла
- •Формулировка парадокса
- •Разрешение парадокса
- •11.3. Область применимости второго начала термодинамики
- •Статистический характер второго начала
- •11.4. Концепция тепловой смерти Вселенной
- •Концепция Клаузиуса
- •Флуктуационная гипотеза Больцмана
- •Несостоятельность концепции тепловой смерти Вселенной
- •11.5. Энтропия и её изменение в различных процессах
- •Постановка задачи
- •Описание системы
- •Актуальные свойства системы и процесса
- •Решение
- •Парадокс Гиббса Описание
- •По разные стороны перегородки находятся различные газы. После устранения перегородки начнется диффузия.
- •По разные стороны перегородки находится один и тот же газ.
- •12.1. Термодинамические функции
- •Свободная энергия
- •Термодинамический потенциал Гиббса
- •12.3. Условия термодинамической устойчивости макроскопических систем. Принцип Ле Шателье-Брауна
- •Принцип Ле Шателье-Брауна
- •Проведение полного термодинамического анализа вещества на полуэмпирической основе
- •12.4. Третье начало термодинамики
- •Формулировка постулата
- •Математическая запись постулата (варианты)
- •Информационное содержание постулата
- •Статус постулата
- •Следствия третьего начала
- •III. Физика реальных макросистем
- •13.1. Твердые тела
- •13.2. Реальные газы и жидкости
- •Потенциал межмолекулярного взаимодействия
- •Природа межмолекулярного взаимодействия
- •Структура жидкостей
- •13.3. Переход из газообразного состояния в жидкое.
- •13.4. Уравнения состояния реального газа
- •13.5. Модель газа Ван-дер-Ваальса. Уравнение Ван-дер-Ваальса
- •14.1. Изотермы газа Ван-дер-Ваальса
- •14.2. Критическое состояние вещества
- •Закон соответственных состояний
- •Свойства вещества в критическом состоянии
- •Анализ применения уравнения Ван-дер-Ваальса для описания свойств реальных газов
- •14.3. Внутренняя энергия газа Ван-дер-Ваальса
- •14.4. Эффект Джоуля-Томсона Основные определения
- •Описание процесса Джоуля-Томсона
- •Сущность эффекта Джоуля-Томсона
- •Расчет дифференциального эффекта Джоуля-Томсона
- •Расчет интегрального эффекта Джоуля-Томсона
- •14.5. Методы получения низких температур
- •Метод противоточного обмена теплотой
- •Метод адиабатического размагничивания
- •15.1. Условие равновесия фаз химически однородного вещества
- •15.2. Классификация фазовых переходов по Эренфесту
- •Фазовые переходы первого рода
- •Фазовые переходы второго рода
- •15.3. Фазовые переходы первого рода. Диаграмма состояний
- •15.4. Уравнение Клапейрона-Клаузиуса
- •Вывод уравнения Клапейрона-Клаузиуса
- •Вывод уравнения Клапейрона-Клаузиуса методом циклов
- •Актуальные свойства процесса
- •Постановка задачи
- •Вывод уравнения
- •15.5. Диаграмма состояний гелия. Сверхтекучесть жидкого гелия.
- •16.1. Релаксационные процессы в молекулярных системах
- •16.2. Стационарные уравнения переноса в газах, жидкостях и твердых телах
- •Уравнение теплопроводности
- •Уравнение самодиффузии
- •Уравнение внутреннего трения
- •16.3. Внутренняя теплопроводность и внешняя теплопередача
- •Стационарное распределение температуры в бесконечной плоско-параллельной пластинке
- •Стационарное распределение температуры между двумя концентрическими бесконечно длинными цилиндрами
- •Стационарное распределение температуры между двумя концентрическими сферами
- •Внешняя теплопередача
- •17.1. Столкновения молекул и их количественные характеристики
- •Эффективное сечение молекул
- •Средняя длина свободного пробега молекулы
- •Кинематические параметры и
- •17.2. Обобщенное уравнение переноса
- •Вывод обобщенного уравнения процесса Описание системы
- •Актуальные свойства модели процесса
- •Постановка задачи
- •Вывод уравнения
- •17.3. Элементарная кинетическая теория теплопроводности,
- •17.4. Явления переноса в ультраразреженных газах
- •Трение и теплопроводность ультраразреженных газов
- •Тепловая и изотермическая эффузия
- •18.1. Атмосфера как открытая система и как открытая книга
- •18.2. Состав и структура атмосферы Земли.
- •18.3. Термофизическая модель атмосферы
- •18.4. Парниковый эффект
- •Сущность парникового эффекта
- •Парниковые газы
- •Проблема глобального потепления
- •Киотский протокол
- •18.5. Инверсия температуры в стратосфере. Озоносфера Земли
- •Мониторинг озонового слоя
- •Монреальский Протокол
- •18.6. Концепция «ядерной зимы»
- •«Ядерная зима» Сценарии ядерной войны
- •Огненные смерчи – суперподъемники
- •Антипарниковый эффект
- •Глобальный характер климатических последствий
- •Список литературы
- •Общая физика. Молекулярная физика
- •660041, Г. Красноярск, пр. Свободный, 79
5.6. Построение эмпирической шкалы на основе газового термометра
Эмпирическая температура при фиксированной шкале и условленных реперных точках не одинакова при различном выборе термометрического тела и термометрической величины. Это означает, что различные термометры при измерении температуры одного и того же тела будут давать, как правило, разные показания.
Для разрешения данной проблемы за основной термометр был принят газовый, по которому было решено градуировать все остальные термометры. Причины выбора в качестве основного газового термометра указаны ниже.
Преимущества газовой шкалы температур
Идеальные газы (достаточно разрежённые реальные газы) с большой точностью подчиняются закону Бойля-Мариотта:
произведение объёма Vданной массы газа на его давлениеpзависит только от температуры:
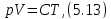
где C– постоянная, зависящая от массы и химической природы газа.
Если для идеального газа
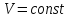 ,
то в этом случае вторым независимым
законом идеальных газов наряду с законом
Бойля-Мариотта следует считать закон
Шарля:
,
то в этом случае вторым независимым
законом идеальных газов наряду с законом
Бойля-Мариотта следует считать закон
Шарля:
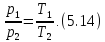
Опытным путём доказано, что температура T, определённая по формулам (5.13) и (5.14), очень слабо зависит от химической природы газа, которым наполнен резервуар газового термометра. Таким образом, показания различных газовых термометров при измерении температуры одного и того же тела очень мало отличаются друг от друга.
Построение газовой шкалы температур
Газовый термометр можно реализовать
двумя способами. В одном из них объём
газа
 поддерживается постоянным. Термометрической
величиной служит давление
поддерживается постоянным. Термометрической
величиной служит давление .
В другом случае поддерживается постоянное
давление газа, измерение температуры
сводится к измерению объёма. Принципиально
оба способа равноправны, но первый
способ наиболее удобен, поэтому и
применяется на практике.
.
В другом случае поддерживается постоянное
давление газа, измерение температуры
сводится к измерению объёма. Принципиально
оба способа равноправны, но первый
способ наиболее удобен, поэтому и
применяется на практике.
Газовый термометр представляет собой стеклянный, кварцевый или металлический баллон, заполненный азотом или гелием и соединенный с манометром с помощью капилляра. По показаниям манометра производится расчет измеряемой температуры.
Для построения идеально-газовой шкалы
температур в качестве реперных точек
рассматриваются нормальные точки
кипения и замерзания воды
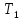 и
и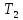 ,
соответственно. Градус температуры
выбирают таким, чтобы выполнялось
условие
,
соответственно. Градус температуры
выбирают таким, чтобы выполнялось
условие
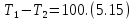
Для некоторой массы газа измеряют
давления
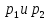 ,
соответствующие
,
соответствующие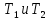 .
Полученное в эксперименте отношение
давлений равно 1,3661. Следовательно
.
Полученное в эксперименте отношение
давлений равно 1,3661. Следовательно
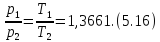
Совместное решение (5.15) и (5.16) дает:
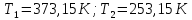 .
.
Таким образом, газовая шкала температур полностью определена.
Термодинамическая шкала температур
Температуры кипения и замерзания воды
зависят от давления, к тому же фиксируются
с недостаточной точностью, поэтому в
СИ условились определять шкалу температур
по одной реперной точке – тройной
точке воды. Это единственное состояние,
когда в равновесии находятся три фазы
(жидкая, газообразная и твёрдая), при
строго определённых значениях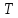 и
и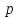 .
.
В термодинамической шкале температур
или шкале Кельвина температура реперной
точки, по определению, принята равной
273,16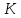 .
.
Единица температуры определяется как
1/273,16 температурного интервала между
тройной точкой и точкой абсолютного
нуля, которая на 273,16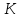 ниже температуры тройной точки воды.
ниже температуры тройной точки воды.
Если используется газовый термометр, то температуру можно определить по формуле
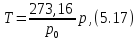
где
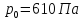 – давление в тройной точке воды. Поскольку
– давление в тройной точке воды. Поскольку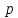 всегда положительная величина, то и
параметр
всегда положительная величина, то и
параметр не может принимать отрицательного
значения. Абсолютный нуль является
самой низкой из возможных температур.
Единицу измерения температуры в этой
шкале называют кельвином (сокращенно
не может принимать отрицательного
значения. Абсолютный нуль является
самой низкой из возможных температур.
Единицу измерения температуры в этой
шкале называют кельвином (сокращенно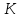 )
в честь английского физика лорда
Кельвина, предложившего термодинамическую
шкалу температур, тождественную с
идеальной газовой шкалой. Важно отметить,
что поскольку (5.17) основана на уравнении
состояния идеального газа, то температура
)
в честь английского физика лорда
Кельвина, предложившего термодинамическую
шкалу температур, тождественную с
идеальной газовой шкалой. Важно отметить,
что поскольку (5.17) основана на уравнении
состояния идеального газа, то температура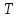 определенная этой формулой совпадает
с
определенная этой формулой совпадает
с ,
которая была введена как обозначение
в микроскопической теории.
,
которая была введена как обозначение
в микроскопической теории.
Наряду с абсолютной температурной
шкалой в физике и в повседневной жизни
применяются эмпирические шкалы, такие
как шкала Цельсия, шкала Фаренгейта и
шкала Реомюра. В этих шкалах величины
градусов различны, поскольку реперным
точкам приписываются разные температуры.
Однако, если взять одно и то же
термометрическое тело и одну и ту же
термометрическую величину, то можно
получить формулы пересчета температур
от одной шкалы к другой:

Контрольные вопросы
1. Дайте определение величине давления газа на стенку сосуда.
2. Почему при выводе формулы для давления газа можно использовать одномерное распределение Максвелла?
3. Чему равна нормальная составляющая передаваемого одной молекулой стенке сосуда при столкновении с ней?
4. Как подсчитать
число частиц, сталкивающихся со стенкой
сосуда единичной площади за одну секунду,
если составляющая скорости в направлении
к стенке принадлежат интервалу (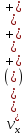 ?
?
5. Обоснуйте законы Паскаля и Дальтона.
6. Какое уравнение называют основным уравнением МКТ? Запишите его.
7. Запишите уравнение Клапейрона-Менделеева.
8. Сформулируйте закон Авогадро.
9. Что называется уравнением эффузии? Запишите его.
10. Какие приборы используются для измерения давления газа в разных диапазонах?
11. Какие величины являются термометрическими в таких термометрах как газовый, жидкостный, термопара?
12. Какая реперная точка используется при построении шкалы Кельвина? Чему равна её температура?
ЛЕКЦИЯ 6
РАСПРЕДЕЛЕНИЕ БОЛЬЦМАНА
