- •О.И.Москвич общая физика Молекулярная физика
- •Предисловие
- •I. Основы молекулярной статистики
- •1.1. Предмет молекулярной физики
- •1.2. Масштабы физических величин в молекулярном мире
- •1.3. Теоретические и экспериментальные методы молекулярной физики
- •1.4. Эволюция молекулярных систем. Порядок и хаос
- •1.5. Принципы организации статистического и термодинамического методов изучения макросистем
- •Статистический метод
- •Термодинамический метод
- •2.1. Классификация моделей молекулярных систем
- •2.2. Идеальные статистические системы
- •Модели идеальных систем
- •2.3. Элементарные сведения из теории вероятностей
- •Случайные события
- •Определения вероятности событий
- •Статистическое или частотное определение вероятности.
- •Теоремы теории вероятностей
- •Условие нормировки вероятности
- •Случайная величина
- •Плотность вероятности
- •2.4. Основные понятия молекулярной статистики
- •Вероятность микроскопического состояния. Статистический ансамбль
- •Статистические постулаты
- •Комментарий к постулату равновероятности
- •Эргодическая гипотеза:
- •Постулат равновероятности доступных микроскопических состояний изолированной системы в состоянии термодинамического
- •Комментарий к эргодической гипотезе
- •Вероятность макроскопического состояния
- •3.1. Вывод закона распределения вероятностей Описание системы
- •Актуальные свойства модели системы
- •Постановка задачи
- •Вывод закона
- •Математические преобразования больших чисел. Введение общепринятых обозначений
- •Формула для вероятности макросостояния. Закон Бернулли, или биномиальное распределение.
- •3.2. Графическое представление биномиального распределения.
- •Основные характеристики биномиального распределении.
- •3.3. Предельные случаи биномиального распределения
- •4.1. Распределение энергии в статической системе
- •Вывод распределения Гиббса
- •4.2. Вывод распределения Максвелла
- •4.3. Плотность вероятности и характерные скорости распределения Максвелла
- •4.4. Распределение Максвелла по компонентам скорости
- •4.5. Экспериментальная проверка распределения Максвелла
- •5.1. Вывод формулы для давления идеального газа
- •5.2. Основное уравнение молекулярно-кинетической теории. Газовые законы
- •5.3. Уравнение эффузии
- •5.4. Измерение давления
- •5.5. Определение и измерение температуры
- •5.6. Построение эмпирической шкалы на основе газового термометра
- •Преимущества газовой шкалы температур
- •Построение газовой шкалы температур
- •Термодинамическая шкала температур
- •6.1. Распределение молекул по энергиям во внешнем потенциальном поле
- •6.2. Формула Больцмана для концентрации молекул в потенциальном поле
- •6.3. Зависимость концентрации молекул газа от координат в однородном гравитационном поле и поле центробежных сил
- •Графическое представление зависимости концентрации молекул от координат
- •6.4. Экспериментальное подтверждение распределения Больцмана: опыты Перрена
- •Получение макромолекул
- •Выделение частиц одинакового размера
- •Измерение диаметра макромолекулы
- •Подсчёт количества частиц на определённой высоте
- •6.5. Барометрическая формула
- •6.6. Закон распределения Максвелла – Больцмана
- •7.1. Формулировка теоремы и её доказательство Формулировка теоремы
- •Актуальные свойства модели статистической системы
- •Доказательство теоремы
- •7.2. Статистические степени свободы
- •7.3. Броуновское движение и его статистическое описание
- •Поступательное броуновское движение
- •Вращательное броуновское движение
- •7.4. Броуновский критерий точности физических измерений
- •7.5. Классическая теория теплоёмкости многоатомных газов. Область её применимости
- •7.6. Классическая теория теплоёмкости твёрдых тел.
- •7.7. Применение квантовых моделей в теории теплоёмкости твёрдых тел
- •Модель Эйнштейна
- •Модель Дебая
- •II. Основы термодинамики
- •8.1. Четыре постулата термодинамики
- •8.2. Нулевое (общее) начало термодинамики
- •Формулировка постулата
- •Свойство транзитивности термодинамического равновесия
- •Информационное содержание постулата
- •Фундаментальное и прикладное значение постулата
- •8.3. Макроскопические процессы
- •8.4. Функция состояния
- •Математические свойства функции состояния
- •8.5. Внутренняя энергия системы. Работа и теплота Внутренняя энергия
- •Макроскопическая работа и теплота
- •8.6. Калорическое и термическое уравнения состояния
- •9.1. Первое начало термодинамики
- •Формулировка постулата
- •Математическая запись постулата
- •Информационное содержание постулата
- •Фундаментальное и прикладное значение постулата
- •9.2. Теплоёмкость
- •Связь между теплоёмкостями и(общий случай)
- •Уравнение Роберта Майера
- •9.3. Политропические процессы в идеальном газе
- •Вывод уравнения политропического процесса в идеальном газе
- •9.4. Тепловые машины и их эффективность.
- •Принципиальная схема работы тепловой машины
- •Показатели эффективности тепловых машин
- •10.1. Цикл Карно
- •Расчёт кпд машины Карно
- •10.2. Теоремы Карно
- •Термодинамическая шкала температур
- •10.3. Метод циклов
- •Задача о нахождении зависимости внутренней энергии макроскопического тела от его объема
- •10.4. Неравенство Клаузиуса. Определение энтропии
- •10.5. Оценка эффективности тепловых машин сверху
- •Примеры оценок эффективности тепловых машин сверху кпд бензинового двигателя внутреннего сгорания
- •Кпд паровой турбины
- •Киэ бытового холодильника
- •Киэ кондиционера воздуха
- •Киэ теплового насоса
- •Тепловое загрязнение окружающей среды
- •11.1. Формулировки второго начала термодинамики
- •Энтропийная формулировка второго начала термодинамики Часть первая
- •Часть вторая
- •Информационное содержание постулата
- •11.2. Закон возрастания энтропии в изолированных системах
- •Демон Максвелла
- •Формулировка парадокса
- •Разрешение парадокса
- •11.3. Область применимости второго начала термодинамики
- •Статистический характер второго начала
- •11.4. Концепция тепловой смерти Вселенной
- •Концепция Клаузиуса
- •Флуктуационная гипотеза Больцмана
- •Несостоятельность концепции тепловой смерти Вселенной
- •11.5. Энтропия и её изменение в различных процессах
- •Постановка задачи
- •Описание системы
- •Актуальные свойства системы и процесса
- •Решение
- •Парадокс Гиббса Описание
- •По разные стороны перегородки находятся различные газы. После устранения перегородки начнется диффузия.
- •По разные стороны перегородки находится один и тот же газ.
- •12.1. Термодинамические функции
- •Свободная энергия
- •Термодинамический потенциал Гиббса
- •12.3. Условия термодинамической устойчивости макроскопических систем. Принцип Ле Шателье-Брауна
- •Принцип Ле Шателье-Брауна
- •Проведение полного термодинамического анализа вещества на полуэмпирической основе
- •12.4. Третье начало термодинамики
- •Формулировка постулата
- •Математическая запись постулата (варианты)
- •Информационное содержание постулата
- •Статус постулата
- •Следствия третьего начала
- •III. Физика реальных макросистем
- •13.1. Твердые тела
- •13.2. Реальные газы и жидкости
- •Потенциал межмолекулярного взаимодействия
- •Природа межмолекулярного взаимодействия
- •Структура жидкостей
- •13.3. Переход из газообразного состояния в жидкое.
- •13.4. Уравнения состояния реального газа
- •13.5. Модель газа Ван-дер-Ваальса. Уравнение Ван-дер-Ваальса
- •14.1. Изотермы газа Ван-дер-Ваальса
- •14.2. Критическое состояние вещества
- •Закон соответственных состояний
- •Свойства вещества в критическом состоянии
- •Анализ применения уравнения Ван-дер-Ваальса для описания свойств реальных газов
- •14.3. Внутренняя энергия газа Ван-дер-Ваальса
- •14.4. Эффект Джоуля-Томсона Основные определения
- •Описание процесса Джоуля-Томсона
- •Сущность эффекта Джоуля-Томсона
- •Расчет дифференциального эффекта Джоуля-Томсона
- •Расчет интегрального эффекта Джоуля-Томсона
- •14.5. Методы получения низких температур
- •Метод противоточного обмена теплотой
- •Метод адиабатического размагничивания
- •15.1. Условие равновесия фаз химически однородного вещества
- •15.2. Классификация фазовых переходов по Эренфесту
- •Фазовые переходы первого рода
- •Фазовые переходы второго рода
- •15.3. Фазовые переходы первого рода. Диаграмма состояний
- •15.4. Уравнение Клапейрона-Клаузиуса
- •Вывод уравнения Клапейрона-Клаузиуса
- •Вывод уравнения Клапейрона-Клаузиуса методом циклов
- •Актуальные свойства процесса
- •Постановка задачи
- •Вывод уравнения
- •15.5. Диаграмма состояний гелия. Сверхтекучесть жидкого гелия.
- •16.1. Релаксационные процессы в молекулярных системах
- •16.2. Стационарные уравнения переноса в газах, жидкостях и твердых телах
- •Уравнение теплопроводности
- •Уравнение самодиффузии
- •Уравнение внутреннего трения
- •16.3. Внутренняя теплопроводность и внешняя теплопередача
- •Стационарное распределение температуры в бесконечной плоско-параллельной пластинке
- •Стационарное распределение температуры между двумя концентрическими бесконечно длинными цилиндрами
- •Стационарное распределение температуры между двумя концентрическими сферами
- •Внешняя теплопередача
- •17.1. Столкновения молекул и их количественные характеристики
- •Эффективное сечение молекул
- •Средняя длина свободного пробега молекулы
- •Кинематические параметры и
- •17.2. Обобщенное уравнение переноса
- •Вывод обобщенного уравнения процесса Описание системы
- •Актуальные свойства модели процесса
- •Постановка задачи
- •Вывод уравнения
- •17.3. Элементарная кинетическая теория теплопроводности,
- •17.4. Явления переноса в ультраразреженных газах
- •Трение и теплопроводность ультраразреженных газов
- •Тепловая и изотермическая эффузия
- •18.1. Атмосфера как открытая система и как открытая книга
- •18.2. Состав и структура атмосферы Земли.
- •18.3. Термофизическая модель атмосферы
- •18.4. Парниковый эффект
- •Сущность парникового эффекта
- •Парниковые газы
- •Проблема глобального потепления
- •Киотский протокол
- •18.5. Инверсия температуры в стратосфере. Озоносфера Земли
- •Мониторинг озонового слоя
- •Монреальский Протокол
- •18.6. Концепция «ядерной зимы»
- •«Ядерная зима» Сценарии ядерной войны
- •Огненные смерчи – суперподъемники
- •Антипарниковый эффект
- •Глобальный характер климатических последствий
- •Список литературы
- •Общая физика. Молекулярная физика
- •660041, Г. Красноярск, пр. Свободный, 79
III. Физика реальных макросистем
ЛЕКЦИЯ 13
РЕАЛЬНЫЕ МАКРОСИСТЕМЫ
Изучение реальных макросистем, т.е. систем с межмолекулярным взаимодействием, начнем с рассмотрения свойств вещества в состоянии термодинамического равновесия, а затем перейдем к анализу процессов в неравновесных системах.
Как вам известно, вещества могут существовать в четырех агрегатных состояниях. Исключим пока из рассмотрения такое состояние вещества как плазма. Забудем про неё до изучения ядерной физики. В ближайшей перспективе сконцентрируем своё внимание на свойствах таких систем как реальный газ, жидкость и твердое тело, а также на их взаимных превращениях. Последние принято называть фазовыми превращениями или фазовыми переходами. Теперь самое время сформулировать определение фазы.
Фазой называется макроскопическая физически однородная часть вещества, отделенная от остальных частей системы границами раздела. Например, вода, лед и пар; вода, ртуть и смесь паров воды, ртути и воздуха; графит и алмаз. Из приведенных примеров и вашего повседневного опыта ясно, что в системе может быть несколько твердых или жидких фаз, но не более одной газообразной, поскольку газы необратимо смешиваются между собой. Прежде чем углубиться в тему фазовых переходов обратимся к моделям материальных тел, разберемся с внутренней структурой вещества в различных агрегатных состояниях. Определяющим фактором в реальных системах являются силы межмолекулярного взаимодействия.
На больших расстояниях молекулы притягиваются друг к другу, а на малых расстояниях порядка размеров самых молекул частицы отталкиваются друг от друга. По своей природе силы межмолекулярного взаимодействия являются электрическими. В зависимости от распределения электронной плотности внутри отдельных молекул и концентрации самих молекул в пространстве существуют различные типы межмолекулярного взаимодействия. Для каждого агрегатного состояния характерны свои типы взаимодействия.
Количественным критерием существования
того или иного агрегатного состояния
вещества может служить соотношение
средней кинетической энергии молекулы
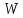 и энергии межмолекулярного притяжения
и энергии межмолекулярного притяжения .
Заметим, что энергия притяжения - величина
отрицательная (знак « - »), а кинетическая
энергия – положительная (знак «+»),
поэтому сравнивать будем не значения,
а модули этих энергий. Итак, если
.
Заметим, что энергия притяжения - величина
отрицательная (знак « - »), а кинетическая
энергия – положительная (знак «+»),
поэтому сравнивать будем не значения,
а модули этих энергий. Итак, если
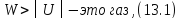
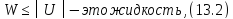
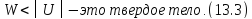
Дадим более детальное описание каждого из этих состояний и начнем с твердого тела.
13.1. Твердые тела
В физике твердыми телами обычно называются только кристаллические тела. Аморфные тела типа воска, стекла, пластика, хотя они и могут быть твердыми (сохранять свою форму), рассматриваются как очень вязкие жидкости. Аморфные тела не имеют определенной температуры плавления. При нагревании они постепенно размягчаются, их вязкость при этом уменьшается, и они превращаются в жидкость. Аморфные тела изотропны, т.е. их свойства одинаковы по всем направлениям.
Кристаллические тела имеют определенную температуру плавления при фиксированном давлении. Свойства кристаллов неодинаковы по различным направлениям. Кристаллы анизотропны. Скорость распространения света, коэффициенты теплопроводности и упругости и многие другие свойства кристалла зависят от направления в нем. Это связано с особенностями внутреннего строения твердого тела.
Условие (13.3) свидетельствует о том, что в кристалле силы межатомного притяжения доминируют, существенно подавляя хаотическое движение атомов. Поступательное движение сведено на нет и возможны только небольшие тепловые колебания атомов около положения равновесия. Устойчивое равновесие достигается при вполне определенном расположении молекул относительно друг друга. Поскольку такое распределение составляющих кристалл элементов должно происходить по всему объему тела, то неизбежно периодическое повторение формы, т.е. возникновение кристаллической решетки с определенной симметрией. Точки равновесного положения атомов, ионов и молекул в кристалле называют узлами кристаллической решетки. Под симметрией понимается способность твердого тела совмещаться с самим собой в результате реальных или воображаемых действий над его точками.
Операциями симметрии называются
действия, с помощью которых производится
совмещение тела. Такими операциями
являются отражение, повороты, инверсии
и трансляции (параллельные переносы).
В частности, если решетка совмещается
сама с собой при мысленном повороте
вокруг некоторой оси на угол 360º, где
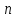 – число совмещений за полный оборот,
то эту ось называют осью симметрииn-го
порядка. В твердых телах имеют место
только оси симметрии с порядками 2, 3, 4
и 6 с соответствующими углами поворота
180, 120, 90 и 60º. Симметрия 5-го порядка в
кристаллах невозможна.
– число совмещений за полный оборот,
то эту ось называют осью симметрииn-го
порядка. В твердых телах имеют место
только оси симметрии с порядками 2, 3, 4
и 6 с соответствующими углами поворота
180, 120, 90 и 60º. Симметрия 5-го порядка в
кристаллах невозможна.
В основе теории твердого тела лежит модель бесконечного совершенного монокристалла. Если выбрать начало координат в некотором узле кристаллической решетки, то радиус-вектор любого другого узла можно представить в виде
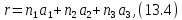
где
 – целые числа, включая ноль. Векторы
– целые числа, включая ноль. Векторы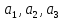 называются базисными, а их совокупность
базисом решетки. Сам вектор
называются базисными, а их совокупность
базисом решетки. Сам вектор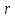 называется вектором трансляции. Длины
векторов
называется вектором трансляции. Длины
векторов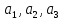 называются основными периодами
(параметрами) решетки. Параллелепипед
с ребрами
называются основными периодами
(параметрами) решетки. Параллелепипед
с ребрами
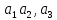 вместе с атомами в его вершинах, а
возможно и внутри объёма параллелепипеда,
называетсяэлементарной ячейкойтрансляцией этой ячейки создаётся
бесконечнаяпространственная
решетка. Если ячейка содержит восемь
атомов в вершинах параллелепипеда и не
одного атома внутри своего объёма, то
ячейка называетсяпримитивной.Сложные ячейкиимеют узлы внутри
своего объёма или на гранях параллелепипеда.
вместе с атомами в его вершинах, а
возможно и внутри объёма параллелепипеда,
называетсяэлементарной ячейкойтрансляцией этой ячейки создаётся
бесконечнаяпространственная
решетка. Если ячейка содержит восемь
атомов в вершинах параллелепипеда и не
одного атома внутри своего объёма, то
ячейка называетсяпримитивной.Сложные ячейкиимеют узлы внутри
своего объёма или на гранях параллелепипеда.
Конкретная кристаллическая решетка может быть представлена не одной решеткой Браве, а совокупностью нескольких решеток Браве. В таких случаях она называется сложной решеткой.
Выбор базиса даже примитивной решетки не является однозначным. На рис. 13.1 приведены примеры примитивных (а, б) и сложных (в, г) ячеек для одного и того же кристалла (двухмерная решётка).
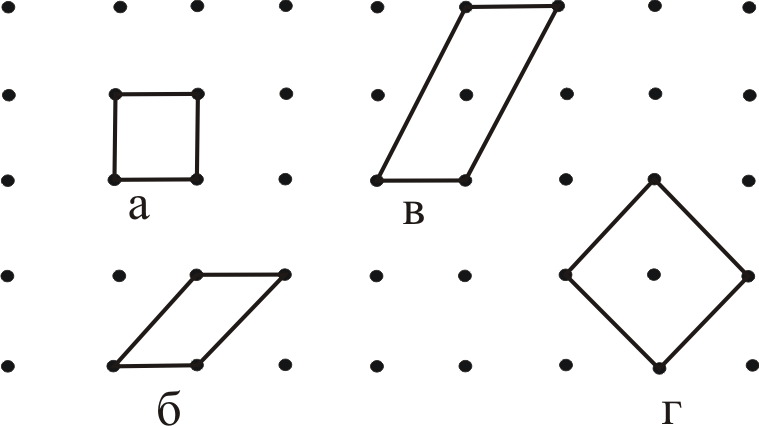
Рис. 13.1.
Наименьшая из примитивных ячеек, включающая в себя все элементы симметрии решетки, называется ячейкой или параллелепипедом Браве.Существует всего семь типов решеток или семь типов кристаллических систем. Характеристики кристаллических систем и их названия приведены в табл. 13.1.
Таблица. 13.1.
|
Кристаллическая система |
Соотношение рёбер элементарной ячейки |
Соотношение между углами в элементарной ячейке |
|
Триклинная |
|
|
|
Моноклинная |
|
|
|
Ромбическая |
|
|
|
Тетрагональная |
|
|
|
Кубическая |
|
|
|
Ромбоэдрическая |
|
|
|
Гексагональная |
|
|
Ограничимся вышеизложенными представлениями о симметрии кристаллов, хотя они, безусловно, не исчерпывают затронутую тему. Последовательно и подробно эти вопросы изучаются в курсе кристаллографии.
Теперь уместно обратиться к рассмотрению
межатомных взаимодействий в твердых
телах. Минимизация энергии взаимодействия
приводит к той или иной симметрии
кристалла и определенному типу
пространственной решетки. Положительная
разность между энергией изолированных
атомов и энергией атомов в кристаллической
решетке называется энергией связи
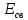 .
Ее значение колеблется в интервале 0,1÷
7,0 эВ на частицу в зависимости от характера
взаимодействия. Мерой
.
Ее значение колеблется в интервале 0,1÷
7,0 эВ на частицу в зависимости от характера
взаимодействия. Мерой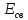 является работа, которую необходимо
совершить для удаления частицы из
кристалла.
является работа, которую необходимо
совершить для удаления частицы из
кристалла.
При химическом взаимодействии, приводящем к образованию кристалла, различают несколько основных типов связи, представленных на схеме 13.1.1. Более подробное изложение вопроса о типах связи можно найти в [11,14].
Кроме основных типов связей между
частицами в твердом теле возможны
смешанные связи. Различные сочетания
взаимодействий приводят к многообразию
строения кристаллов. Такое явление как
анизотропия кристаллов становится
очевидным благодаря рассмотренной
модели материального тела. Действительно,
ведь в различных плоскостях, которые
можно провести в кристалле, расстояния
между частицами оказываются различными.
Так как силы, действующие между частицами,
зависят от расстояния, то физические
свойства кристаллов (оптические,
электрические, механические) зависят
от направления, а в этом и заключается
их анизотропия. Следует также отметить,
что между
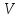 ,
температурой плавления кристаллов (при
постоянном давлении) и энергией связи
наблюдается прямая корреляция.
,
температурой плавления кристаллов (при
постоянном давлении) и энергией связи
наблюдается прямая корреляция.
Схема 13.1.1.


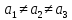
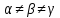
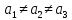


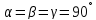

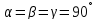


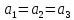
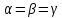 но
но