
- •О.И.Москвич общая физика Молекулярная физика
- •Предисловие
- •I. Основы молекулярной статистики
- •1.1. Предмет молекулярной физики
- •1.2. Масштабы физических величин в молекулярном мире
- •1.3. Теоретические и экспериментальные методы молекулярной физики
- •1.4. Эволюция молекулярных систем. Порядок и хаос
- •1.5. Принципы организации статистического и термодинамического методов изучения макросистем
- •Статистический метод
- •Термодинамический метод
- •2.1. Классификация моделей молекулярных систем
- •2.2. Идеальные статистические системы
- •Модели идеальных систем
- •2.3. Элементарные сведения из теории вероятностей
- •Случайные события
- •Определения вероятности событий
- •Статистическое или частотное определение вероятности.
- •Теоремы теории вероятностей
- •Условие нормировки вероятности
- •Случайная величина
- •Плотность вероятности
- •2.4. Основные понятия молекулярной статистики
- •Вероятность микроскопического состояния. Статистический ансамбль
- •Статистические постулаты
- •Комментарий к постулату равновероятности
- •Эргодическая гипотеза:
- •Постулат равновероятности доступных микроскопических состояний изолированной системы в состоянии термодинамического
- •Комментарий к эргодической гипотезе
- •Вероятность макроскопического состояния
- •3.1. Вывод закона распределения вероятностей Описание системы
- •Актуальные свойства модели системы
- •Постановка задачи
- •Вывод закона
- •Математические преобразования больших чисел. Введение общепринятых обозначений
- •Формула для вероятности макросостояния. Закон Бернулли, или биномиальное распределение.
- •3.2. Графическое представление биномиального распределения.
- •Основные характеристики биномиального распределении.
- •3.3. Предельные случаи биномиального распределения
- •4.1. Распределение энергии в статической системе
- •Вывод распределения Гиббса
- •4.2. Вывод распределения Максвелла
- •4.3. Плотность вероятности и характерные скорости распределения Максвелла
- •4.4. Распределение Максвелла по компонентам скорости
- •4.5. Экспериментальная проверка распределения Максвелла
- •5.1. Вывод формулы для давления идеального газа
- •5.2. Основное уравнение молекулярно-кинетической теории. Газовые законы
- •5.3. Уравнение эффузии
- •5.4. Измерение давления
- •5.5. Определение и измерение температуры
- •5.6. Построение эмпирической шкалы на основе газового термометра
- •Преимущества газовой шкалы температур
- •Построение газовой шкалы температур
- •Термодинамическая шкала температур
- •6.1. Распределение молекул по энергиям во внешнем потенциальном поле
- •6.2. Формула Больцмана для концентрации молекул в потенциальном поле
- •6.3. Зависимость концентрации молекул газа от координат в однородном гравитационном поле и поле центробежных сил
- •Графическое представление зависимости концентрации молекул от координат
- •6.4. Экспериментальное подтверждение распределения Больцмана: опыты Перрена
- •Получение макромолекул
- •Выделение частиц одинакового размера
- •Измерение диаметра макромолекулы
- •Подсчёт количества частиц на определённой высоте
- •6.5. Барометрическая формула
- •6.6. Закон распределения Максвелла – Больцмана
- •7.1. Формулировка теоремы и её доказательство Формулировка теоремы
- •Актуальные свойства модели статистической системы
- •Доказательство теоремы
- •7.2. Статистические степени свободы
- •7.3. Броуновское движение и его статистическое описание
- •Поступательное броуновское движение
- •Вращательное броуновское движение
- •7.4. Броуновский критерий точности физических измерений
- •7.5. Классическая теория теплоёмкости многоатомных газов. Область её применимости
- •7.6. Классическая теория теплоёмкости твёрдых тел.
- •7.7. Применение квантовых моделей в теории теплоёмкости твёрдых тел
- •Модель Эйнштейна
- •Модель Дебая
- •II. Основы термодинамики
- •8.1. Четыре постулата термодинамики
- •8.2. Нулевое (общее) начало термодинамики
- •Формулировка постулата
- •Свойство транзитивности термодинамического равновесия
- •Информационное содержание постулата
- •Фундаментальное и прикладное значение постулата
- •8.3. Макроскопические процессы
- •8.4. Функция состояния
- •Математические свойства функции состояния
- •8.5. Внутренняя энергия системы. Работа и теплота Внутренняя энергия
- •Макроскопическая работа и теплота
- •8.6. Калорическое и термическое уравнения состояния
- •9.1. Первое начало термодинамики
- •Формулировка постулата
- •Математическая запись постулата
- •Информационное содержание постулата
- •Фундаментальное и прикладное значение постулата
- •9.2. Теплоёмкость
- •Связь между теплоёмкостями и(общий случай)
- •Уравнение Роберта Майера
- •9.3. Политропические процессы в идеальном газе
- •Вывод уравнения политропического процесса в идеальном газе
- •9.4. Тепловые машины и их эффективность.
- •Принципиальная схема работы тепловой машины
- •Показатели эффективности тепловых машин
- •10.1. Цикл Карно
- •Расчёт кпд машины Карно
- •10.2. Теоремы Карно
- •Термодинамическая шкала температур
- •10.3. Метод циклов
- •Задача о нахождении зависимости внутренней энергии макроскопического тела от его объема
- •10.4. Неравенство Клаузиуса. Определение энтропии
- •10.5. Оценка эффективности тепловых машин сверху
- •Примеры оценок эффективности тепловых машин сверху кпд бензинового двигателя внутреннего сгорания
- •Кпд паровой турбины
- •Киэ бытового холодильника
- •Киэ кондиционера воздуха
- •Киэ теплового насоса
- •Тепловое загрязнение окружающей среды
- •11.1. Формулировки второго начала термодинамики
- •Энтропийная формулировка второго начала термодинамики Часть первая
- •Часть вторая
- •Информационное содержание постулата
- •11.2. Закон возрастания энтропии в изолированных системах
- •Демон Максвелла
- •Формулировка парадокса
- •Разрешение парадокса
- •11.3. Область применимости второго начала термодинамики
- •Статистический характер второго начала
- •11.4. Концепция тепловой смерти Вселенной
- •Концепция Клаузиуса
- •Флуктуационная гипотеза Больцмана
- •Несостоятельность концепции тепловой смерти Вселенной
- •11.5. Энтропия и её изменение в различных процессах
- •Постановка задачи
- •Описание системы
- •Актуальные свойства системы и процесса
- •Решение
- •Парадокс Гиббса Описание
- •По разные стороны перегородки находятся различные газы. После устранения перегородки начнется диффузия.
- •По разные стороны перегородки находится один и тот же газ.
- •12.1. Термодинамические функции
- •Свободная энергия
- •Термодинамический потенциал Гиббса
- •12.3. Условия термодинамической устойчивости макроскопических систем. Принцип Ле Шателье-Брауна
- •Принцип Ле Шателье-Брауна
- •Проведение полного термодинамического анализа вещества на полуэмпирической основе
- •12.4. Третье начало термодинамики
- •Формулировка постулата
- •Математическая запись постулата (варианты)
- •Информационное содержание постулата
- •Статус постулата
- •Следствия третьего начала
- •III. Физика реальных макросистем
- •13.1. Твердые тела
- •13.2. Реальные газы и жидкости
- •Потенциал межмолекулярного взаимодействия
- •Природа межмолекулярного взаимодействия
- •Структура жидкостей
- •13.3. Переход из газообразного состояния в жидкое.
- •13.4. Уравнения состояния реального газа
- •13.5. Модель газа Ван-дер-Ваальса. Уравнение Ван-дер-Ваальса
- •14.1. Изотермы газа Ван-дер-Ваальса
- •14.2. Критическое состояние вещества
- •Закон соответственных состояний
- •Свойства вещества в критическом состоянии
- •Анализ применения уравнения Ван-дер-Ваальса для описания свойств реальных газов
- •14.3. Внутренняя энергия газа Ван-дер-Ваальса
- •14.4. Эффект Джоуля-Томсона Основные определения
- •Описание процесса Джоуля-Томсона
- •Сущность эффекта Джоуля-Томсона
- •Расчет дифференциального эффекта Джоуля-Томсона
- •Расчет интегрального эффекта Джоуля-Томсона
- •14.5. Методы получения низких температур
- •Метод противоточного обмена теплотой
- •Метод адиабатического размагничивания
- •15.1. Условие равновесия фаз химически однородного вещества
- •15.2. Классификация фазовых переходов по Эренфесту
- •Фазовые переходы первого рода
- •Фазовые переходы второго рода
- •15.3. Фазовые переходы первого рода. Диаграмма состояний
- •15.4. Уравнение Клапейрона-Клаузиуса
- •Вывод уравнения Клапейрона-Клаузиуса
- •Вывод уравнения Клапейрона-Клаузиуса методом циклов
- •Актуальные свойства процесса
- •Постановка задачи
- •Вывод уравнения
- •15.5. Диаграмма состояний гелия. Сверхтекучесть жидкого гелия.
- •16.1. Релаксационные процессы в молекулярных системах
- •16.2. Стационарные уравнения переноса в газах, жидкостях и твердых телах
- •Уравнение теплопроводности
- •Уравнение самодиффузии
- •Уравнение внутреннего трения
- •16.3. Внутренняя теплопроводность и внешняя теплопередача
- •Стационарное распределение температуры в бесконечной плоско-параллельной пластинке
- •Стационарное распределение температуры между двумя концентрическими бесконечно длинными цилиндрами
- •Стационарное распределение температуры между двумя концентрическими сферами
- •Внешняя теплопередача
- •17.1. Столкновения молекул и их количественные характеристики
- •Эффективное сечение молекул
- •Средняя длина свободного пробега молекулы
- •Кинематические параметры и
- •17.2. Обобщенное уравнение переноса
- •Вывод обобщенного уравнения процесса Описание системы
- •Актуальные свойства модели процесса
- •Постановка задачи
- •Вывод уравнения
- •17.3. Элементарная кинетическая теория теплопроводности,
- •17.4. Явления переноса в ультраразреженных газах
- •Трение и теплопроводность ультраразреженных газов
- •Тепловая и изотермическая эффузия
- •18.1. Атмосфера как открытая система и как открытая книга
- •18.2. Состав и структура атмосферы Земли.
- •18.3. Термофизическая модель атмосферы
- •18.4. Парниковый эффект
- •Сущность парникового эффекта
- •Парниковые газы
- •Проблема глобального потепления
- •Киотский протокол
- •18.5. Инверсия температуры в стратосфере. Озоносфера Земли
- •Мониторинг озонового слоя
- •Монреальский Протокол
- •18.6. Концепция «ядерной зимы»
- •«Ядерная зима» Сценарии ядерной войны
- •Огненные смерчи – суперподъемники
- •Антипарниковый эффект
- •Глобальный характер климатических последствий
- •Список литературы
- •Общая физика. Молекулярная физика
- •660041, Г. Красноярск, пр. Свободный, 79
17.4. Явления переноса в ультраразреженных газах
Состояние разреженного газа называют
вакуумом.Степень разрежения
характеризуют тремя параметрами: Понятие вакуума относительно, чем больше
размеры области, тем при меньшем давлении
он достигается. В теоретических
рассмотрениях обычно используется
сравнение величины
Понятие вакуума относительно, чем больше
размеры области, тем при меньшем давлении
он достигается. В теоретических
рассмотрениях обычно используется
сравнение величины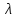 с линейным размером сосуда
с линейным размером сосуда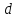 ,
ограничивающего объем газа. Принято
различать четыре степени вакуума.
Признаки градации и соответствующие
названия вакуума приведены в табл. 17.1.
,
ограничивающего объем газа. Принято
различать четыре степени вакуума.
Признаки градации и соответствующие
названия вакуума приведены в табл. 17.1.
Таблица. 17.1.

Для описания явлений переноса наиболее «прозрачным» является случай ультраразреженного газа. Поскольку в этих условиях столкновения между молекулами практически отсутствуют, то и «эстафетный» механизм передачи молекулярных свойств не работает. Молекулы по прямым линиям летят от одной стенки сосуда к другой и обмениваются с ними, например, энергией (это уже не теплопроводность, а теплопередача) или импульсом упорядоченного движения (трение при малых давлениях). Механизмы переноса можно легко смоделировать, используя уравнение эффузии.
Одной из особенностей высокого вакуума
является невозможность возникновения
в нем конвекционных потоков. Наиболее
трудным для теории является случай
среднего вакуума, когда
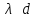 .
.
Трение и теплопроводность ультраразреженных газов
Независимость коэффициентов внутреннего
трения и теплопроводности от давления
газа, обоснованная нами в 17.3. имеет место
при таких давлениях, когда
 .
В сильно разреженных газах, как отмечалось
выше, механизм трения совершенно иной,
нежели в плотных газах. Изменение
импульсов молекул происходит только
при ударах о стенку сосуда, поэтому
трение становится не внутренним, а
внешним. Внешнее трение зависит от числа
ударов о стенку, которое пропорционально
концентрации частиц, а следовательно,
и давлению газа.
.
В сильно разреженных газах, как отмечалось
выше, механизм трения совершенно иной,
нежели в плотных газах. Изменение
импульсов молекул происходит только
при ударах о стенку сосуда, поэтому
трение становится не внутренним, а
внешним. Внешнее трение зависит от числа
ударов о стенку, которое пропорционально
концентрации частиц, а следовательно,
и давлению газа.
Аналогичное заключение можно сделать и по поводу теплопередачи. Молекула как пчела, несущая нектар, летит от горячей стенки к холодной и передает ей свою кинетическую энергию. После чего она «холодная и голодная» возвращается к горячей стенке за новой порцией энергии. Механизм выравнивания температуры именно таков. Количество перенесенной молекулами энергии пропорционально числу ударов о стенки, т.е. концентрации или давлению газа. Коэффициент теплопередачи растет пропорционально давлению.
Тепловая и изотермическая эффузия
Интересные явления наблюдаются в сосудах
с газом, сообщающихся через очень тонкую
пористую перегородку. Размеры пор могут
быть столь малыми (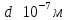 ),
что в них соблюдаются условия вакуума
уже при нормальном атмосферном давлении.
Если по разные стороны перегородки
имеется один и тот же газ и поддерживаются
различные температуры, то наблюдается
явлениетепловой эффузии.А если
по разные стороны перегородки находятся
разные газы при одних и тех же начальных
давлениях и температурах – наблюдается
явлениеизотермической эффузии.
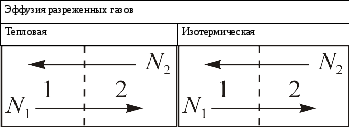
На схеме 17.4.1 наглядно представлены
необходимые начальные условия для
тепловой и изотермической эффузии.
),
что в них соблюдаются условия вакуума
уже при нормальном атмосферном давлении.
Если по разные стороны перегородки
имеется один и тот же газ и поддерживаются
различные температуры, то наблюдается
явлениетепловой эффузии.А если
по разные стороны перегородки находятся
разные газы при одних и тех же начальных
давлениях и температурах – наблюдается
явлениеизотермической эффузии.
На схеме 17.4.1 наглядно представлены
необходимые начальные условия для
тепловой и изотермической эффузии.
Схема 17.4.1.
Число частиц в эффузионном потоке через пористую перегородку в одном направлении равно

здесь произведение всех констант
обозначено
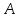 .
Результирующий поток складывается из
двух встречных потоков
.
Результирующий поток складывается из
двух встречных потоков и
и
в равновесном состоянии равен нулю.
В случае тепловой эффузии, когда молекулы тождественны, равновесному состоянию согласно (17.15) соответствует равенство

или

Очевидно, что в той половинке сосуда,
где температура больше установится и
более высокое давление. Это произойдет
за счет увеличения концентрации частиц
в «теплом» отсеке. Особенно наглядно
это проявляется, если первоначально
давления в разных отсеках были равны
 .
Газ начнет перетекать в направлении
повышения температуры: от более низкой
к более высокой температуре. Явление
тепловой эффузии называют такжеэффектом
Кнудсена.Перефразируя известную
поговорку, можно сказать: «Рыба ищет,
где глубже, а молекула – где теплее».
.
Газ начнет перетекать в направлении
повышения температуры: от более низкой
к более высокой температуре. Явление
тепловой эффузии называют такжеэффектом
Кнудсена.Перефразируя известную
поговорку, можно сказать: «Рыба ищет,
где глубже, а молекула – где теплее».
В случае изотермической эффузии в
начальный момент времени
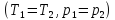 потоки
потоки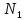 и
и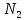 не равны:
не равны:

Если
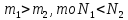 .Это значит, что более легкий газ будет
быстрее проходить через пористую
перегородку, чем более тяжелый. Образно
говоря, стройные молекулы обгоняют
молекулы толстушки. При
.Это значит, что более легкий газ будет
быстрее проходить через пористую
перегородку, чем более тяжелый. Образно
говоря, стройные молекулы обгоняют
молекулы толстушки. При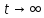 происходит одновременное выравнивание
давления по обе стороны перегородки и
концентрации молекул с разными массами.
Зависимость
происходит одновременное выравнивание
давления по обе стороны перегородки и
концентрации молекул с разными массами.
Зависимость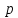 от времени по разные стороны перегородки
показана на рис.17.4:
от времени по разные стороны перегородки
показана на рис.17.4:
Рассмотренные виды эффузии имеют
практическое значение. Изотермическая
эффузия лежит в основе одного из методов
разделения изотопов. Тепловая эффузия
играет важную роль в явлениях природы,
обеспечивая обмен воздуха в почве,
необходимый для нормальной жизни
растений. Дадим пояснения этому
практически значимому феномену.
Рис. 17.4.
Летом в дневное время суток поверхность земли нагревается солнечным излучением. Поэтому воздух из более глубоких и менее нагретых слоев почвы выходит по капиллярам природного происхождения наверх и разносится ветром. Ночью верхний слой земли охлаждается и возникает обратный поток воздуха с поверхности в более глубокие слои почвы. Таким образом, осуществляется суточная циркуляция воздуха в плодородных слоях земли.
В заключение темы отметим, что рассмотренные нами процессы переноса в газах не исчерпывают всех явлений такого рода. Например, в плотных газах мы обошли вниманием взаимную диффузию различных газов, а также термодиффузию. Остались в запасниках и некоторые явления в ультраразреженных газах, например, такие как течение Кнудсена, тепловое скольжение, радиометрический эффект. Вот уж воистину, чем больше узнаешь, тем больше граница с непознанным…
Контрольные вопросы
1. Назовите параметры, определяющие интенсивность столкновений молекул друг с другом.
2. Как определяется вероятность столкновения молекулы с другими частицами?
3. Что характеризует эффективное сечение молекулы?
4. Какого рода столкновения молекул определяют явления переноса?
5. Как
определяется
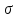 в модели твердых тел?
в модели твердых тел?
6. Как
определяется
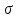 в теории Сёзерленда?
в теории Сёзерленда?
7. Дайте определение средней длины свободного пробега молекул.
8. Назовите исходные положения, необходимые для вывода обобщенного уравнения переноса. Запишите это уравнение.
9. На основе обобщенного уравнения переноса получите выражение для а) теплопроводности; б) вязкости; в) коэффициента диффузии.
10. Раскройте физическую (микроскопическую) сущность явлений переноса.
11. Какие существуют градации состояний разреженного газа?
12. Назовите явления переноса в ультраразреженном газе, которые были рассмотрены на этой лекции? Какие эффекты и количественные соотношения для них характерны?
ЛЕКЦИЯ 18
АТМОСФЕРЫ ПЛАНЕТ
