
- •Содержание
- •§ 2. Краткий исторический очерк возникновения и развития отечественной токсикологической химии
- •Глава I. Общие вопросы химико-токсикологического анализа
- •§ 1. Объекты химико-токсикологического анализа. Вещественные доказательсва
- •§ 2. Особенности химико-токсикологического анализа
- •§ 3. Осмотр объектов исследования и определение некоторых их свойств
- •§ 4. Предварительные пробы в химико-токсикологическом анализе
- •§ 5. План химико-токсикологического анализа
- •§ 6. Организация органов судебно-медицинской и судебно-химической экспертизы в ссср
- •§ 7. Эксперт-химик
- •§ 8. Правила судебно-химической экспертизы вещественных доказательств
- •§ 9. Акт судебно-химической экспертизы вещественных доказательств
- •§ 10. Некоторые вопросы терминологии в токсикологической химии
- •§ 11. Классификация ядовитых и сильнодействующих веществ в токсикологической химии
- •Глава II. Отравления и некоторые вопросы токсикокинетики ядов
- •§ 1. Отравления и их классификация
- •§ 2. Пути поступления ядов в организм
- •§ 3. Всасывание ядов в организме
- •§ 4. Распределение ядов в организме
- •§ 5. Связывание ядов в организме
- •§ 6. Выделение ядов из организма
- •§ 7. Факторы, влияющие на токсичность химических соединений
- •§ 8. Методы детоксикации
- •§ 9. Метаболизм чужеродных соединений
- •§ 10. Окисление чужеродных соединений
- •§ 11. Восстановление чужеродных соединений
- •§ 12. Гидролиз чужеродных соединений
- •§ 13. Дезалкилирование, дезаминирование и десульфирование чужеродных соединений
- •§ 14. Другие метаболические превращения
- •§ 15. Реакции конъюгации
- •§ 16. Посмертные изменения лекарственных веществ и ядов в трупах
- •§ 17. Разложение биологического материала после наступления смерти
- •§ 18. Изменение ядов при разложении трупов
- •Глава III. Методы анализа, применяемые в токсикологической химии
- •§ 1. Метод экстракции
- •§ 2. Микрокристаллоскопический анализ
- •§ 3. Метод микродиффузии
- •Глава IV. Ядовитые и сильнодействующие вещества, изолируемые из биологического материала перегонкой с водяным паром
- •§ 1. Аппараты для перегонки с водяным паром
- •§2. Влияние рН среды на перегонку химических соединений с водяным паром
- •§ 3. Перегонка ядовитых веществ с водяным паром из подкисленного биологического материала
- •§ 4. Перегонка ядовитых веществ с водяным паром из подкисленного, а затем из подщелоченного биологического материала
- •§ 5. Фракционная перегонка веществ, содержащихся в дистиллятах
- •§ 6. Синильная кислота
- •§ 7. Формальдегид
- •§ 8. Метиловый спирт
- •§ 9. Этиловый спирт
- •§ 10. Изоамиловый спирт
- •§ 11. Ацетон
- •§ 12. Фенол
- •§ 13. Крезолы
- •§ 14. Хлороформ
- •§ 15. Хлоралгидрат
- •§ 16. Четыреххлористый углерод
- •§ 17. Дихлорэтан
- •§ 18. Реакции, позволяющие отличить хлорпроизводные друг от друга
- •§ 19. Тетраэтилсвинец
- •§ 20. Уксусная кислота
- •§ 21. Этиленгликоль
- •Глава V. Ядовитые и сильнодействующие вещества, изолируемые из биологического материала подкисленным этиловым спиртом или подкисленной водой
- •§ 1. Развитие методов выделения алкалоидов и других азотистых оснований из биологического материала
- •§ 2. Влияние рН среды на изолирование алкалоидов и других азотистых оснований из биологического материала
- •§ 3. Влияние состава извлекающих жидкостей на изолирование алкалоидов и других азотистых основании из биологического материала
- •§ 4. Влияние подкисленной воды и подкисленного спирта на извлечение примесей, переходящих в вытяжки из биологического материала
- •§ 5. Очистка вытяжек из биологического материала от примесей
- •§ 6. Экстракция алкалоидов и других токсических веществ из вытяжек
- •§ 7. Обнаружение ядовитых веществ, изолируемых подкисленной водой или подкисленным этиловым спиртом
- •§ 8. Количественное определение токсических веществ, изолированных подкисленной водой или подкисленным спиртом
- •§ 9. Метод выделения токсических веществ, основанный на изолировании их этиловым спиртом подкисленным щавелевой кислотой
- •§ 10. Метод выделения токсических веществ, основанный на изолировании их водой, подкисленной щавелевой кислотой
- •§ 11. Метод выделения токсических веществ, основанный на изолировании их водой, подкисленной серной кислотой
- •§ 12. Барбитураты и методы их исследования
- •§ 13. Барбамил
- •§ 14. Барбитал
- •§ 15. Фенобарбитал
- •§ 16. Бутобарбитал
- •§ 17. Этаминал-натрий
- •8.Обнаружение этаминала-натрия по уф- и ик-спектрам.
- •§ 18. Бензонал
- •§ 19. Гексенал
- •§ 20. Производные ксантина
- •§ 21. Кофеин
- •§ 22. Теобромин
- •§ 23. Теофиллин
- •§ 24. Наркотин
- •§ 25. Меконовая кислота
- •§ 26. Меконин
- •§ 27. Ноксирон
- •§ 28. Салициловая кислота
- •§ 29. Антипирин
- •§ 30. Амидопирин
- •§ 31. Фенацетин
- •§ 32. Хинин
- •§ 33. Опий и омнопон
- •§ 34. Морфин
- •§ 35. Кодеин
- •§ 36. Папаверин
- •§ 37. Галантамин
- •§ 38. Анабазин
- •§ 39. Никотин
- •§ 40. Ареколин
- •§ 41. Кониин
- •§ 42. Атропин
- •§ 43. Скополамин
- •§ 44. Кокаин
- •§ 45. Стрихнин
- •§ 46. Бруцин
- •§ 47. Резерпин
- •§ 48. Пахикарпин
- •§ 49. Секуренин
- •§ 50. Эфедрин
- •§ 51. Аконитин
- •§ 52. Новокаин
- •§ 53. Дикаин
- •§ 54. Аминазин
- •§ 55. Дипразин
- •§ 56. Тизерцин
- •§ 57. Хлордиазепоксид
- •§ 58. Диазепам
- •§ 59. Нитразепам
- •§ 60. Оксазепам
- •§ 61. Апоморфин
- •§ 62. Дионин
- •§ 63. Промедол
- •Глава VI. Вещества, изолируемые из объектов минерализацией биологического материала
- •§ 1. Связывание «металлических ядов» биологическим материалом
- •§ 2. Методы минерализации органических веществ
- •§ 3. Сухое озоление и сплавление органических веществ
- •§ 4. Окислители, применяемые для минерализации органических веществ
- •§ 5. Отбор и подготовка проб биологического материала для минерализации
- •§ 6. Разрушение биологического материала азотной и серной кислотами
- •§ 7. Разрушение биологического материала хлорной, азотной и серной кислотами
- •§ 8. Разрушение биологического материала пергидролем и серной кислотой
- •§ 9. Дробный метод и систематический ход анализа «металлических ядов»
- •§ 10. Маскировка ионов в дробном анализе
- •§ 11. Реактивы, применяемые в дробном анализе «металлических ядов» для маскировки ионов
- •§ 12. Реакции, применяемые в химико-токсикологическом анализе для обнаружения ионов металлов
- •§ 13. Соединения бария
- •§ 14. Соединения свинца
- •§ 15. Соединения висмута
- •§ 16. Соединения кадмия
- •§ 17. Соединения марганца
- •§ 18. Соединения меди
- •§ 19. Соединения мышьяка
- •§ 20. Соединения серебра
- •§ 21. Соединения сурьмы
- •§ 22. Соединения таллия
- •§ 23. Соединения хрома
- •§ 24, Соединения цинка
- •§ 25. Соединения ртути
- •§ 26. Количественное определение «металлических ядов» в минерализатах
- •§ 27. Количественное определение ртути
- •§ 28. Экстракционно-фотоколориметрическое определение меди
- •Глава VII. Вещества, изолируемые из биологического материала настаиванием исследуемых объектов с водой
- •Минеральные кислоты и щелочи
- •§ 1. Серная кислота
- •§ 2. Азотная кислота
- •§ 3. Соляная кислота
- •§ 4. Гидроксид калия
- •§ 5. Гидроксид натрия
- •§ 6. Аммиак
- •§ 7. Нитриты
- •Глава VIII. Ядохимикаты и методы их химико-токсикологического анализа
- •§ 1. Классификация ядохимикатов
- •§ 2. Гексахлорциклогексан (гхцг)
- •§ 3. Гептахлор
- •§ 4. Фосфорсодержащие органические соединения и методы их анализа
- •§ 5. Хлорофос
- •§ 6. Карбофос
- •§ 7. Метафос
- •§ 8. Карбарил
- •§ 9. Гранозан
- •Глава IX. Вещества, определяемые непосредственно в биологическом материале
- •§ 1. Оксид углерода (II)
- •§ 2. Спектроскопический метод обнаружения оксида углерода (II) в крови
- •§ 3. Химические методы обнаружения оксида углерода (II) в крови
- •§ 4. Количественное определение оксида углерода (II) в крови
- •Приложение 1. Приготовление реактивов
- •Приложение 2. Приготовление хроматографических пластинок
- •Список рекомендуемой литературы
Минеральные кислоты и щелочи
Для доказательства присутствия минеральных кислот в диализатах определяют кислотность этих жидкостейи наличие в ниханионовсоответствующих кислот.
Определение кислотности диализатов проводится с помощью кислотно-основных индикаторов, которые изменяют свою окраску в кислой среде (метиловый фиолетовый,метиловый оранжевый,конго красныйи др.).
К небольшому объему диализата прибавляют несколько капель раствораиндикатора, изменение окраски которого указывает на наличие кислот в исследуемыхжидкостях. От прибавленияраствораметилового фиолетового(интервал рН перехода окраски 0,1—1,5 и 1,5—3,2) к исследуемойжидкостис рН= 1,5...3,2 зеленая окраскаиндикаторапереходит в фиолетовую. Красная окраскаметилового оранжевогопри рН = 3,0...4,4 переходит в желтую. Сине-фиолетовая окраскаконго красногопри рН = 3,0...5,2 переходит в красную. Для проверки кислотности вытяжек (диализатов) и для ориентировочного определения рН среды может быть использованабумага, пропитанная универсальныминдикатором.
После того как установлена ярко выраженная кислая реакция вытяжек из биологического материала или диализатов, проводят исследование этих жидкостейна наличиеанионовсерной, азотной, соляной и других кислот.
Обнаружение сульфат-ионов, хлорид-ионов и ионовдругих кислот в вытяжках (диализатах) еще не является доказательством отравлений серной, соляной или другой кислотой. Это объясняется тем, чтоанионыуказанных кислот могут быть ворганизмекак составная часть органов итканей.
Для доказательства отравлений минеральными кислотами необходимо отогнать их из диализатов. При этом отгоняются только свободные кислоты. Солиэтих кислот, поступившие в вытяжки из исследуемых объектов, не перегоняются. Учитывая то, что серная иазотная кислотыперегоняются при относительно высокойтемпературе, вначале эти кислоты переводят в более летучие соединения, которые в процессеперегонкилегко переходят в дистилляты.
§ 1. Серная кислота
На отравление серной кислотойможет указывать внешний вид объектов исследования. Так, например, у лиц, принявших концентрированнуюсерную кислоту, могут быть повреждениятканейгуб, языка, пищевода, желудка и т. д. Одежда, на которую попаласерная кислота, может быть повреждена. Однако доказательством отравлениясерной кислотойявляется обнаружение ее в дистиллятах, полученных послеперегонкиэтой кислоты из диализатов.
Выделение серной кислоты из биологического материала. Подлежащие исследованию органы трупов измельчают, заливаютводойдо получения кашицеобразной массы, которую оставляют на 1—2 ч. Полученную вытяжку отфильтровывают, подвергаютдиализу, а затем из диализата отгоняютсерную кислоту.
При химико-токсикологическом исследовании серной кислотына одежде или на других объектах эту кислоту можно извлечьэтиловым спиртом, в котором растворяется эта кислота и не растворяются еесоли. С этой целью исследуемый материал измельчают и прибавляют к немуэтиловый спирт. Через некоторое времяжидкостьотфильтровывают от твердых частиц исследуемого материала. Фильтрат на водяной бане выпаривают досуха. К сухому остатку прибавляют 10 млводы, кипятят несколько минут, а затем охлаждаютжидкостьдо комнатнойтемпературы. Из полученнойжидкостиотгоняютсерную кислотуи исследуют ее в дистилляте.
Отгонка серной кислоты. К диализатам прибавляют медныеопилкии нагревают. При этом образуетсяангидрид сернистойкислоты SO2, который отгоняют и собирают в приемник, содержащийраствориода. При взаимодействииангидрида сернистойкислоты сводойииодомобразуетсясерная кислота:

Способ отгонки серной кислотысостоит в следующем: в колбуаппаратадля отгонкижидкостей, состоящего из колбы, холодильника с форштосом и приемника, вносят диализат и медныеопилки. Конец форштоса опускают в приемник, содержащийраствориода. Колбу устанавливают на масляную или песочную баню и нагревают. Если во времяперегонкипроисходит быстрое обесцвечиваниеиода, то егорастворнебольшими порциями дополнительно вносят в приемник. После окончания отгонкисерной кислотыв приемник прибавляют 2—3 мл разбавленнойсоляной кислотыи нагреваютжидкостьдо полного исчезновенияиода, не вступившего в реакцию сангидридом сернистойкислоты. Освобожденный отиодадистиллят используют для обнаружения в немсерной кислоты.
Для обнаружения серной кислотыв дистилляте применяют реакции схлоридом бария,ацетатом свинцаи родизонатомнатрия.
Реакция с хлоридом бария. К 3—5 каплям дистиллята прибавляют 1—2 капли 5 %-горастворахлорида бария. Появление белого осадкасульфата барияуказывает на наличие серной кис-
лоты в дистилляте. Образовавшийся осадок не растворяется в азотной и соляной кислотах, а также вщелочах.
Реакция с ацетатом свинца. К нескольким каплям дистиллята прибавляют 2—3 капли 3 %-гораствораацетата свинца. При наличиисерной кислотывыпадает белый осадоксульфата свинца, который не растворяется вазотной кислоте, но растворяется в едкихщелочахи враствореацетата аммонияпри нагревании:

Реакция с родизонатом натрия основана на том, что родизо-натнатрияссолямибарияобразует родизонатбария, имеющий красную окраску. От прибавлениясерной кислотыили сульфатов к родизонатубарияон разлагается. При этом образуется осадоксульфата барияи исчезает красная окраска родизоната:
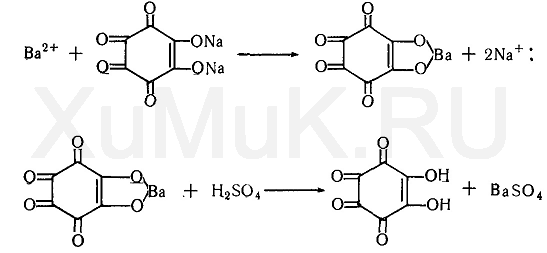
Выполнение реакции. Нафильтровальную бумагунаносят каплю 1 %-горастворахлорида барияи каплю свежеприготовленного 0,2 %-горастворародизонатанатрия. При этом набумагепятно приобретает красную окраску. На это пятно наносят 1—2 капли дистиллята. В присутствиисерной кислотыокраска пятна исчезает. Эта реакция является специфичной на сульфаты исерную кислоту.
