
- •Содержание
- •§ 2. Краткий исторический очерк возникновения и развития отечественной токсикологической химии
- •Глава I. Общие вопросы химико-токсикологического анализа
- •§ 1. Объекты химико-токсикологического анализа. Вещественные доказательсва
- •§ 2. Особенности химико-токсикологического анализа
- •§ 3. Осмотр объектов исследования и определение некоторых их свойств
- •§ 4. Предварительные пробы в химико-токсикологическом анализе
- •§ 5. План химико-токсикологического анализа
- •§ 6. Организация органов судебно-медицинской и судебно-химической экспертизы в ссср
- •§ 7. Эксперт-химик
- •§ 8. Правила судебно-химической экспертизы вещественных доказательств
- •§ 9. Акт судебно-химической экспертизы вещественных доказательств
- •§ 10. Некоторые вопросы терминологии в токсикологической химии
- •§ 11. Классификация ядовитых и сильнодействующих веществ в токсикологической химии
- •Глава II. Отравления и некоторые вопросы токсикокинетики ядов
- •§ 1. Отравления и их классификация
- •§ 2. Пути поступления ядов в организм
- •§ 3. Всасывание ядов в организме
- •§ 4. Распределение ядов в организме
- •§ 5. Связывание ядов в организме
- •§ 6. Выделение ядов из организма
- •§ 7. Факторы, влияющие на токсичность химических соединений
- •§ 8. Методы детоксикации
- •§ 9. Метаболизм чужеродных соединений
- •§ 10. Окисление чужеродных соединений
- •§ 11. Восстановление чужеродных соединений
- •§ 12. Гидролиз чужеродных соединений
- •§ 13. Дезалкилирование, дезаминирование и десульфирование чужеродных соединений
- •§ 14. Другие метаболические превращения
- •§ 15. Реакции конъюгации
- •§ 16. Посмертные изменения лекарственных веществ и ядов в трупах
- •§ 17. Разложение биологического материала после наступления смерти
- •§ 18. Изменение ядов при разложении трупов
- •Глава III. Методы анализа, применяемые в токсикологической химии
- •§ 1. Метод экстракции
- •§ 2. Микрокристаллоскопический анализ
- •§ 3. Метод микродиффузии
- •Глава IV. Ядовитые и сильнодействующие вещества, изолируемые из биологического материала перегонкой с водяным паром
- •§ 1. Аппараты для перегонки с водяным паром
- •§2. Влияние рН среды на перегонку химических соединений с водяным паром
- •§ 3. Перегонка ядовитых веществ с водяным паром из подкисленного биологического материала
- •§ 4. Перегонка ядовитых веществ с водяным паром из подкисленного, а затем из подщелоченного биологического материала
- •§ 5. Фракционная перегонка веществ, содержащихся в дистиллятах
- •§ 6. Синильная кислота
- •§ 7. Формальдегид
- •§ 8. Метиловый спирт
- •§ 9. Этиловый спирт
- •§ 10. Изоамиловый спирт
- •§ 11. Ацетон
- •§ 12. Фенол
- •§ 13. Крезолы
- •§ 14. Хлороформ
- •§ 15. Хлоралгидрат
- •§ 16. Четыреххлористый углерод
- •§ 17. Дихлорэтан
- •§ 18. Реакции, позволяющие отличить хлорпроизводные друг от друга
- •§ 19. Тетраэтилсвинец
- •§ 20. Уксусная кислота
- •§ 21. Этиленгликоль
- •Глава V. Ядовитые и сильнодействующие вещества, изолируемые из биологического материала подкисленным этиловым спиртом или подкисленной водой
- •§ 1. Развитие методов выделения алкалоидов и других азотистых оснований из биологического материала
- •§ 2. Влияние рН среды на изолирование алкалоидов и других азотистых оснований из биологического материала
- •§ 3. Влияние состава извлекающих жидкостей на изолирование алкалоидов и других азотистых основании из биологического материала
- •§ 4. Влияние подкисленной воды и подкисленного спирта на извлечение примесей, переходящих в вытяжки из биологического материала
- •§ 5. Очистка вытяжек из биологического материала от примесей
- •§ 6. Экстракция алкалоидов и других токсических веществ из вытяжек
- •§ 7. Обнаружение ядовитых веществ, изолируемых подкисленной водой или подкисленным этиловым спиртом
- •§ 8. Количественное определение токсических веществ, изолированных подкисленной водой или подкисленным спиртом
- •§ 9. Метод выделения токсических веществ, основанный на изолировании их этиловым спиртом подкисленным щавелевой кислотой
- •§ 10. Метод выделения токсических веществ, основанный на изолировании их водой, подкисленной щавелевой кислотой
- •§ 11. Метод выделения токсических веществ, основанный на изолировании их водой, подкисленной серной кислотой
- •§ 12. Барбитураты и методы их исследования
- •§ 13. Барбамил
- •§ 14. Барбитал
- •§ 15. Фенобарбитал
- •§ 16. Бутобарбитал
- •§ 17. Этаминал-натрий
- •8.Обнаружение этаминала-натрия по уф- и ик-спектрам.
- •§ 18. Бензонал
- •§ 19. Гексенал
- •§ 20. Производные ксантина
- •§ 21. Кофеин
- •§ 22. Теобромин
- •§ 23. Теофиллин
- •§ 24. Наркотин
- •§ 25. Меконовая кислота
- •§ 26. Меконин
- •§ 27. Ноксирон
- •§ 28. Салициловая кислота
- •§ 29. Антипирин
- •§ 30. Амидопирин
- •§ 31. Фенацетин
- •§ 32. Хинин
- •§ 33. Опий и омнопон
- •§ 34. Морфин
- •§ 35. Кодеин
- •§ 36. Папаверин
- •§ 37. Галантамин
- •§ 38. Анабазин
- •§ 39. Никотин
- •§ 40. Ареколин
- •§ 41. Кониин
- •§ 42. Атропин
- •§ 43. Скополамин
- •§ 44. Кокаин
- •§ 45. Стрихнин
- •§ 46. Бруцин
- •§ 47. Резерпин
- •§ 48. Пахикарпин
- •§ 49. Секуренин
- •§ 50. Эфедрин
- •§ 51. Аконитин
- •§ 52. Новокаин
- •§ 53. Дикаин
- •§ 54. Аминазин
- •§ 55. Дипразин
- •§ 56. Тизерцин
- •§ 57. Хлордиазепоксид
- •§ 58. Диазепам
- •§ 59. Нитразепам
- •§ 60. Оксазепам
- •§ 61. Апоморфин
- •§ 62. Дионин
- •§ 63. Промедол
- •Глава VI. Вещества, изолируемые из объектов минерализацией биологического материала
- •§ 1. Связывание «металлических ядов» биологическим материалом
- •§ 2. Методы минерализации органических веществ
- •§ 3. Сухое озоление и сплавление органических веществ
- •§ 4. Окислители, применяемые для минерализации органических веществ
- •§ 5. Отбор и подготовка проб биологического материала для минерализации
- •§ 6. Разрушение биологического материала азотной и серной кислотами
- •§ 7. Разрушение биологического материала хлорной, азотной и серной кислотами
- •§ 8. Разрушение биологического материала пергидролем и серной кислотой
- •§ 9. Дробный метод и систематический ход анализа «металлических ядов»
- •§ 10. Маскировка ионов в дробном анализе
- •§ 11. Реактивы, применяемые в дробном анализе «металлических ядов» для маскировки ионов
- •§ 12. Реакции, применяемые в химико-токсикологическом анализе для обнаружения ионов металлов
- •§ 13. Соединения бария
- •§ 14. Соединения свинца
- •§ 15. Соединения висмута
- •§ 16. Соединения кадмия
- •§ 17. Соединения марганца
- •§ 18. Соединения меди
- •§ 19. Соединения мышьяка
- •§ 20. Соединения серебра
- •§ 21. Соединения сурьмы
- •§ 22. Соединения таллия
- •§ 23. Соединения хрома
- •§ 24, Соединения цинка
- •§ 25. Соединения ртути
- •§ 26. Количественное определение «металлических ядов» в минерализатах
- •§ 27. Количественное определение ртути
- •§ 28. Экстракционно-фотоколориметрическое определение меди
- •Глава VII. Вещества, изолируемые из биологического материала настаиванием исследуемых объектов с водой
- •Минеральные кислоты и щелочи
- •§ 1. Серная кислота
- •§ 2. Азотная кислота
- •§ 3. Соляная кислота
- •§ 4. Гидроксид калия
- •§ 5. Гидроксид натрия
- •§ 6. Аммиак
- •§ 7. Нитриты
- •Глава VIII. Ядохимикаты и методы их химико-токсикологического анализа
- •§ 1. Классификация ядохимикатов
- •§ 2. Гексахлорциклогексан (гхцг)
- •§ 3. Гептахлор
- •§ 4. Фосфорсодержащие органические соединения и методы их анализа
- •§ 5. Хлорофос
- •§ 6. Карбофос
- •§ 7. Метафос
- •§ 8. Карбарил
- •§ 9. Гранозан
- •Глава IX. Вещества, определяемые непосредственно в биологическом материале
- •§ 1. Оксид углерода (II)
- •§ 2. Спектроскопический метод обнаружения оксида углерода (II) в крови
- •§ 3. Химические методы обнаружения оксида углерода (II) в крови
- •§ 4. Количественное определение оксида углерода (II) в крови
- •Приложение 1. Приготовление реактивов
- •Приложение 2. Приготовление хроматографических пластинок
- •Список рекомендуемой литературы
§ 35. Кодеин
Кодеинпредставляет собой монометиловый эфирморфина. Он является одним изалкалоидовопия. В опии, полученном из снотворного мака, содержится 0,2—2 %кодеина. В отдельныхсортахиндийского опия содержится около 6 %кодеина.Кодеинявляется сильным основанием, которое не осаждаетсяаммиаком. Основаниекодеинарастворяется в холодной (1 : 120) и кипящейводе(1 :20),диэтиловом эфире(1 : 50),хлороформе(1:2) иэтиловом спирте(1:2). Гидрохлоридкодеинаслабо растворяется вхлороформе(1 : 800), лучше —вэтиловом спирте(1:100) иводе(1 : 30).Фосфат кодеинаплохо растворяется вэтиловом спирте(1 : 450),диэтиловом эфиреихлороформе, лучше — вводе(1 :4), сульфаткодеинаплохо растворяется вэтиловом спирте(1:1300),диэтиловом эфиреихлороформе, лучше — вводе(1:30).
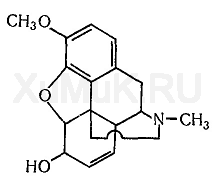
Кодеинэкстрагируется органическимирастворителямииз подщелоченных водных вытяжек. Максимальные количествакодеинаэкстрагируютсяхлороформомпри рН = 8,0...3,5.
Применение. Действие на организм. Кодеинприменяется в медицине в виде основания и фосфата. По действию наорганизмкодеинблизок кморфину. Однако болеутоляющее свойствокодеинавыражено слабее, чем уморфина.Кодеинв меньшей степени, чемморфин, угнетаетдыхание.Кодеинуменьшает возбудимость кашлевого центра, и поэтому назначается для успокоения кашля, в сочетании санальгином,амидопирином,кофеином, фенобарбиталом и другими препаратами применяется при головных болях, невралгиях и т. д.Кодеинменее токсичен, чемморфин. Однако при частом, повторяющемся приемекодеинавозможно привыкание к нему.
Метаболизм. Кодеинподвергаетсяметаболизмутремя путями. Частькодеинасвязывается сглюкуроновой кислотойи выделяется изорганизмас мочой в виде глюкуронида. Некоторое количествокодеинаподвергается О-деметилированию (образуется морфин) и N-деметилированию (образуется норкодеин). Образовавшиесяметаболиты(морфин и норкодеин) выделяется с мочой в виде глюкуронидов. Незначительная частькодеинавыделяется с мочой в несвязанном виде. Через 6 ч после поступлениякодеинав кровь изорганизмавыделяется около двух третихдозыэтогоалкалоида, а через 24 ч он почти полностью исчезает изорганизма.
Обнаружение кодеина
Предварительная проба на наличие кодеина в моче. В делительную воронку вносят 50 мл мочи, подщелачиваютраствором аммиакадо рН=10, прибавляют 50 млхлороформаи взбалтывают в течение 5 мин. Хлороформную вытяжку отделяют от водной фазы, вытяжку взбалтывают с 3 млводыв течение 3 мин. Водную фазу отделяют отхлороформа, фильтруют через безводныйсульфат натрияи выпаривают досуха. Сухой остаток растворяют в 1 млэтилового спирта. Полученный спиртовойраствориспользуют для обнаружениякодеинаодним из следующих способов:
а) на фильтровальную бумагунаносят каплю полученного спиртовогораствораи прибавляют каплю реактива Марки. При наличиикодеинапятно приобретает красноватую окраску, переходящую в сине-фиолетовую;
б) на фильтровальную бумагунаносят каплю указанного выше спиртовогораствораи прибавляют каплю 0,5%-гораствораванадатааммонияи каплю 2 %-горастворасерной кислоты. При наличиикодеинапоявляется зеленая окраска, переходящая в синюю.
Для подтверждения результатов указанных реакций необходимо призвести обнаружение кодеинав вытяжке методомхроматографиив тонком слое сорбента.
Реакция с реактивами группового осаждения алкалоидов. При взаимодействиикодеинас реактивами Драгендорфа, Бушарда, Майера и другими образуются осадки.
Цветные реакции. Кодеинс реактивами Манделина, Марки и Фредедаетокрашенные продукты реакции, которые описаны выше (см. гл. V,§ 7).
Реакция Пеллагри. При нагреваниикодеинас концентрированнойсоляной кислотой, а затем с концентрированнойсерной кислотойпроисходит деметоксилирование этогоалкалоидаи образуетсяапоморфин, которыйдаетреакцию со спиртовымрастворомиода. Выполнение реакции Пеллагри описано выше (см. гл. V,§ 34).
Обнаружение кодеина методом хроматографии. Налиниюстарта на хроматографической пластинке наносят каплю хлороформногораствораисследуемоговещества. Правее на расстоянии 2 см налиниюстарта наносят каплюраствора«свидетеля» (0,01 %-йрастворкодеина). Пятна нанесенныхрастворовподсушивают навоздухе, а затем пластинку вносят в камеру для хроматографирования, насыщеннуюпарамирастворителей(хлороформ-ацетон-диэтиламин в соотношении 50 : 30 : 2). После продвижения системырастворителейна 10 см вышелиниистарта пластинку вынимают из камеры, подсушивают навоздухеи опрыскивают реактивом Драгендорфа, модифицированным по Мунье.
При наличии кодеинав исследуемомрастворепятна этогоалкалоидаприобретают буровато-розовую окраску (Rf = 0,40± ±0,02).
Приготовление хроматографических пластинок (см. Приложение 2, способ 1).
Обнаружение кодеина по УФ- и ИК-спектрам. Основаниекодеинавраствореэтилового спиртаимеет максимум поглощения при 286 нм; в ИК-области спектра основаниекодеина(диск с бромидом калия) имеет основные пики при 1052 1268, 1500 см-1.
Способы идентификации, позволяющие отличить кодеин от морфина. Ввиду того чтоморфиникодеинявляются близкими по строениюалкалоидами, онидаютряд реакций с одними и теми же реактивами. Однакокодеиннедаетреакций схлоридом железа(III), с НIO3, с гексацианоферратом (III)калияихлоридом железа(III), которыедаетморфин.Кодеинможно отличить отморфинаи по светопоглощению в ИК-области спектра.
Кодеинотличается отморфинаи тем, чтоморфинне экстрагируетсядиэтиловым эфиромиз щелочныхрастворов(образуется морфинат). Это свойство указанныхалкалоидовиспользуется для разделения их в ходе анализа.
Экстракционно-фотоколориметрический метод определения кодеина
Метод фотоколориметрического определения кодеинаоснован на реакции стропеолином00, при которой образуется ионный ассоциат, экстрагирующийсяхлороформом:

Техника определения. 1 мл исследуемогорастворавносят в делительную воронку, прибавляют 9 мл ацетатной буферной смеси (рН = 4,6), 5 мл 0,1 %-го водногорастворатропеолина00 и 5 млхлороформа. Содержимое делительной воронки взбалтывают в течение 5 мин. Через 3 мин от водного слоя отделяют хлороформную вытяжку. Водный слой взбалтывают с новыми порциямихлороформа(по 5 мл) до тех пор, пока 3—4 капли последней хлороформной вытяжки не перестанутдаватьокраску с 1—2 каплями 1 %-гораствораконцентрированнойсерной кислотывметиловом спирте. Хлороформные вытяжки соединяют и доводятхлороформомдо 50 мл. К 5 мл полученного хлороформногораствораприбавляют 20 млхлороформаи 2,5 мл 1 %-гораствораконцентрированнойсерной кислотывметиловом спирте. Затем измеряют оптическую плотность полученного фиолетово-красногорастворас помощью фотоэлектроколориметра ФЭК-М (светофильтр зеленый, кювета 10 мм). В качестверастворасравненияберутхлороформную вытяжку из смеси, совтоящей из 5 мл 0,1 %-горастворатропеолина00, 9 мл ацетатной буферной смеси (рН = 4,6) и 1 млводы. К полученной хлороформной вытяжке прибавляют 2,5 мл 1 %-гораствораконцентрированнойсерной кислотывметиловом спирте.
Расчет содержания кодеинав пробе производят по калибровочному графику. Для построения калибровочного графикаберутделительные воронки, в которые вносят по 0,1; 0,2; 0,4; 0,6; 0,8 и 1 мл стандартногораствора(в 1 мл содержится 2 мг фосфата кодеина). В первые 5 делительных воронок прибавляютводудо 1 мл. Затем во все делительные воронки вносят по 9 мл ацетатной буферной смеси (рН = 4,6), по 5 мл 0,1 %-горастворатропеолина00 и поступают, как указано выше.
С помощью этого метода можно определить от 0,2 до 2,0 мг кодеинав пробе.
