
- •Содержание
- •§ 2. Краткий исторический очерк возникновения и развития отечественной токсикологической химии
- •Глава I. Общие вопросы химико-токсикологического анализа
- •§ 1. Объекты химико-токсикологического анализа. Вещественные доказательсва
- •§ 2. Особенности химико-токсикологического анализа
- •§ 3. Осмотр объектов исследования и определение некоторых их свойств
- •§ 4. Предварительные пробы в химико-токсикологическом анализе
- •§ 5. План химико-токсикологического анализа
- •§ 6. Организация органов судебно-медицинской и судебно-химической экспертизы в ссср
- •§ 7. Эксперт-химик
- •§ 8. Правила судебно-химической экспертизы вещественных доказательств
- •§ 9. Акт судебно-химической экспертизы вещественных доказательств
- •§ 10. Некоторые вопросы терминологии в токсикологической химии
- •§ 11. Классификация ядовитых и сильнодействующих веществ в токсикологической химии
- •Глава II. Отравления и некоторые вопросы токсикокинетики ядов
- •§ 1. Отравления и их классификация
- •§ 2. Пути поступления ядов в организм
- •§ 3. Всасывание ядов в организме
- •§ 4. Распределение ядов в организме
- •§ 5. Связывание ядов в организме
- •§ 6. Выделение ядов из организма
- •§ 7. Факторы, влияющие на токсичность химических соединений
- •§ 8. Методы детоксикации
- •§ 9. Метаболизм чужеродных соединений
- •§ 10. Окисление чужеродных соединений
- •§ 11. Восстановление чужеродных соединений
- •§ 12. Гидролиз чужеродных соединений
- •§ 13. Дезалкилирование, дезаминирование и десульфирование чужеродных соединений
- •§ 14. Другие метаболические превращения
- •§ 15. Реакции конъюгации
- •§ 16. Посмертные изменения лекарственных веществ и ядов в трупах
- •§ 17. Разложение биологического материала после наступления смерти
- •§ 18. Изменение ядов при разложении трупов
- •Глава III. Методы анализа, применяемые в токсикологической химии
- •§ 1. Метод экстракции
- •§ 2. Микрокристаллоскопический анализ
- •§ 3. Метод микродиффузии
- •Глава IV. Ядовитые и сильнодействующие вещества, изолируемые из биологического материала перегонкой с водяным паром
- •§ 1. Аппараты для перегонки с водяным паром
- •§2. Влияние рН среды на перегонку химических соединений с водяным паром
- •§ 3. Перегонка ядовитых веществ с водяным паром из подкисленного биологического материала
- •§ 4. Перегонка ядовитых веществ с водяным паром из подкисленного, а затем из подщелоченного биологического материала
- •§ 5. Фракционная перегонка веществ, содержащихся в дистиллятах
- •§ 6. Синильная кислота
- •§ 7. Формальдегид
- •§ 8. Метиловый спирт
- •§ 9. Этиловый спирт
- •§ 10. Изоамиловый спирт
- •§ 11. Ацетон
- •§ 12. Фенол
- •§ 13. Крезолы
- •§ 14. Хлороформ
- •§ 15. Хлоралгидрат
- •§ 16. Четыреххлористый углерод
- •§ 17. Дихлорэтан
- •§ 18. Реакции, позволяющие отличить хлорпроизводные друг от друга
- •§ 19. Тетраэтилсвинец
- •§ 20. Уксусная кислота
- •§ 21. Этиленгликоль
- •Глава V. Ядовитые и сильнодействующие вещества, изолируемые из биологического материала подкисленным этиловым спиртом или подкисленной водой
- •§ 1. Развитие методов выделения алкалоидов и других азотистых оснований из биологического материала
- •§ 2. Влияние рН среды на изолирование алкалоидов и других азотистых оснований из биологического материала
- •§ 3. Влияние состава извлекающих жидкостей на изолирование алкалоидов и других азотистых основании из биологического материала
- •§ 4. Влияние подкисленной воды и подкисленного спирта на извлечение примесей, переходящих в вытяжки из биологического материала
- •§ 5. Очистка вытяжек из биологического материала от примесей
- •§ 6. Экстракция алкалоидов и других токсических веществ из вытяжек
- •§ 7. Обнаружение ядовитых веществ, изолируемых подкисленной водой или подкисленным этиловым спиртом
- •§ 8. Количественное определение токсических веществ, изолированных подкисленной водой или подкисленным спиртом
- •§ 9. Метод выделения токсических веществ, основанный на изолировании их этиловым спиртом подкисленным щавелевой кислотой
- •§ 10. Метод выделения токсических веществ, основанный на изолировании их водой, подкисленной щавелевой кислотой
- •§ 11. Метод выделения токсических веществ, основанный на изолировании их водой, подкисленной серной кислотой
- •§ 12. Барбитураты и методы их исследования
- •§ 13. Барбамил
- •§ 14. Барбитал
- •§ 15. Фенобарбитал
- •§ 16. Бутобарбитал
- •§ 17. Этаминал-натрий
- •8.Обнаружение этаминала-натрия по уф- и ик-спектрам.
- •§ 18. Бензонал
- •§ 19. Гексенал
- •§ 20. Производные ксантина
- •§ 21. Кофеин
- •§ 22. Теобромин
- •§ 23. Теофиллин
- •§ 24. Наркотин
- •§ 25. Меконовая кислота
- •§ 26. Меконин
- •§ 27. Ноксирон
- •§ 28. Салициловая кислота
- •§ 29. Антипирин
- •§ 30. Амидопирин
- •§ 31. Фенацетин
- •§ 32. Хинин
- •§ 33. Опий и омнопон
- •§ 34. Морфин
- •§ 35. Кодеин
- •§ 36. Папаверин
- •§ 37. Галантамин
- •§ 38. Анабазин
- •§ 39. Никотин
- •§ 40. Ареколин
- •§ 41. Кониин
- •§ 42. Атропин
- •§ 43. Скополамин
- •§ 44. Кокаин
- •§ 45. Стрихнин
- •§ 46. Бруцин
- •§ 47. Резерпин
- •§ 48. Пахикарпин
- •§ 49. Секуренин
- •§ 50. Эфедрин
- •§ 51. Аконитин
- •§ 52. Новокаин
- •§ 53. Дикаин
- •§ 54. Аминазин
- •§ 55. Дипразин
- •§ 56. Тизерцин
- •§ 57. Хлордиазепоксид
- •§ 58. Диазепам
- •§ 59. Нитразепам
- •§ 60. Оксазепам
- •§ 61. Апоморфин
- •§ 62. Дионин
- •§ 63. Промедол
- •Глава VI. Вещества, изолируемые из объектов минерализацией биологического материала
- •§ 1. Связывание «металлических ядов» биологическим материалом
- •§ 2. Методы минерализации органических веществ
- •§ 3. Сухое озоление и сплавление органических веществ
- •§ 4. Окислители, применяемые для минерализации органических веществ
- •§ 5. Отбор и подготовка проб биологического материала для минерализации
- •§ 6. Разрушение биологического материала азотной и серной кислотами
- •§ 7. Разрушение биологического материала хлорной, азотной и серной кислотами
- •§ 8. Разрушение биологического материала пергидролем и серной кислотой
- •§ 9. Дробный метод и систематический ход анализа «металлических ядов»
- •§ 10. Маскировка ионов в дробном анализе
- •§ 11. Реактивы, применяемые в дробном анализе «металлических ядов» для маскировки ионов
- •§ 12. Реакции, применяемые в химико-токсикологическом анализе для обнаружения ионов металлов
- •§ 13. Соединения бария
- •§ 14. Соединения свинца
- •§ 15. Соединения висмута
- •§ 16. Соединения кадмия
- •§ 17. Соединения марганца
- •§ 18. Соединения меди
- •§ 19. Соединения мышьяка
- •§ 20. Соединения серебра
- •§ 21. Соединения сурьмы
- •§ 22. Соединения таллия
- •§ 23. Соединения хрома
- •§ 24, Соединения цинка
- •§ 25. Соединения ртути
- •§ 26. Количественное определение «металлических ядов» в минерализатах
- •§ 27. Количественное определение ртути
- •§ 28. Экстракционно-фотоколориметрическое определение меди
- •Глава VII. Вещества, изолируемые из биологического материала настаиванием исследуемых объектов с водой
- •Минеральные кислоты и щелочи
- •§ 1. Серная кислота
- •§ 2. Азотная кислота
- •§ 3. Соляная кислота
- •§ 4. Гидроксид калия
- •§ 5. Гидроксид натрия
- •§ 6. Аммиак
- •§ 7. Нитриты
- •Глава VIII. Ядохимикаты и методы их химико-токсикологического анализа
- •§ 1. Классификация ядохимикатов
- •§ 2. Гексахлорциклогексан (гхцг)
- •§ 3. Гептахлор
- •§ 4. Фосфорсодержащие органические соединения и методы их анализа
- •§ 5. Хлорофос
- •§ 6. Карбофос
- •§ 7. Метафос
- •§ 8. Карбарил
- •§ 9. Гранозан
- •Глава IX. Вещества, определяемые непосредственно в биологическом материале
- •§ 1. Оксид углерода (II)
- •§ 2. Спектроскопический метод обнаружения оксида углерода (II) в крови
- •§ 3. Химические методы обнаружения оксида углерода (II) в крови
- •§ 4. Количественное определение оксида углерода (II) в крови
- •Приложение 1. Приготовление реактивов
- •Приложение 2. Приготовление хроматографических пластинок
- •Список рекомендуемой литературы
§ 12. Барбитураты и методы их исследования
В современной медицине применяется большое число барбитуратов (производных барбитуровой кислоты). Барбитураты представляют собой одну из групп веществ, имеющих большое токсикологическое значение. Самабарбитуровая кислота(малонилмочевина) не применяется в медицине, зато широко используются ее производные.
Барбитуровая кислотасощелочамиобразуетсоли. Кислотные свойствабарбитуровой кислотыобусловлены наличиематомовводородав — NH-группах, находящихся рядом с карбонильной группой —СО—.
Применяемые в медицине барбитураты являются 5,5-замещен-ными (барбамил, барбитал,фенобарбитали др.) и 1,5,5-замещен-ными (гексенал, гексабарбитал,бензонали др.)барбитуровой кислоты.
Выделение барбитуратов из биологического материала
Для выделения барбитуратов из биологического материала долгое время применялись методы, которые были разработаны для выделения алкалоидов(см. гл. V, § 9—11). В последние десятилетия для выделения барбитуратов из объектов биологического происхождения предложен ряд специальных методов, которые описаны ниже.
Изолирование барбитуратов водой, подкисленной щавелевой кислотой. Оптимальные условия изолирования барбитуратов из биологического материалаводой, подкисленнойщавелевой кислотой, и способ очистки полученных вытяжек разработала М. Д. Швайкова с сотрудниками. Согласно этому методу, в коническую колбу илистаканвносят 100 г тщательно измельченных органов трупов, прибавляют 200 млводы, подкисляют насыщенным воднымрастворомщавелевой кислотыдо рН = 2 (по универсальному индикатору) и оставляют на 2 ч при частомперемешивании. Затем содержимое колбы переносят встакандляцентрифугированиявместимостью 500 мл и центрифугируют в течение 30 мин (3000 об/мин). Центрифугат сливают с осадка и процеживают черезватный тампон. Процеженнуюжидкостьсобирают в делительную воронку и проверяют рН этойжидкости. В случае необходимостижидкостьдоводят до рН = 2. Содержимое делительной воронки взбалтывают с тремя порциямихлороформа(по 20, 15 и 15 мл) в течение 5 мин. Если образуетсяэмульсия, то ее разрушаютцентрифугированием.
Хлороформные вытяжки соединяют, доводят хлороформомдо 50 мл и переносят в делительную воронку, в которую прибавляют 25 мл 0,1 н.растворагидроксида натрия, и взбалтывают. Водную фазу отделяют от хлороформной вытяжки. Эту вытяжку взбалтывают с двумя порциямиводыпо 1,5 мл. Первую и вторую порцииводы(по 1,5 мл), которыми промывали хлороформные вытяжки, присоединяют к щелочной водной фазе. Потом водную фазу подкисляютсоляной кислотойдо рН = 2, вносят в делительную воронку и взбалтывают с двумя новыми порциямихлороформа(по 20 мл) в течение 5 мин. Хлороформные вытяжки соединяют и доводятхлороформомдо 50 мл. В этих вытяжках определяют наличие и количественное содержание барбитуратов.
Изолирование барбитуратов водой, подкисленнойсерной кислотой. Метод выделения барбитуратов из биологического материала, основанный на изолировании этихвеществводой, подкисленнойсерной кислотой, разработала В. И. Попова. Согласно этому методу, биологический материал настаивают сводой, подкисленнойсерной кислотой(рН = 2...3). Полученные вытяжки освобождают от примесей методом гель-хроматографии. Для этой цели используетсягельсефадекса G = 25.
В стаканвносят 100 г измельченного биологического материала, прибавляют 80 мл 0,02 н.растворасерной кислоты, перемешивают и проверяют рН среды. При необходимости смесь доводят до рН = 2...3 (по универсальному индикатору) 30 %-мрастворомсерной кислоты. Смесь биологического материала и подкисленнойводынастаивают в течение 2 ч при частомперемешивании. Затем вытяжку сливают, а биологический материал еще 2 раза настаивают с новыми порциями 0,02 н.растворасерной кислоты(по 80 мл) в течение 1 ч. Кислые водные вытяжки соединяют, процеживают через сложенную в три слоямарлюи центрифугируют в течение 25—30 мин.
Надосадочную жидкость(центрифугат) сливают с осадка и очищают от примесей методом гель-хроматографии. Этот метод обеспечивает хорошую очистку барбитуратов, выделенных из биологического материала.
После очистки вытяжек из биологического материала с помощью метода гель-хроматографии получают большие объемы элюатов, в одном миллилитре которых содержатся малые количества барбитуратов. Поэтому барбитураты, находящиеся в элюатах, подвергают экстракционному концентрированию. С этой целью объединенные кислые элюаты 3 раза взбалтывают с новыми порциямихлороформа(по 50 мл) в течение 7 мин. Хлороформные вытяжки, полученные после каждой экстракции, соединяют и на водяной бане при 70 °С отгоняют из них 120—130 млхлороформа. Оставшуюся упаренную хлороформную вытяжку при комнатнойтемпературевыпаривают досуха. Сухие остатки используют дляидентификациии количественного определения барбитуратов при помощи соответствующих реакций и методов.
Изолирование барбитуратов подщелоченной водой. Подщелоченнуюводудля изолирования барбитуратов из биологического материала впервые применил П. Валов. Дляосажденияпримесей, переходящих из биологического материала в вытяжки, он использовалвольфрамат натрия. В настоящее время известно несколько модификаций метода Валова. Одна из модификаций метода Валова, предложенная М. Д. Швайковой с сотрудниками, приводится ниже.
В стаканили в коническую колбу вносят 100 г измельченного биологического материала, прибавляют 180 млводыи 20 мл 10 %-горастворагидроксида натрия. Содержимоестакана(или колбы) оставляют на 30 мин при частомперемешивании, а затем центрифугируют в течение 30 мин (3000 об/мин). От осадка отделяют надосадочнуюжидкость(центрифугат), к которой прибавляют 120 мл 10 %-горастворавольфрамата натрияи 1 н.растворсерной кислоты(до pH = 2).Жидкостьнагревают на кипящей водяной бане в течение 20 мин, а затем подвергаютцентрифугированию(30 мин). Центрифугат сливают с осадка и процеживают черезватный тампон, смоченныйводой. Процеженнуюжидкостьсобирают в делительную воронку.Тампонпромываютводой(10 мл). Промывнуюводутоже выливают в делительную воронку. К процеженнойжидкостиприбавляют равный объемдиэтилового эфираи взбалтывают в течение 15 мин. Эфирный слой отделяют и взбалтывают с 50 мл 10 %-горастворагидроксида натрия. Щелочной водный слой отделяют, подкисляют 25 %-мрастворомсерной кислотыдо рН = 2 и взбалтывают с равным объемомдиэтилового эфира. Полученную при этом эфирную вытяжку используют для обнаружения и количественного определения барбитуратов.
Обнаружение барбитуратов
Для обнаружения барбитуратов применяются цветные реакции, реакции осаждения, микрокристаллоскопические реакции, методыхроматографии, УФ- и ИК-спектроскопии и др.
Предварительная проба. Для обнаружения барбитуратов в моче применяют предварительную пробу, основанную на реакции этих веществсацетатом кобальтаигидроксидом лития.
В делительную воронку вносят 50 мл мочи, к которой по каплям прибавляют 10 %-й растворсерной кислотыдо рН = 4...5 и 50 млдиэтилового эфира. Содержимое делительной воронки взбалтывают. После разделения фаз отделяют эфирную вытяжку. Водную фазу еще раз взбалтывают с 50 млдиэтилового эфира.
Эфирные вытяжки соединяют и выпаривают досуха. Сухой остаток растворяют в 1 мл хлороформа. К хлороформномурастворуприбавляют 2 капли свежеприготовленного 1 %-гораствораацетата кобальтавметиловом спиртеи несколько капель свежеприготовленного 1 %-горастворагидроксида литиявметиловом спирте. После прибавления каждой капли указанных реактивовжидкостьвзбалтывают. Появление голубой окраски указывает на наличие барбитуратов в моче.
Реакция барбитуратов с изопропиламином и солями кобальта.Для обнаружения барбитуратов Парри (1924) предложил реакцию, основанную на взаимодействии этихвеществссолямикобальтаиаммиаком. Позднее другие исследователиаммиакзаменилиизопропиламином. При взаимодействии барбитуратов сизопропиламиномисолямикобальтаобразуются внутриком-плексные соединения:

Выполнение реакции.К 2 мл хлороформногораствораисследуемоговеществаприбавляют 0,3 мл 1 %-гораствораацетата кобальтав безводномэтиловом спиртеи 1 мл 5 %-гораствораизопропиламинавэтиловом спирте. При наличии барбитуратов появляется фиолетовое окрашивание. Вместоэтилового спиртаможно использоватьметиловый спирт.
Реакция с солями кобальта и щелочами.Цвиккер (1931) установил, что от прибавленияхлорида кобальтаигидроксида барияк барбитуратам образуется окрашенное соединение. В 1932 г. Цвиккер вместогидроксида барияприменилгидроксид калия. Другие исследователи вместогидроксида барияприменялигидроксид лития.
Выполнение реакции.Исследуемоевеществоили остаток, полученный послевыпариваниявытяжек из соответствующих объектов, растворяют в 0,2—0,5 мл абсолютногоэтилового спирта. К этомурастворуприбавляют 1—2 капли 1 %-гораствораацетата кобальтав абсолютномэтиловом спиртеи 1—2 капли 1 %-горастворагидроксида калияв абсолютномэтиловом спирте. При наличии барбитуратов появляется розовая или красная окраска.
Выполнению этой реакции мешает вода, которая разлагает окрашенное соединение. Поэтому при выполнении указанной реакции используют реактивы, растворенные в абсолютном этиловом илиметиловом спирте. Оттенок и интенсивность окраски зависят от применяемогоспирта, что объясняется различной соль-ватирующей способностью образовавшихся соединений этимиспиртами. Указанную реакциюдаютнекоторые гидантоины,сульфаниламидные препараты,пурины,пиримидиныи др.
Реакция с пиридином и солями меди.При взаимодействии барбитуратов спиридиномисолямимедиобразуются труднорастворимыекомплексные соединения.
Под влиянием пиридинапроисходят енолизация и частичная ионизация барбитуратов.Пиридинсионамимедиобразует положительно заряженный комплексныйион[Cu(Py)]2+.
При взаимодействии комплекса пиридинасионамимедии ионизированнымимолекуламибарбитуратов образуется внутрикомплексное соединение:
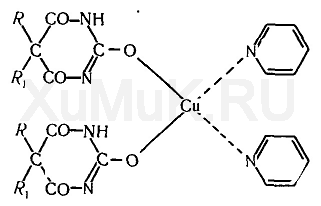
Минеральные кислоты разлагают это соединение.
Осадки, образующиеся при взаимодействии барбитуратов с солямимедиипиридином, могут быть аморфными и кристаллическими.
Выполнение реакции.На предметное стекло наносят несколько капельраствораисследуемоговеществавхлороформеи выпаривают досуха. К сухому остатку прибавляют 2 капли 10 %-гораствора аммиакаи 1—2 капли реактива (растворсульфата медиваммиакеи пиридине). При наличии барбитуратов через 10-15 мин появляются кристаллические или аморфные осадки.
Приготовление реактива(см. Приложение 1, реактив 53).
Мурексидная реакция.Для обнаружения барбитуратов предложено несколько вариантов мурексидной реакции. Один из вариантов этой реакции приводится ниже.
В фарфоровую чашкук сухому остатку, полученному послевыпариваниявытяжек из биологического материала, или к небольшому количеству сухоговеществаприбавляют 3 капли 3 %-горастворапероксида водородаи 3 капли реактива, содержащегосольМора ихлорид аммония. Содержимоечашкивыпаривают, сухой остаток нагревают до появления белыхпаров. После охлаждения прибавляют 3 капли 6 н.раствора аммиака.
При наличии некоторых барбитуратов и тиобарбитуратов появляется розовая окраска.
Мурексидную реакцию даютбарбамил,барбитал,фенобарбитал, этаминал-натрий итиопентал. Недаютэтой реакции гек-сенал, гексобарбитал ициклобарбитал(В. И. Попова).
Приготовление реактива(см. Приложение 1, реактив 51).
Выделение кислотной формы барбитуратов. На предметное стекло наносят несколько капель растворабарбитурата вхлороформе, который выпаривают при комнатнойтемпературе. Послевыпариванияисследуемогорастворана то же место наносят следующую каплю этогораствора, который также выпаривают досуха. Сухой остаток растворяют в одной капле концентрированнойсерной кислоты. Через 3—5 мин после охлаждениярастворарядом с ним наносят каплюводы. Затем эти капли соединяют при помощи капилляра. Через 10—20 мин (а при малых количествах барбитуратов через 1—2 ч) появляются кристаллические осадки. Для каждого барбитуратакристаллыимеют определенную форму.
Гадамер, а также К. П. Стюарт и А. Стольман указывают, что многие барбитураты могут находиться в нескольких полиморфных модификациях. Поэтому при идентификациибарбитуратов по формекристалловнеобходимо учитывать возможность появления нескольких кристаллических форм одного и того жевещества.
Реакция с хлорцинкиодом.На предметное стекло наносят несколько капель хлороформногораствораисследуемоговеществаи выпаривают досуха. К сухому остатку прибавляют 1 каплюрастворахлорцинкиода. Через 10—15 мин под микроскопом наблюдают форму образовавшихсякристаллов. При наличии барбитуратов (барбамил,барбитал, бутобарбитал, эта-минал) в исследуемомрастворепоявляются кристаллические осадки.
Приготовление реактива(см. Приложение 1, реактив 60).
Реакция со смесью растворовхлорида железаииодида калия. На предметное стекло наносят несколько капельраствораисследуемоговеществавхлороформе. Этотрастворвыпаривают досуха. К сухому остатку прибавляют каплю реактива. Через 10— 15 мин под микроскопом наблюдают форму образовавшихсякристаллов, которые появляются при наличии ряда барбитуратов (барбамил, бутобарбитал,фенобарбитал, этаминал).
Приготовление реактива(см. Приложение 1, реактив 57).
Реакция с дииодокупратом калиявраствореиода. На предметное стекло к сухому остатку, полученному послевыпариванияраствораисследуемоговещества, прибавляют каплю реактива. При наличии барбитуратов (барбамил, бутобарбитал, этаминал) образуются кристаллические осадки.
Приготовление реактива(см. Приложение 1, реактив 11).
Реакция с подкисленным спиртовым растворомиодида калия. На предметное стекло к сухому остатку, полученному при выпа-
ривании исследуемого раствора, наносят 2 капли реактива. При наличии барбитуратов (барбитал, бутобарбитал,гексенал, этаминал) через 10—15 мин появляются кристаллические осадки.
Приготовление реактива(см. Приложение 1, реактив 16).
Реакция с родамином 6Ж.При взаимодействииродамина6Ж ссолямибарбитуратов (барбамил,гексенал, этаминал-натрий) образуются окрашенные ионные ассоциаты, экстрагируемыечетыреххлористым углеродом.
Выполнение реакции.В делительную воронку вносят 0,1 млраствораисследуемоговещества, прибавляют 0,2 мл 0,1 %-горастворародамина6Ж и 1 млчетыреххлористого углерода. Смесь взбалтывают в течение 1 мин. При наличиисолейбарбитуратов слойчетыреххлористого углеродаприобретает светло-оранжевую или оранжево-красную окраску.
Эта реакция пригодна для обнаружения барбамила, гексена-ла и этаминал-натрия в фармакопейных препаратах и в лекарственных смесях (В. И. Попова).
Обнаружение барбитуратов по спектрам поглощения в УФ-области. Описанный ниже метод позволяет обнаружить отдельные барбитураты и определить принадлежность их к соответствующим группам барбитуратов.
К сухому остатку, полученному при выпариваниивытяжек из биологического материала или лекарственных форм, прибавляют 5 млводы. Послерастворениясухого остатка полученныйрастворфильтруют, затем к фильтрату прибавляют 1 каплю 2 н.раствора аммиака(рН~10) и снимают спектр поглощения. При этом 5,5-замещенные (барбамил,барбитал, бутобарбитал,фенобарбитал,циклобарбитал, этаминал) и 1,5,5-замещенные (гексенал, гексобарбитал)барбитуровой кислотыимеют максимум поглощения при длине волны около 240 нм, а производные тиобарбитуровой кислоты имеют 2 максимума (при 305 и при 255 нм). Если к этомурастворуприбавить 1—2 капли 2 н.растворасерной кислоты(рН~2), то максимум поглощения 1,5,5- и 5,5-замещенныхбарбитуровой кислотыисчезает. В этих условиях для тиобарбитуратов максимумы поглощения смещаются до 290 и 239 нм. После прибавления к указаннымрастворам1—2 капель 4 н.растворагидроксида натрия(рН~13) появляется максимум поглощения 1,5, 5-замещенныхбарбитуровой кислотыпри 240 нм, а для 5,5-производных этой кислоты — при 255 нм. Для тиобарбитуратов появляется максимум при 305 нм, а второй максимум исчезает.
Обнаружение барбитуратов методом хроматографиив тонком слое сорбента. Для обнаружения барбитуратов применяют методхроматографиив тонком слое сорбента. Этот метод позволяет не только обнаружить отдельные барбитураты, но и отличить их друг от друга.
Способы обнаружения отдельных барбитуратов приведены ниже.
Количественное определение барбитуратов
Для количественного определения барбитуратов, выделенных из биологического материала, применяют фотоколориметрические и спектрофотометрические методы. Один из фотоколориметрических методов количественного определения барбитуратов, разработанный В. И. Поповой, приводится ниже.
Сухие остатки барбитуратов, выделенных из биологического материала методом изолирования этих веществводой, подкисленнойсерной кислотой(см. выше), в зависимости от исследуемого барбитурата растворяют вхлороформеили вметиловом спирте. Сухие остаткибарбитала,гексенала,фенобарбиталаициклобарбиталарастворяют в 6 млхлороформа, а сухие остатки барба-мила и этаминала — в 2 млметилового спирта. Объемырастворовбарбамилаи этаминала вметиловом спиртедоводятхлороформомдо 6 мл. К полученнымрастворамбарбитуратов прибавляют по 5 мл 0,125 %-гораствораацетата кобальтавметиловом спиртеи по 1 мл 50 %-гораствораизопропиламинавметиловом спирте. Оптическую плотность окрашенных в фиолетовый цветрастворовизмеряют при помощи фотоэлектроколориметра ФЭК-М (светофильтр зеленый, кювета 20 мм) или с помощью другой марки фотоэлектроколориметра.
В качестве растворасравнения применяют смесь перечисленных выше реактивов.
