- •Перелік умовних скорочень
- •Структура і функціонування імунної системи
- •Природні бар'єри
- •4) Розселення т- і в-лімфоцитів на периферії та індукція толерант-
- •5) Антигенозалежний етап диференціювання лімфоцитів (імуноге-
- •Дефіцит компонентів комплементу
- •2. Інтерферони
- •3. Фактори некрозу пухлин (фнп)
- •4. Інші цитокіни
- •Toll-like рецептори
- •2. Особливості механізмів набутого і вродженого імунітету.
- •3. Структура імунної системи. Основні органи і клітини.
- •4. Функції комплементу, його роль в нормі і при патології.
- •5. Основні механізми клітинної цитотоксичності.
- •6. Популяції і субпопуляції лімфоцитів. Cd-номенклатура.
- •7. Макрофаги, їх роль у специфічному і неспецифічному імунітеті.
- •8. Класи і функції імуноглобулінів. Роль імунних комплексів.
- •9. Типи цитокінів. Їх функції і біологічна роль.
- •10. Молекули міжклітинної адгезії.
- •Організація імунної відповіді
- •4. Стадія формування та підтримки імунологічної пам'яті. Відбувається
- •5. Відповідь при повторному контакті з антигеном. За рахунок існуван-
- •Дисфункції імунної системи
- •1. Розлади процесів перетравлення (кілінгу):
- •2. Розлади хемотаксису, міграції і дегрануляції:
- •3. Дефекти опсонізації і поглинання:
- •1. Вісім або більше випадків отиту протягом 1 року.
- •2. Два або більше випадків синуситів протягом 1 року.
- •3. Два або більше місяців призначення антибіотиків без значного
- •4. Дві пневмонії або більше протягом 1 року.
- •5. Значне відставання дитини у рості або у масі тіла.
- •6. Рецидивні глибокі абсцеси підшкірної клітковини або абсцеси
- •7. Персистентна молочниця ротової порожнини або інших ділянок
- •8. Потреба у внутрішньовенному введенні антибіотиків для досяг-
- •9. Дві "глибокі" інфекції або більше: менінгіти, остеомієліти, целю-
- •10. Первинні імунодефіцити в родинному анамнезі.
- •Клінічні синдроми, які часто виявляються:
- •Клінічні синдроми, які виявляються у частини хворих:
- •1. Алергічні захворювання.
- •2. Автоімунні захворювання.
- •3. Онкозахворювання.
- •4. Дисбактеріози.
- •5. Хроніосепсис.
- •III. Розлади обміну речовин та інтоксикації, зумовлені:
- •1. Ураженням детоксикаційних органів і систем (печінка, нирки).
- •2. Хронічним ураженням інших органів.
- •3. Ендокринопатіями.
- •4, Втратою крові, білків.
- •1. Екологічні і виробничі чинники.
- •2. Аліментарні фактори (дефіцит вітамінів, мікроелементів, якіс-
- •3. Інфекційні хвороби:
- •II. Зумовлені соціальними факторами:
- •1. Спосіб життя і шкідливі звички (куріння, алкоголь, урбанізація,
- •2. Надмірний рівень сумарного стресового навантаження.
- •3. Ятрогенії:
- •Імунопатологічні синдроми
- •1. Синдром швидкої втоми [втомливості] — екологічний імуноде-
- •2. Синдром хронічної втоми - стан з глибшими імунологічними
- •Оцінка імунного статусу людини
- •3. На сьогодні у клініках та імунологічних лабораторіях світу викорис-
- •1. Забираючи кров для імунологічного обстеження, необхідно макси-
- •2. Показники імунограми найкраще порівнювати з індивідуальною нор-
- •3. Комплексний аналіз імунограми більш інформативний, ніж характе-
- •4. Якщо показники індивідуальної норми не відомі, особливо необхід-
- •5. Реальну інформацію в імунограмі несуть лише значні зсуви показни-
- •6. Висновки можна робити лише після порівняння імунологічних і
- •Період реконвалесценції:
- •Трансплантаційна імунологія. Імуногенетика
- •1990 Р. Більше 18 тис. Американців потребували тансплантації органів
- •2. Dn і do локуси розміщені між dp і dq ділянками. Dn і do
- •//|Pp|dq |drhc2|BdC4Af210hAlC4b| 21-онвн tnFojTnFpHв[ с | а
- •1. Якщо лімфоцити донора і реципієнта змішати у культурі клітин, то в
- •2. Проте mlr зазвичай проводиться у вигляді односпрямованого тесту,
- •1. Протягом певного часу забирають кілька зразків сироватки кро-
- •2. Якщо хоча б в одному випадку виявляється лізис донорських
- •2. Гостре або пришвидшене відторгнення. Реакція опосередковується
- •3. Лабораторні: лейкоцитоз із еозинофілією і збільшенням шое, пока-
- •4, Імунологічні: важливими критеріями кризу є зростання співвідношен-
- •Генетика імунної відповіді
- •1. Пептиди, які зв'язуються з ніа-і класу, містять 8-10 амінокислот,
- •2. Молекули ніа-і класу синтезуються в цитозолі клітини, де зали-
- •9 Алельних варіантів. При цьому виявилося, що лише деякі з них пов'я-
- •50 Млн хворих на віл/снід, більшість із них, очевидно, помре протя-
- •3. Автоімунні ураження:
- •1) Пряма цитопатична дія вірусу. Вона підтверджується тим, що три-
- •2) Пригнічення продукції іл-2 — основного фактора росту і актива-
- •3) Поверхневий глікопротеїд віЛу др120, одночасно зв'язуючись з
- •4) Вірусні антигени та імунні комплекси активують так званий пе-
- •5) Можливе також ураження вірусом клітин-попередників т-лімфо-
- •6) Віруси цитомегалії та мікобактерії туберкульозу, які часто акти-
- •20 І більше разів рідше, ніж у віці 60-69 років. Очевидно, імунна систе-
- •Вакцини. Імунопрофілактика
- •1 Рік після трансплантації кісткового мозку можна застосувати вбиті
- •Хірургічна імунологія
- •Медіатори септичної запальної відповіді та їх антагоністи
- •2. Етіотропне лікування при сепсисі відіграє важливу, але не вирі-
- •3. Патогенетична терапія полягає у профілактиці і лікуванні син-
- •8 Год вводять біфідумбактерин, який пришвидшує формування біфідо-
- •70 % Випадків втрата яйцеклітини відбувається до імплантації [преім-
- •4. Потужним фактором імунологічного захисту плода є децидуальна
- •5. Після дозрівання трофобласта він сам починає продукувати імуносу-
- •6. Аменорея з гіпоестрогенією.
- •7. Олігоменорея.
- •8. Нерегулярний менструальний цикл з овуляцією.
- •9. Ановуляція.
- •10. Врождені аномалії.
- •11. Непрохідність маткових труб.
- •12. Злуковий процес в малому тазі.
- •13. Ендометріоз.
- •14. Набута патологія матки, цервікального каналу.
- •15. Набута патологія труб.
- •16. Набута патологія яйників.
- •17. Туберкульоз.
- •18. Імунологічні причини.
- •19. Ятрогенна причина.
- •20. Системні захворювання.
- •21. Причина не встановлена (немає лапароскопії).
- •22. Від'ємний посткоїтальний тест.
- •23. Відсутність видимої причини безпліддя.
- •1) Вторинний імунодефіцит;
- •2) Антигаметний (антиоваріальний) імунний конфлікт;
- •3} Антигаметний (антиспермальний) імунний конфлікт;
- •4) Високий рівень гістосумісності між подружжям.
- •1. Прискіпливо зібраний анамнез (див. Вище).
- •2. Огляд пацієнтки. Клінічна оцінка фертильності жінки при огляді вклю-
- •7) З метою імунореабілітації таким хворим часто призначають фізі-
- •8) З метою покращання регуляторних зв'язків між імунною та ен-
- •9} Для отримання достовірних результатів повторне імунологічне
- •1:32, Для сім'яної плазми — 1:64. Визначення титрів у динаміці дозволяє
- •Імунологія пухлин
- •6. Антологічні пухлини швидко розсмоктуються організмом у випадку,
- •7. Частота розвитку пухлин набагато вища у період новонародженості
- •8. Позитивні шкірні проби з пухлинними антигенами (екстракт з клі-
- •9. Зростання частоти виникнення пухлин у хворих, які отримують іму-
- •10. У пацієнтів з пригніченням функції клітинної ланки імунітету зрос-
- •1. Оцінка імунного статусу хворого. Окрім формування груп підвищено-
- •2. Виявлення специфічних антигенів пухлини. Метою таких обстежень
- •Основні ембріональні антигени
- •3) Активації імунної відповіді, оскільки як сама пухлина, так і цитоста-
- •1. Моноклонові антитіла. Основний принцип дії моноклонових анти-
- •2. Пухлиноінфільтруючі лімфоцити (til) — лімфоцити, активовані іп
- •Vitro у присутності клітин пухлини та іл-2 (їх ще іноді називають
- •3. Макрофагоактивуючі фактори, застосування яких забезпечує акти-
- •5. Перші серйозні досягнення в онкоімунології третього тисячоліття
- •Автоімунні хвороби
- •9 Разів, ревматоїдним артритом — утричі. Лише при анкілозуючому
- •10 До 15 типів автоантитіл різної специфіки.
- •Основні автоімунні процеси
- •4) Тироксин (трийодотиронін) — звичайно виступає в ролі гаптену,
- •5) Тетрайодотиронін — як правило, діє як гаптен;
- •6) Поверхневі мембранні антигени залози.
- •Класифікація системних васкулітів
- •2.3. Вторинні, асоційовані з імунними комплексами:
- •3. Системні васкуліти з переважним пошкодженням середніх та малих
- •3.1. Первинні, асоційованні з антитілонейтрофільно-цитоплазматич-
- •3.2. Первинні, зумовлені антиендотеліальними клітинно-фіксовани-
- •3.3. Первинні імунокомплекснозалежні:
- •3.4. Вторинні, антитілозалежні:
- •3.5. Вторинні, асоційованні з імунними комплексами:
- •4. Системні васкуліти з переважаючими пошкодженнями дрібних су-
- •4.1. Первинні, асоційованні з клітинами до базальних мембран:
- •4.2. Первинні, асоційовані з антинейтрофільноцитоплазматичними
- •4.3. Первинні, асоційовані з імунними комплексами:
- •2 (Мелоксикам), які меншою мірою подразнюють слизові оболонки.
- •5. Велика кількість хвороб і багато клінічних симптомів у одного
- •1. Тривалість симптомів хвороби.
- •2. Зв'язок симптомів з подорожами, контактом з токсичними речо-
- •3. Локальний чи генералізований характер симптомів.
- •4. Зв'язок генералізації симптомів зі зниженням маси тіла, загаль-
- •5. Детальний терапевтичний анамнез хворого за органами і системами.
- •6. Спадковий анамнез.
- •7. Особливості способу життя.
- •8. Лікувальні заходи в анамнезі (променева терапія, гемодіаліз).
- •9. Недоношеність.
- •60 %, А, окрім того, еозинофілією зазвичай супроводжується серпоподіб-
- •138,0 Г/л, при цьому 93 % з них — еозинофіли. Перебіг злоякісний,
- •Алергічні хвороби
- •Vitro. Але, як і в інших галузях медицини, лабораторні методи не мо-
- •IgG) або підвищення активності т-лімфоцитів-супресорів, що веде до
- •10"6), Поступово збільшуючи дозу до появи слабопозитивної реакції.
- •10 Таблеток на добу або по 1 таблетці за 15-30 хв до контакту з потен-
- •Псевдоалерпя і параалергія
- •X. Найважливішим і найпоширенішим є гістаміновий варіант псев-
- •2. Розлади активації системи комплементу. При вродженій чи набу-
- •3. Розлади метаболізму арахідонової кислоти. Відомо, що продукти пе-
- •Клінічні форми алергічних хвороб
- •2 % Розчину допаміну; якщо його немає, можна застосувати 1 %
- •Клінічні симптоми бронхіальної астми різної тяжкості до початку лікування
- •2,4 Г/добу дає змогу тривалий час контролювати симптоми бронхіаль-
- •10 Мг на добу. Його вплив, очевидно, пов'язаний з блокуванням лейко-
- •4. Клініко-дієтологічні методи
- •Спектр алергенів при харчовій сенсибілізації у дітей (за а. Потьомкіною, 1990)
- •Спектр алергенів при харчовій сенсибілізації у дорослих
- •Найважливіші лібератори гістаміну (за в. Казьмірчук, 1996)
- •1 Капсулі (20 мг) 3-4 рази на добу.
- •9. Вплив ліків на екологію мікроорганізмів:
- •10. Вплив медикаментів на основні обмінні процеси в організмі.
- •11. Побічні реакції та ускладнення:
- •12. Побічні реакції і ускладнення змішаного генезу:
- •13. Побічний вплив ліків, обумовлений факторами зовнішнього сере-
- •Життєвої сенсибілізації".
- •Імунотерапія
- •2) Антилімфоцитарна сироватка і глобулін;
- •3) Моноклонові антитіла;
- •4) Високоселективні цитостатики (циклоспорин а, такролімус, гус-
- •II. Глюкокортикоїди.
- •III. "Малі" імунодепресанти:
- •1} Похідні 4-амінохінліни (делагіл, плаквеніл);
- •2) Пеніциламін і препарати золота;
- •3) Гепарини та інгібітори ферментів;
- •4) Колхіцин;
- •5) Нестероїдні протизапальні засоби (у великих дозах).
- •IV. Немедикаментозні методи імуносупресивного впливу:
- •1) Хірургічне втручання (спленектомія, синовектомія);
- •2) Іонізуюче опромінення (тотальне, локальне, екстракорпоральне)
- •3) Методи, що зумовлюють розвиток цитопенії (дренаж грудного про-
- •Імуностимулятори
- •1) Вакцини (живі, вбиті, рекомбінантні);
- •2) Анатоксини.
- •II. Пасивні:
- •1) Сироватки;
- •2) Імуноглобуліни;
- •3) Моноклонові антитіла..
- •II. З переважним впливом на гуморальну ланку: препарати кістково-
- •III. З переважним впливом на синтез інтерферону: нуклеїнові кисло-
- •IV. Препарати з комплексним впливом на імунну систему: рекомбі-
- •(В. Кресюн, 1993)
- •1000 Мг, 2000-1500-1000 мг тощо). Дози 2500 і 3000 мг на добу застосову-
- •Гусперимус.
- •0,5 Г тричі на добу (або у свічках чи клізмах) протягом 8-16 тижнів.
- •8 Років. Збільшення доз анти-сд20 мкат до максимальних забезпечи-
- •IgG, знайшов практичне.
- •Шуностимулятори
- •Зен, тимозин альфа (тимальфазии).
- •1. Інтерферони
- •2. Колонієстимулювальні фактори
- •3. Інтерлейкіни
- •4. Фактор некрозу пухлин (фнп)
- •5. Нейроцитокіни
- •6. Лейкоцитарні екстракти
- •Irs 19 (ipc 19) — новий імуностамулятор, який містить глюкопроте-
- •Ipc 19 застосовують при гострих, хронічних і рецидивних інфекці-
- •1 Інгаляції протягом ще 2-4 тижнів. З профілактичною метою засіб мо-
- •2 Доби після одноразового прийому (1-1,5 мг/кг) збільшує синтез ендо-
- •1870 P.). На сьогодні у світі застосовується близько 300 препаратів, які
- •1. Антибіотики
але
змінюючи структуру під впливом протеаз,
може ставати ав-
тоанти
геном ;
Імунну
відповідь на власні антигени у цьому
випадку не можна по-
яснити
лише "нормальним" синтезом антитіл
на забар'єрні, звичайно
приховані
антигени щитоподібної залози. Хоча
тиреоглобулін постійно
присутній
у крові здорових людей, автоантитіла
до нього в нормі не
утворюються
ніколи.
У
крові хворих на автоімунний тиреоїдит
виявляють не лише бло-
кувальні,
але і цитотоксичні антитіла, які у
присутності комплементу
можуть
пошкоджувати клітини щитоподібної
залози. Дуже часто вини-
кають
клітинноопосередковані реакції. В
таких випадках виявляють
позитивні
шкірні реакції через добу після
внутрішньошкірного введен-
ня
екстракту щитоподібної залози: еритема,
набряк, ущільнення, мік-
рокрововиливи
у шкіру з переважанням нейтрофілів.
Лімфоцити цих
хворих
мають пряму цитотоксичну дію, виділяючи
деякі лімфокіни,
зокрема
лімфотоксин. Певну роль відіграють
також К-клітини (антиті-
лозалежна
клітинна цитотоксичність): антитіла
класу G
взаємодіють з
рецепторами
К-лімфоцитів, які зумовлюють лізис
тиреоцитів без ком-
плементу.
Комбінований
вплив цих факторів спричиняє лімфоїдну
інфільтра-
цію
органа з наступним розвитком фіброзу,
що клінічно проявляється
зниженням
функції щитоподібної залози.
Лікування
автоімунного тиреоїдиту полягає у
призначенні засобів
протизапальної
і замісної терапії:
• глюкокортикоїди
по 0,5-2 мг/кг маси (у преднізолоновому
еквіва-
ленті)
протягом 4-6 тижнів;
• тиреоїдні
гормони по 25-150 мкг L-тироксину
залежно від ступеня
пригнічення
функції щитоподібної залози.
АВТОІМУННИЙ
ГЕПАТИТ
Автоімунний
гепатит — це хронічне некротично-запальне
уражен-
ня
печінки невідомої етіології, при якому
виявляють циркулювальні
автоантитіла
і високий рівень глобулінів у сироватці
крові.
Гістологічно
процес проявляється фіброзом з наявністю
"містків" і
порушенням
архітектоніки печінки; з часом може
формуватися карти-
на
цирозу. Крім того, виділяють 2 форми,
при яких автоімунний гепа-
тит
поєднується з біліарним цирозом:
• перехресний
синдром — гістологічні прояви первинного
біліарно-
го
цирозу поєднуються із серологічною
симптоматикою автоімун-4) Тироксин (трийодотиронін) — звичайно виступає в ролі гаптену,
5) Тетрайодотиронін — як правило, діє як гаптен;
6) Поверхневі мембранні антигени залози.
ного
гепатиту (антимітохондріальні антитіла
й
антитіла
до ліпо-
протеїну
печінки);
• автоімунна
холангіопатія — одночасно виявляються
гістологічні
ознаки
автоімунного гепатиту і первинного
біліарного цирозу.
Такі
випадки, як правило, тяжче перебігають
і більш резистентні
до
стандартних методів терапії. Прогноз
погіршується також при появі
гістологічних
ознак цирозу.
Пусковим
моментом автоімунного гепатиту дуже
часто буває віру-
сна
інфекція (віруси гепатитів, Епштейна-Барр,
кору) в осіб із HLA-DR-
обумовленими
розладами синтезу комплементу і
рецепторів Т-лімфо-
цитів.
У частині випадків це може зумовити
недостатність функції Т-
супресорів.
Виявилося, що пусковим фактором може
стати тривале
лікування
інтерферонами, яке зумовлює активацію
латентного авто-
імунного
гепатиту. Процес завершується синтезом
анти ядерних і анти-
актинових
автоантитіл.
Автоімунний
гепатит часто поєднується з іншими
автоімунними
процесами,
що свідчить про генетичну схильність
до розвитку автоіму-
нних
процесів у таких пацієнтів. Найчастіше
виявляють: автоімунний
тиреоїдит,
тиреотоксикоз, виразковий коліт,
гемолітичну анемії, ідіо-
патичну
цитопенію, цукровий і нецукровий діабет,
целіакію, поліміо-
зит,
міастенію гравіс, легеневий фіброз,
перикардит, гломерулонефрит,
гіпереозинофільний
синдром, синдром Шегрена.
ХАРАКТЕРИСТИКА
АВТОАНТИТІЛ ПРИ АВТОІМУННОМУ ГЕПАТИТІ
Тип
антигенів
Характерні
автоантитіла
Нетипові
автоантитіла
І
тип (класичні)
Антиядерні,
антиактинові,
проти
гладких м'язів і
асіалоглюкопротеїнового фактора
Антимітохондріальні,
анти-
нейтрофільні,
протипечінкового
розчинного
антигену, печінково- підшлункового
протеїну
11
тип (anti-LKM-1)
Анти-ІЛСМ*-1, Протипечінкового
цитозолю Антиядерні
Примітка:
*
— печінково-ниркові мікросоми.
Для
підтвердження діагнозу автоімунного
гепатиту використовують
як
перелічені серологічні, так і гістологічні
критерії.
Медикаментозне
лікування автоімунного гепатиту
проводиться лише
при
активності процесу (визначеній за
змінами біохімічних показни-
ків,
гістологічними параметрами). При
безсимптомному перебізі, а та-
кож
у період ремісії терапія не проводиться.
Засобами
вибору при автоімунному гепатиті є
глюкокортикоїди і
цитостатики.
Як
правило, нормалізація біохімічних
показників спостерігається
вже
через 1-3 місяці після початку лікування,
хоч іноді ремісія настає
аж
після кількох років лікування.
Існує
ряд хвороб, які за особливостями
імунопатогенезу не можна
вважати
автоімунними, але вони є своєрідним
"містком" між процесами
інфекційними,
запальними та автоімунними. Серед таких
— системні
васкуліти
і реактивні артрити. За класифікацією
ВООЗ 1995 p.,
первинні
васкуліти
вважаються системними захворюваннями
сполучної тканини.
СИСТЕМНІ
ВАСКУЛІТИ
Системні
васкуліти (СВ) — гетерогенна група
хвороб головною озна-
кою
яких є запалення судин, що призводить
до ішемічних змін відпо-
відних
органів та тканин, причому клінічні
прояви СВ залежать від
типу,
розміру і локалізації уражених судин,
тяжкості супутніх запаль-
них
порушень.
Васкуліти
можуть виникати без базової патології
(первинні
СВ)
або
асоціюватись
з різними соматичними хворобами
[вторинні
СВ).
Вас-
куліти
рідко бувають локальними,
пошкоджуючи
лише один орган, але
частіше
зустрічаються генералізовані,
які
викликають пошкодження
декількох
органів. Запалення судинної стінки
може викликати сегмен-
тарне
пошкодження, зумовлюючи розвиток
стенозу та оклюзії чи утво-
рення
аневризм.
Сучасна
класифікація СВ грунтується на підставі
розподілу розмі-
рів
пошкодження судин, що дозволяє також
враховувати етіологію,
провідні
механізми розвитку, морфологічні зміни,
різноманітну клініку
цих
хвороб.
Загальна
щорічна захворюваність СВ наближається
у світі до 50
випадків
на 1 млн. населення. За останні 10 років
розповсюдженість
СВ
зросла в 4-5 разів і складає 42-56 нових
випадків на 1 млн. населен-
ня
в рік. На жаль, в Україні немає національного
реєстру СВ, над чим
ретельно
необхідно працювати, бо в клініці та
при патологоанатоміч-
них
знахідках число таких випадків значно
росте.
Етіологія.
Перші спроби пояснити причини того чи
іншого захво-
рювання
з групи СВ були зроблені в 30-40-х роках
минулого сторіччя і
домінуюче
значення надавалось мікобактеріям,
блідій трепонемі, стре-
птококу,
неінфекційним факторам (артеріальній
гіпертонії, медикамен-
тозній
алергії). Етіологія більшості первинних
СВ до цього часу зали-
шається
невідомою, але вважається, що багато
факторів зовнішнього
середовища
можуть ініціювати розвиток запалення
судин різного роз-
міру.
Для різних видів СВ встановлено провідний
вплив певних чинни-
ків,
але головне місце належить різноманітним
інфекційним збудни-
кам:
в першу чергу — вірусним (віруси
гепатитів, цитомегаловірус,
вірус
Епштейн-Барр, простого герпесу,
респіраторного синцитію, пар-
вовірус
В19, ВІЛ, пікорнавірус). Так, у більшості
хворих на вузликовий
поліартеріїт
виявляють серологічні і клінічні ознаки
інфекції, обумов-
леної
вірусом гепатиту В (40-90 % випадків). Є
вагомі докази того, що
вірус
гепатиту С відіграє важливу роль у
розвитку кріоглобулінемічно-
го
васкуліту — есенціальної змішаної
кріоглобулінемії. Обговорюється
етіологічне
значення в розвитку СВ інших вірусів.
ВІЛ-індуковані
васкуліти не є надто поширеними.
Причинами вас- .
куліту
у ВЇЛ-інфікованих хворих можуть бути,
крім ВІЛ, також опорту-
ністичні
інфекції (цитомегаловірус, інші
герпетичні віруси, паразити).
Розрізняють
чисто цитомегаловірусні васкуліти у
хворих з імуносупре-
сією
(трансплантація органів, лікування
цитостатиками, променева те-
рапія),
які проявляються ушкодженнями
шлунково-кишкового тракту,
шкіри,
центральної нервової системи.
Лейкокластичний
васкуліт часто розвивається в результаті
стреп-
тококової,
стафілококової, єрсиніозної, тубекульозної,
хламідійної, са-
льмонельозної
інфекцій, а також при бруцельозі,
клебсієльозі, кампі-
лобактеріозі,
бореліозі, мікоплазмозі, грибкових
інфекціях. При деяких
з
цих інфекцій активно проявляє себе,
вузликова еритема. У хворих на
гранулематоз
Вегенера розвитку захворювання або
його загостренню
передує
бактерійна інфекція верхніх дихальних
шляхів, особливо ви-
кликана
золотистим стафілококом.
Обговорюється
роль інфекції в розвитку гігантоклітинного
артерії-
ту
та хвороби Такаясу. Наприклад, у хворих
на гігантоклітинний арте-
ріїт,
значно частіше, ніж в нормі, виявляється
реплікація вірусів пара-
грипу,
Епштейна-Барр респіраторно-синцитіального,
герпесів). Не ви-
ключається
участь туберкульозної інфекції при
розвитку неспецифічного
аортоартеріїту.
Пряма дія туберкульозної інфекції на
стінку судини
майже
виключається, але пошкодження медії,
інтими може бути нас-
лідком
неспецифічної реакції на антигени
палички Коха. У хворих на
хворобу
Такаясу виявлені високі титри сироваткових
антитіл до білка
теплового
шоку, який міститься в мікобактеріях
туберкульозу. Можли-
во,
цей антиген має перехресну активність
і відіграє певну роль у роз-
витку
запального процесу в артеріальній
стінці.
Частою
формою васкулітів, пов'язаних з
інфекціями, є васкуліт дрі-
бних
судин шкіри (лейкоцитокластичний
шкірний васкуліт), включаючи
геморагічний
васкуліт. Його розвиток супроводжується
різноманітними
бактерійними
(частіше грампозитивними мікроорганізмами),
вірусними,
інфекціями,
паразитарними збудниками (аскаридоз,
стронгілоїдоз та
філяріатоз),
вірусами. Все ж необхідно вказати, що
при всій різноманіт-
ності
клінічних проявів, СВ при інфекційних
захворюваннях розвива-
ється
не часто. Ймовірно, що вирішальну роль
в індукції СВ відіграють
такі
фактори, як імунологічна відповідь
організму, тропність інфекцій-
ного
агента до певних тканин, гемодинамічні
особливості органа.
Важливою
причиною васкуліту дрібних судин є
гіперчутливість до
різноманітних
лікарських препаратів (сульфаніламіди,
антибіотики,
антитуберкульозні,
антивірусні засоби, нітрофурани,
аналгетики тощо).
Вважають,
що медикаментозна гіперчутливість
може індукувати не тіль-
ки
доброякісний шкірний, але і системний
некротизуючий васкуліт,
який
є проявом вузликового та мікроскопічного
поліартеріїту. Інколи
СВ
розвивається після вакцинації. Найчастіше
викликають вакциналь-
ну
хворобу з проявами СВ вакцини проти
кашлюку, правця, кору, по-
ліомієліту,
дифтерії тощо. Може виникнути уртикарний
васкуліт при
проведенні
специфічної імунотерапії.
До
потенційних тригерних факторів відносять
такі токсини, як солі
ртуті,
свинцю, наркотичні речовини, оксид
вуглецю, силікатний порох
тощо.
Гіперчутливість до компонентів тютюну
також може бути причи-
ною
облітеруючого тромбангіїту. Провокаційним
фактором розвитку СВ
є
дія холоду, який посилює клінічні
прояви у 40 % всіх хворих на СВ.
Вторинні
шфекційні, медикаментозні СВ, хвороба
Бюргера, Такаясу, спо-
лучнотканинні
СВ тощо). Хронічні переохолодження,
гостра холодова тра-
вма
можуть провокувати розвиток
кріоглобулінемічного васкуліту.
Все
частіше обговорюється значення
генетичної схильності при
деяких
формах СВ (гранулематоз Вегенера,
мікроскопічний поліарте-
ріїт,
хвороба Бехчета і особливо хвороба
Такаясу). Отримані дані про
помірно
збільшену частоту носійства деяких
антигенів І і II класів голо-
вного
комплексу гістосумісності в хворих на
СВ. Виявлені й інші гене-
тичні
особливості у хворих на СВ: поліморфізм
генів, які кодують син-
тез
антинейтрофільно-цитоплазматичних
антигенів та їх фізіологічних
інігібіторів
(aj-антитрипсин).
Важливі
докази імуногенетичної схильності
отримані в хворих на
гігантоклітинний
скроневий артеріїт і ревматоїдний
артрит, які асоцію-
ються
з антигеном HIA-DR4.
Встановлено
генетичну схильність до роз-
витку
неспецифічного аортоартеріїту (хвороби
Такаясу), що підтверджу-
ється
виявленням його в сім'ях хворих і в
однояйцевих близнюків. Вияв-
лений
зв'язок хвороби Такаясу з HLA-A10,
В5, Bw52,
Dwl2,
DR2,
DQwl.
Наявність
HLA-Bw52
у
цих хворих (в японській популяції) часто
супро-
воджуються
ураженням аортального клапана і лівого
шлуночка серця.
Імунопатогенез.
Згідно зі сучасними уявленнями, в
розвитку СВ
одночасно
беруть участь декілька (імунозалежних
та неімунозалежних)
патологічних
процесів. Можна умовно виділили основні
патогенетичні
механізми,
які можуть визначити клінічні та
діагностичні особливості
тої
чи іншої форми СВ.
Провідними
імунопатологічними процесами при СВ
є:
— імунокомплексні;
— асоційовані
з нейтрофільно-цитоплазматичними і
органоспеци-
фічними
антитілами;
— лімфоцитарно-макрофагальні
механізми.
Значне
місце в розвитку СВ належить імунним
комплексам. Ще в
50-х
роках C.G.
Cochrane
та
F.
Dixon
показали
їх роль у виникненні СВ
на
моделі у тварин при їх імунізації
чужорідним білком, що супроводжу-
ється
виробленням специфічних антитіл,
утворенням високих рівнів ЦІК
та
гіпокомплементемією. Найчастіше цей
механізм індукується прийо-
мом
медикаментів, інфекціями та системними
захворюваннями сполуч-
ної
тканини. Так, у хворих на ревматоїдний
васкуліт виявляється висо-
кий
рівень ревматоїдного фактора, присутність
кріоглобулінів з вмістом
ревматоїдного
фактора, зниження активності комплементу.
У хворих на
геморагічний
васкуліт у склад ЦІК входить ІдА, який
є комплемент-акти-
вуючим
фактором альтернативного шляху. У таких
хворих в основному
підвищується
синтез IgAj-ізомеру,
який формує макромолекулярні агре-
гати
з сироватковим фібронектином. ІдА^полімери
та IgAj-вмісні
ЦІК
характеризуються
тривалою циркуляцією у крові.
Часто
у хворих на імунокомплексні васкуліти
виявляють кріоглобу-
ліни.
Вони підтримують хронічне запалення
шляхом активації системи
комплементу
та моноцитів. Особливо часто кріоглобуліни
виявляються
у
хворих на системний червоний вовчак,
хворобу Шегрена. Крім того,
виділяється
окремий вид СВ, при якому пошкоджуються
дрібні суди-
ни
— есенціальна змішана кріоглобулінемія
(кріоглобулінемічний вас-
куліт).
Пошкодження ендотеліоцитів імунними
комплексами відбува-
ється
внаслідок наявності на їх мембранах
рецепторів до СЗ-компонен-
ту
комплементу та Fc-фрагментів
імуноглобулінів.
Провідне
місце в розвитку СВ належить антитіло
залежним проце-
сам.
Велику увагу зараз приділяють АНЦА —
гетерогенній популяції
автоантитіл,
які реагують з різними ферментами
цитоплазми нейтро-
філів,
у першу чергу — з протеазою-3 і
мієлопероксидазою, рідше з
лактоферином,
катепсином G,
Особливо
важливе значення надають
антитілам,
які реагують з протеазою-3 і
мієлопероксидазою. Ці антиті-
ла
є не тільки серологічними маркерами
гранулематозу Вегенера, син-
дрому
Чарджа-Стросса, мікроскопічного
поліангіїту, але і відіграють
важливу
роль у патогенезі СВ:
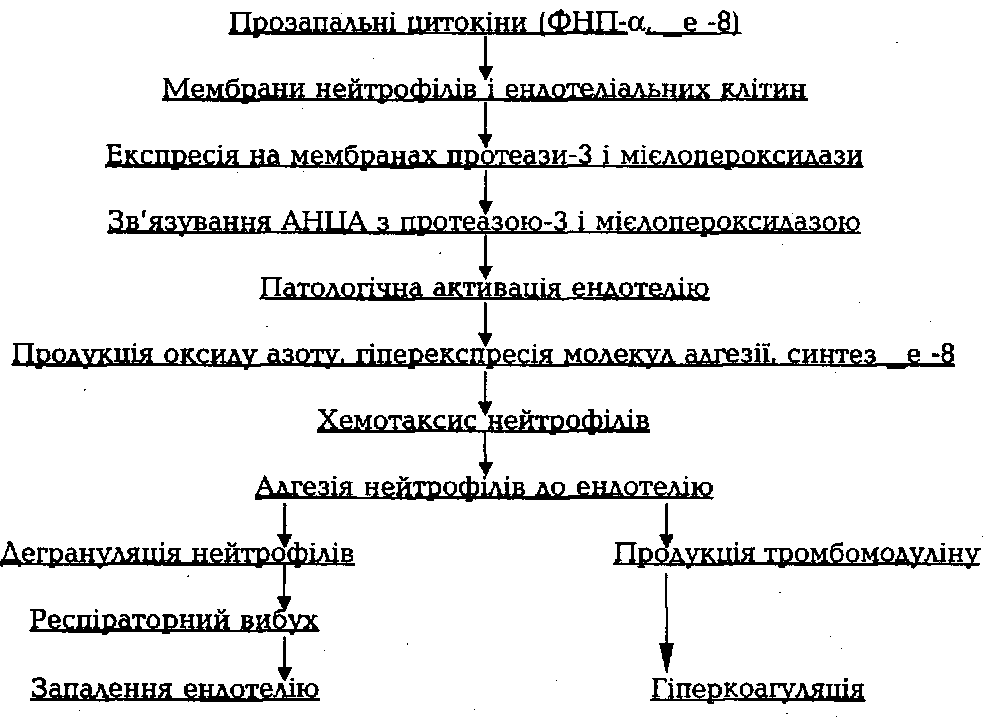
Інший
механізм дії АНЦА характеризується їх
впливом на ендоте-
ліоцити.
Під впливом прозалальних цитокінів
відбувається експресія
протеази-3
на мембрані ендотеліоцитів, з якою
зв'язується АНЦА та
індукують
антитілозалежну клітинну цитотоксичність
з експресією Е-
селектину
та судинної молекули адгезії-1 (VCAM-1),
Це
забезпечує при-
липання
лейкоцитів, лімфоцитів і їх перехід
через стінку судини в тка-
нини.
Встановлена перехресна реактивність
АНЦА з мембранними лей-
коцитарними
та ендотеліальними глюкопротеїдами,
за рахунок чого вони
можуть
активно підтримувати хронічне запалення.
Поряд
з АНЦА, важливе значення в патогенезі
СВ надають антиен-
дотеліальним
антитілам (АЕА), які можуть пошкоджувати
клітини шля-
хом
комплементзалежного цитолізу або
антитілозалежної цитотоксич-
ності
і модулювати функціональну активність
ендотеліоцитів. Встанов-
лено,
що АЕА розпізнають цитокініндуковані
антигени на мембрані
ендотелію.
Лізис клітин ендотелію індукується
γ-інтерфероном,
або ІЛ-
1
і ФНП-ОЕ.
АНЦА теж часто проявляють активність
АЕА.
Обговорюється
роль антитіл до фосфоліпідів, які можуть
бути мар-
керами
ендотеліального пошкодження і брати
участь у розвитку тром-
ботичних
ускладнень у хворих СВ. Є дані про
взаємозв'язок між АЕА