
- •Перелік умовних скорочень
- •Структура і функціонування імунної системи
- •Природні бар'єри
- •4) Розселення т- і в-лімфоцитів на периферії та індукція толерант-
- •5) Антигенозалежний етап диференціювання лімфоцитів (імуноге-
- •Дефіцит компонентів комплементу
- •2. Інтерферони
- •3. Фактори некрозу пухлин (фнп)
- •4. Інші цитокіни
- •Toll-like рецептори
- •2. Особливості механізмів набутого і вродженого імунітету.
- •3. Структура імунної системи. Основні органи і клітини.
- •4. Функції комплементу, його роль в нормі і при патології.
- •5. Основні механізми клітинної цитотоксичності.
- •6. Популяції і субпопуляції лімфоцитів. Cd-номенклатура.
- •7. Макрофаги, їх роль у специфічному і неспецифічному імунітеті.
- •8. Класи і функції імуноглобулінів. Роль імунних комплексів.
- •9. Типи цитокінів. Їх функції і біологічна роль.
- •10. Молекули міжклітинної адгезії.
- •Організація імунної відповіді
- •4. Стадія формування та підтримки імунологічної пам'яті. Відбувається
- •5. Відповідь при повторному контакті з антигеном. За рахунок існуван-
- •Дисфункції імунної системи
- •1. Розлади процесів перетравлення (кілінгу):
- •2. Розлади хемотаксису, міграції і дегрануляції:
- •3. Дефекти опсонізації і поглинання:
- •1. Вісім або більше випадків отиту протягом 1 року.
- •2. Два або більше випадків синуситів протягом 1 року.
- •3. Два або більше місяців призначення антибіотиків без значного
- •4. Дві пневмонії або більше протягом 1 року.
- •5. Значне відставання дитини у рості або у масі тіла.
- •6. Рецидивні глибокі абсцеси підшкірної клітковини або абсцеси
- •7. Персистентна молочниця ротової порожнини або інших ділянок
- •8. Потреба у внутрішньовенному введенні антибіотиків для досяг-
- •9. Дві "глибокі" інфекції або більше: менінгіти, остеомієліти, целю-
- •10. Первинні імунодефіцити в родинному анамнезі.
- •Клінічні синдроми, які часто виявляються:
- •Клінічні синдроми, які виявляються у частини хворих:
- •1. Алергічні захворювання.
- •2. Автоімунні захворювання.
- •3. Онкозахворювання.
- •4. Дисбактеріози.
- •5. Хроніосепсис.
- •III. Розлади обміну речовин та інтоксикації, зумовлені:
- •1. Ураженням детоксикаційних органів і систем (печінка, нирки).
- •2. Хронічним ураженням інших органів.
- •3. Ендокринопатіями.
- •4, Втратою крові, білків.
- •1. Екологічні і виробничі чинники.
- •2. Аліментарні фактори (дефіцит вітамінів, мікроелементів, якіс-
- •3. Інфекційні хвороби:
- •II. Зумовлені соціальними факторами:
- •1. Спосіб життя і шкідливі звички (куріння, алкоголь, урбанізація,
- •2. Надмірний рівень сумарного стресового навантаження.
- •3. Ятрогенії:
- •Імунопатологічні синдроми
- •1. Синдром швидкої втоми [втомливості] — екологічний імуноде-
- •2. Синдром хронічної втоми - стан з глибшими імунологічними
- •Оцінка імунного статусу людини
- •3. На сьогодні у клініках та імунологічних лабораторіях світу викорис-
- •1. Забираючи кров для імунологічного обстеження, необхідно макси-
- •2. Показники імунограми найкраще порівнювати з індивідуальною нор-
- •3. Комплексний аналіз імунограми більш інформативний, ніж характе-
- •4. Якщо показники індивідуальної норми не відомі, особливо необхід-
- •5. Реальну інформацію в імунограмі несуть лише значні зсуви показни-
- •6. Висновки можна робити лише після порівняння імунологічних і
- •Період реконвалесценції:
- •Трансплантаційна імунологія. Імуногенетика
- •1990 Р. Більше 18 тис. Американців потребували тансплантації органів
- •2. Dn і do локуси розміщені між dp і dq ділянками. Dn і do
- •//|Pp|dq |drhc2|BdC4Af210hAlC4b| 21-онвн tnFojTnFpHв[ с | а
- •1. Якщо лімфоцити донора і реципієнта змішати у культурі клітин, то в
- •2. Проте mlr зазвичай проводиться у вигляді односпрямованого тесту,
- •1. Протягом певного часу забирають кілька зразків сироватки кро-
- •2. Якщо хоча б в одному випадку виявляється лізис донорських
- •2. Гостре або пришвидшене відторгнення. Реакція опосередковується
- •3. Лабораторні: лейкоцитоз із еозинофілією і збільшенням шое, пока-
- •4, Імунологічні: важливими критеріями кризу є зростання співвідношен-
- •Генетика імунної відповіді
- •1. Пептиди, які зв'язуються з ніа-і класу, містять 8-10 амінокислот,
- •2. Молекули ніа-і класу синтезуються в цитозолі клітини, де зали-
- •9 Алельних варіантів. При цьому виявилося, що лише деякі з них пов'я-
- •50 Млн хворих на віл/снід, більшість із них, очевидно, помре протя-
- •3. Автоімунні ураження:
- •1) Пряма цитопатична дія вірусу. Вона підтверджується тим, що три-
- •2) Пригнічення продукції іл-2 — основного фактора росту і актива-
- •3) Поверхневий глікопротеїд віЛу др120, одночасно зв'язуючись з
- •4) Вірусні антигени та імунні комплекси активують так званий пе-
- •5) Можливе також ураження вірусом клітин-попередників т-лімфо-
- •6) Віруси цитомегалії та мікобактерії туберкульозу, які часто акти-
- •20 І більше разів рідше, ніж у віці 60-69 років. Очевидно, імунна систе-
- •Вакцини. Імунопрофілактика
- •1 Рік після трансплантації кісткового мозку можна застосувати вбиті
- •Хірургічна імунологія
- •Медіатори септичної запальної відповіді та їх антагоністи
- •2. Етіотропне лікування при сепсисі відіграє важливу, але не вирі-
- •3. Патогенетична терапія полягає у профілактиці і лікуванні син-
- •8 Год вводять біфідумбактерин, який пришвидшує формування біфідо-
- •70 % Випадків втрата яйцеклітини відбувається до імплантації [преім-
- •4. Потужним фактором імунологічного захисту плода є децидуальна
- •5. Після дозрівання трофобласта він сам починає продукувати імуносу-
- •6. Аменорея з гіпоестрогенією.
- •7. Олігоменорея.
- •8. Нерегулярний менструальний цикл з овуляцією.
- •9. Ановуляція.
- •10. Врождені аномалії.
- •11. Непрохідність маткових труб.
- •12. Злуковий процес в малому тазі.
- •13. Ендометріоз.
- •14. Набута патологія матки, цервікального каналу.
- •15. Набута патологія труб.
- •16. Набута патологія яйників.
- •17. Туберкульоз.
- •18. Імунологічні причини.
- •19. Ятрогенна причина.
- •20. Системні захворювання.
- •21. Причина не встановлена (немає лапароскопії).
- •22. Від'ємний посткоїтальний тест.
- •23. Відсутність видимої причини безпліддя.
- •1) Вторинний імунодефіцит;
- •2) Антигаметний (антиоваріальний) імунний конфлікт;
- •3} Антигаметний (антиспермальний) імунний конфлікт;
- •4) Високий рівень гістосумісності між подружжям.
- •1. Прискіпливо зібраний анамнез (див. Вище).
- •2. Огляд пацієнтки. Клінічна оцінка фертильності жінки при огляді вклю-
- •7) З метою імунореабілітації таким хворим часто призначають фізі-
- •8) З метою покращання регуляторних зв'язків між імунною та ен-
- •9} Для отримання достовірних результатів повторне імунологічне
- •1:32, Для сім'яної плазми — 1:64. Визначення титрів у динаміці дозволяє
- •Імунологія пухлин
- •6. Антологічні пухлини швидко розсмоктуються організмом у випадку,
- •7. Частота розвитку пухлин набагато вища у період новонародженості
- •8. Позитивні шкірні проби з пухлинними антигенами (екстракт з клі-
- •9. Зростання частоти виникнення пухлин у хворих, які отримують іму-
- •10. У пацієнтів з пригніченням функції клітинної ланки імунітету зрос-
- •1. Оцінка імунного статусу хворого. Окрім формування груп підвищено-
- •2. Виявлення специфічних антигенів пухлини. Метою таких обстежень
- •Основні ембріональні антигени
- •3) Активації імунної відповіді, оскільки як сама пухлина, так і цитоста-
- •1. Моноклонові антитіла. Основний принцип дії моноклонових анти-
- •2. Пухлиноінфільтруючі лімфоцити (til) — лімфоцити, активовані іп
- •Vitro у присутності клітин пухлини та іл-2 (їх ще іноді називають
- •3. Макрофагоактивуючі фактори, застосування яких забезпечує акти-
- •5. Перші серйозні досягнення в онкоімунології третього тисячоліття
- •Автоімунні хвороби
- •9 Разів, ревматоїдним артритом — утричі. Лише при анкілозуючому
- •10 До 15 типів автоантитіл різної специфіки.
- •Основні автоімунні процеси
- •4) Тироксин (трийодотиронін) — звичайно виступає в ролі гаптену,
- •5) Тетрайодотиронін — як правило, діє як гаптен;
- •6) Поверхневі мембранні антигени залози.
- •Класифікація системних васкулітів
- •2.3. Вторинні, асоційовані з імунними комплексами:
- •3. Системні васкуліти з переважним пошкодженням середніх та малих
- •3.1. Первинні, асоційованні з антитілонейтрофільно-цитоплазматич-
- •3.2. Первинні, зумовлені антиендотеліальними клітинно-фіксовани-
- •3.3. Первинні імунокомплекснозалежні:
- •3.4. Вторинні, антитілозалежні:
- •3.5. Вторинні, асоційованні з імунними комплексами:
- •4. Системні васкуліти з переважаючими пошкодженнями дрібних су-
- •4.1. Первинні, асоційованні з клітинами до базальних мембран:
- •4.2. Первинні, асоційовані з антинейтрофільноцитоплазматичними
- •4.3. Первинні, асоційовані з імунними комплексами:
- •2 (Мелоксикам), які меншою мірою подразнюють слизові оболонки.
- •5. Велика кількість хвороб і багато клінічних симптомів у одного
- •1. Тривалість симптомів хвороби.
- •2. Зв'язок симптомів з подорожами, контактом з токсичними речо-
- •3. Локальний чи генералізований характер симптомів.
- •4. Зв'язок генералізації симптомів зі зниженням маси тіла, загаль-
- •5. Детальний терапевтичний анамнез хворого за органами і системами.
- •6. Спадковий анамнез.
- •7. Особливості способу життя.
- •8. Лікувальні заходи в анамнезі (променева терапія, гемодіаліз).
- •9. Недоношеність.
- •60 %, А, окрім того, еозинофілією зазвичай супроводжується серпоподіб-
- •138,0 Г/л, при цьому 93 % з них — еозинофіли. Перебіг злоякісний,
- •Алергічні хвороби
- •Vitro. Але, як і в інших галузях медицини, лабораторні методи не мо-
- •IgG) або підвищення активності т-лімфоцитів-супресорів, що веде до
- •10"6), Поступово збільшуючи дозу до появи слабопозитивної реакції.
- •10 Таблеток на добу або по 1 таблетці за 15-30 хв до контакту з потен-
- •Псевдоалерпя і параалергія
- •X. Найважливішим і найпоширенішим є гістаміновий варіант псев-
- •2. Розлади активації системи комплементу. При вродженій чи набу-
- •3. Розлади метаболізму арахідонової кислоти. Відомо, що продукти пе-
- •Клінічні форми алергічних хвороб
- •2 % Розчину допаміну; якщо його немає, можна застосувати 1 %
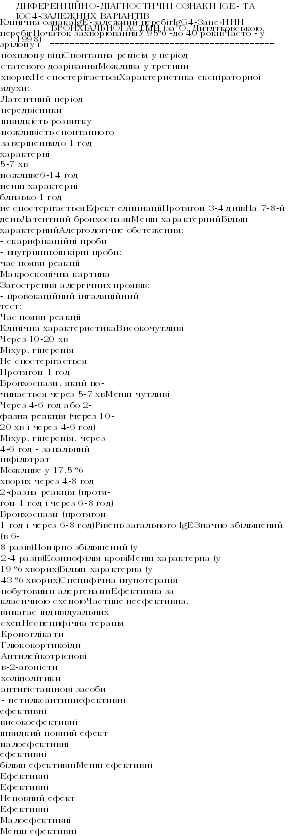
- •Клінічні симптоми бронхіальної астми різної тяжкості до початку лікування
- •2,4 Г/добу дає змогу тривалий час контролювати симптоми бронхіаль-
- •10 Мг на добу. Його вплив, очевидно, пов'язаний з блокуванням лейко-
- •4. Клініко-дієтологічні методи
- •Спектр алергенів при харчовій сенсибілізації у дітей (за а. Потьомкіною, 1990)
- •Спектр алергенів при харчовій сенсибілізації у дорослих
- •Найважливіші лібератори гістаміну (за в. Казьмірчук, 1996)
- •1 Капсулі (20 мг) 3-4 рази на добу.
- •9. Вплив ліків на екологію мікроорганізмів:
- •10. Вплив медикаментів на основні обмінні процеси в організмі.
- •11. Побічні реакції та ускладнення:
- •12. Побічні реакції і ускладнення змішаного генезу:
- •13. Побічний вплив ліків, обумовлений факторами зовнішнього сере-
- •Життєвої сенсибілізації".
- •Імунотерапія
- •2) Антилімфоцитарна сироватка і глобулін;
- •3) Моноклонові антитіла;
- •4) Високоселективні цитостатики (циклоспорин а, такролімус, гус-
- •II. Глюкокортикоїди.
- •III. "Малі" імунодепресанти:
- •1} Похідні 4-амінохінліни (делагіл, плаквеніл);
- •2) Пеніциламін і препарати золота;
- •3) Гепарини та інгібітори ферментів;
- •4) Колхіцин;
- •5) Нестероїдні протизапальні засоби (у великих дозах).
- •IV. Немедикаментозні методи імуносупресивного впливу:
- •1) Хірургічне втручання (спленектомія, синовектомія);
- •2) Іонізуюче опромінення (тотальне, локальне, екстракорпоральне)
- •3) Методи, що зумовлюють розвиток цитопенії (дренаж грудного про-
- •Імуностимулятори
- •1) Вакцини (живі, вбиті, рекомбінантні);
- •2) Анатоксини.
- •II. Пасивні:
- •1) Сироватки;
- •2) Імуноглобуліни;
- •3) Моноклонові антитіла..
- •II. З переважним впливом на гуморальну ланку: препарати кістково-
- •III. З переважним впливом на синтез інтерферону: нуклеїнові кисло-
- •IV. Препарати з комплексним впливом на імунну систему: рекомбі-
- •(В. Кресюн, 1993)
- •1000 Мг, 2000-1500-1000 мг тощо). Дози 2500 і 3000 мг на добу застосову-
- •Гусперимус.
- •0,5 Г тричі на добу (або у свічках чи клізмах) протягом 8-16 тижнів.
- •8 Років. Збільшення доз анти-сд20 мкат до максимальних забезпечи-
- •IgG, знайшов практичне.
- •Шуностимулятори
- •Зен, тимозин альфа (тимальфазии).
- •1. Інтерферони
- •2. Колонієстимулювальні фактори
- •3. Інтерлейкіни
- •4. Фактор некрозу пухлин (фнп)
- •5. Нейроцитокіни
- •6. Лейкоцитарні екстракти
- •Irs 19 (ipc 19) — новий імуностамулятор, який містить глюкопроте-
- •Ipc 19 застосовують при гострих, хронічних і рецидивних інфекці-
- •1 Інгаляції протягом ще 2-4 тижнів. З профілактичною метою засіб мо-
- •2 Доби після одноразового прийому (1-1,5 мг/кг) збільшує синтез ендо-
- •1870 P.). На сьогодні у світі застосовується близько 300 препаратів, які
- •1. Антибіотики
го
і чутливість його до бронходилятаторів
та інших медикаментів. Фор-
мується
так звана:
с)
стероїдозалежна астма.
Класифікація
бронхіальної астми
Тяжкість
перебігу:
1.
Інтермітуюча (періодична).
2.
Легка
персистуюча (постійна).
3.
Середньої тяжкості персистуюча.
4.
Тяжка
персистуюча.
Контрольованість
перебігу:
1.
Контрольований.
2.
Неконтрольований
— загострення:
— легке;
— середньої
тяжкості;
— тяжке;
— загроза
зупинки дихання.
Ускладнення:
1.
Легеневі (емфізема легень, легенева
недостатність, ателектаз, пнев-
моторакс
та ін.).
2.
Позалегеневі (дистрофія міокарда,
легеневе серце, серцева недоста-
тність
та ін.).
Персистую ча
Симптоми Інтермітуюча
легка
середньої
тяжкості
тяжка Короткотривалі
<
1 разу на
<
1 разу на
Щоденні
Постійні,
тривалі
симтоми
тиждень
день
Короткотривалі
Кілька
годин
Іноді
Порушують
Постійні,
тривалі,
загострення
— кілька
днів
порушують
активність
і
обмежують
активність
і
сон
фізичну
сон
активність
Нічні
симтоми
До
2 разів на
2-5
разів на
Частіше
1
Постійні
місяць
місяць
разу
на
тиждень
ОФВ,і
ПОШВид
>80%
>80
%
60-80
%
<60%
(щодо
норми)
Добові
коливання
<20%
20-30
%
>30%
>30%
ОФВ1
і ПОШвид
Бронхіальна
астма звичайно перебігає як алергічне
захворювання у
дорослих
протягом перших 3-5
років.
На цьому етапі за хворим пови-
нні
наглядати алерголог і пульмонолог.
Алергічний період у дітей можеКлінічні симптоми бронхіальної астми різної тяжкості до початку лікування
тривати
довше і досить часто його завершення
співпадає з періодом
статевого
формування (зміна гормонального
балансу). У цьому віці іно-
ді
спостерігається спонтанне видужання
або "переростання" астми в
неалергічну
фазу.
Патогенетичний
ланцюг бронхіальної астми розпочинається
з ан-
тигенної
сенсибілізації Т-лімфоцитів. Як правило,
"вмикаються" Т-хел-
пери
2-го типу, які стимулюють В-клітини для
утворення реагінів-ІдЕ,
рідше
— IgG4.
При
повторному контакті з антигеном
відбувається вза-
ємодія
комплексів алерген-реагін з мастоцитами
і виділення медіаторів
гіперчутливості
негайного типу. Рання фаза запального
процесу харак-
теризується
розвитком бронхоспазму і набряком
слизової оболонки
бронхів
за рахунок ексудації плазми. У пізній
фазі відбувається фаго-
цитарна
інфільтрація, яка посилює запальний
процес. За впливом на
організм
хворого можна виділити "індукційні
фактори", які сприяють
появі
гіперреактивності бронхів: екологічні
(полютанти), фармакологі-
чні,
вірусні і бактерійні агенти. Інші
фактори, "провокаційні", або "пу-
скові"
(тригерні) сприяють розвитку бронхоспазму:
повторний контакт
з
алергеном, переохолодження, емоційні
та фізичні перевантаження.
Ушкоджений
епітелій бронхів чутливий не тільки
до потенційних але-
ргенів,
але й неспецифічних чинників.
Якщо
з огляду на патогенетичні і терапевтичні
особливості в краї-
нах
Східної Європи традиційно виділяли
атопічну
та
інфєкційнозалеж-
ну
форми
перебізі, то в країнах Євросоюзу —
відповідно ІдЕ-
та
ІдС4-
залежні
варіанти астми. IgE-варіант
переважно виявляється при атопі-
чній
формі захворювання, IgG4-
—
при інфекційно-алергічній
бронхіальній
астмі.
Варто
зазначити, що як ІдЕ-, так і ІдС4-механізми
беруть участь в
усіх
варіантах перебігу, проте один з них,
як правило, домінує. Це ви-
значає
патоімунологічні та клінічні особливості
астми, диктує необхід-
ність
вибору певного методу терапії. При
інших патогенетичних фор-
мах
додатково нашаровуються розлади з боку
адренергічної регуляції,
гормонального
балансу, психіки тощо.
Визначення
провідного патоімунологічного
механізму дасть змогу
прогнозувати
ефективність елімінаційної терапії,
специфічної гіпосен-
сибілізації,
підібрати засоби для медикаментозного
впливу.
Клінічна
картина бронхіальної астми значною
мірою залежить від
типу
алергену. Своєчасна ідентифікація
екзоалергену вкрай важлива
для
ефективної елімінації, можливого
проведення специфічної гіпосе-
нсибілізації.
Ще до застосування специфічних
лабораторних і провока-
ційних
методів, значну допомогу для діагностики
може дати вияснення
клініко-анамнестичних
особливостей перебігу атопічної
бронхіальної
астми.

Яри
сенсибілізації
до побутових алергенів (переважно —
мікроклі-
щів)
характерні:
• ремісії
поза домом (елімінація) і загострення
при поверненні;
• нечітко
виражена сезонність загострень
(серпень-жовтень), по-
в'язана
з періодом розмноження кліщів;
• поєднання
алергії на домашній пил з алергією на
пір'я (у третини
пацієнтів);
• загострення
захворювання в зимовий період, пов'язане
з макси-
мальним
насиченням повітря приміщень пилом;
• часте
поєднання (у 50-60 %) з алергічним ринітом.
Для
пилкової бронхіальної астми характерні:
• переважний
розвиток на тлі алергічного
ринокон'юнктивіту;
• приєднання
астматичних проявів до ринокон'юнктивальних
сим-
птомів
у розпал сезону цвітіння. Лише у 4 %
хворих спостеріга-
ється
ізольована форма пилкової бронхіальної
астми. Як правило,
такі
варіанти перебігають дуже тяжко,
можливий розвиток стату-
сів.
Шкірні проби у таких випадках можуть
бути негативними.
Основним
діагностичним методом стає провокаційний
інгаляцій-
ний
тест;
• при
поєднанні з харчовою алергією
(псевдоалергічний компонент),
часто
втрачає сезонність перебігу і
трансформується у цілорічну
форму
захворювання;
• поєднується
з медикаментозною алергією на препарати
з рослин,
що
мають спільні алергени (наприклад, при
сенсибілізації до по-
лину,
виявляють медикаментозну алергію на
екстракти з кукуру-
дзяних
стовпчиків, настоянкам безсмертника,
календули). Дещо
рідше
трапляється перехресна сенсибілізація
до харчових проду-
ктів
рослинного походження.
При
епідермальній бронхіальній астмі:
• у
зв'язку з високою алергенною активністю
астмогенність епідер-
мальних
алергенів відзначають самі пацієнти;
• на
відміну від інших форм бронхіальної
астми, часто спостеріга-
ються
пролонговані напади ядухи — у зв'язку
з цим вислухову-
ється
дуже багата і виразна аускультативна
картина;
• іноді
поєднується з алергічним ринокон'юнктивітом;
• може
поєднуватися з полілімфаденопатією,
артралгією, субфеб-
рилітетсм;
• при
специфічному алергологічному обстеженні
виявляють артю-
соподібні
реакції на алергени.
Останнім
часом окремо виділяють епідермальний
і харчовий варіа-
нти
хвороби, які мають певні особливості
перебігу.
Для
харчової
бронхіальної астми характерні:
• часте
поєднання з шкірними проявами алергії.
У дитинстві час-
то
— есудативно-катаральний діатез;
• напади
ядухи можуть виникати на конкретний
запах їжі;
• за
перебігом і характером нападів ядухи,
аускультативної симпто-
матики,
розвитку ускладнень, частотою астматичних
статусів на-
ближається
до ендогенної форми бронхіальної
астми;
• на
відміну від інших атоігічних форм,
характерна астматична трі-
ада
(поліпоз носа, непереносність нестероїдних
протизапальних
засобів
і, передусім, саліцилатів);
*
частий перебіг на тлі хронічних
захворювань органів травлення.
їх
лікування, компенсація ферментної
недостатності та ефектив-
на
дегельмінтизація значно полегшує
перебіг бронхіальної астми;
• тромбоцитопенія
і лейкопенія.
Проблемі
лікування бронхіальної астми присвячена
обширна літе-
ратура,
тому нижче розглянуто лише алергологічні
та імунологічні осо-
бливості
терапії.
Етіотропна
терапія
бронхіальної астми має значення
переважно в
перші
3-4 роки захворювання. Усунути контакт
з потенційним алерге-
ном
легше при сенсибілізації до побутових
(шерсть домашніх тварин,
дафнії,
таргани, харчові алергени) чи професійних
факторів, що дося-
гається
раціональним працевлаштуванням або
організацією побуту.
Тяжче
здійснити це у випадку сенсибілізації
до кліщових чи грибкових
алергенів
домашнього пилу. Ще тяжче уникнути
контакту з пилковими
алергенами.
Необхідно зазначити, що гіперреактивність
бронхів суттє-
во
знижується лише через 2-6 місяців після
елімінації побутових АлГ.
Хворим
на аспіринову астму забороняється
приймати нестероїдні
протизапальні
препарати в амбулаторних умовах, а
також продукти і
фітотерапевтичні
засоби, які містять саліцилати (кора
верби, цитрусо-
ві,
чорна смородина). Досить поширеним за
кордоном методом є гіпо-
сенсибілізація
до аспірину. З цією метою пацієнти
приймають ацетил-
саліцилову
кислоту у стаціонарних умовах, через
день, починаючи з
низьких
доз (2-20 мг). За іншою методикою, початкова
доза визнача-
ється
як така, що знижує об'єм форсованого
видиху за першу секунду
на
20 %. Лікування, як правило, розпочинають
у рефрактерний період,
який
триває 72 год після нападу аспіринової
ядухи. У багатьох хворих
гіпосенсибілізація
до ацетисаліцилової кислоти (а також
тартразину)
зумовлює
стійкий клінічний ефект. Проте у частини
пацієнтів, особли-
во
при тяжкому перебізі астми і гормональній
залежності, не вдається
покращити
перебіг захворювання чи зменшити дозу
глюкокортикоїдів.
Крім
того, гіпосенсибілізація у таких хворих
пов'язана із значним ри-
зиком,
а тому не рекомендується. Оскільки
непереносність аспірину
має
псевдоалергічний генез, то гіпосенсибілізація
спрямована не на
специфічні
імунологічні механізми, а на індукцію
синтезу печінкою
ферментів
метаболічного циклу арахідонової
кислоти.
Специфічна
гіпосенсибілізація (за західною
термінологією — спе-
цифічна
імунотерапія астми) як етіотропний
метод лікування забезпе-
чує
нечутливість до дії алергенів, які
зумовлюють патологічні прояви,
після
лікувального введення цих алергенів.
Кращий ефект від гіпосен-
сибілізації
спостерігається у хворих на пилкову і
пилову астму, при
короткому
анамнезі захворювання, негормонозалежному
перебізі, у
дітей
і при проведенні повторних курсів.
Механізм дії імунотерапії
пов'язують
з виробленням блокувальних антитіл
класу IgG,
стимуляці-
єю
синтезу IgG
та
ІдА у бронхіальному секреті, зростанням
активності
Т-супресорів,
стабілізацією мембран мастоцитів.
Гіпосенсибілізація
проводиться
лише при наявності умов для чіткого
відбору хворих і
оцінки
ефективності лікування (PACT,
інгаляційні
проби). Надзвичай-
но
важливою умовою є виключення механізмів
псевдоалергії у розвит-
ку
бронхоспазму. Таким хворим специфічна
гіпосенсибілізація проти-
показана,
оскільки не тільки не дає клінічного
ефекту, але і може зумо-
вити
розвиток серйозних ускладнень, тому
що тяжкість клінічних
проявів
псевдоалергії зростає зі збільшенням
дози речовини, яка її зу-
мовлює.
Менш ефективна специфічна гіпосенсибілізація
при IgG4-3a-
лежній
формі бронхіальної астми.
Метод
екстракорпоральної імуносорбції
(видалення специфічних
антитіл
при перфузії крові через колонки із
сорбентом і зафіксованим
до
нього алергеном) практично не впливає
на клінічний перебіг захво-
рювання
у більшості пацієнтів і в клінічній
практиці не застосовується.
Деякі
особливості мають і ті засоби
патогенетичної
медикаменто-
зної
терапії бронхіальної астми, вплив яких
спрямований на початкові,
імунологічну
і патохімічну, фази патологічного
процесу.
Досить
широко в клінічній практиці застосовують
так звані нестеро-
їдні
стабілізатори клітинних мембран
(кетотіфен, кромоглікат і недокро-
міл
натрію), які інколи неправильно відносять
до класу нестероїдних
протизапальних
засобів. На відміну від блокаторів
гістамінових рецепто-
рів
1-го типу, ці препарати не здатні швидко
змінювати реактивність
бронхів.
Антигістамінові засоби діють на
рецептори, розміщені на орга-
нах-мішенях,
а тому "вимикають" дію гістаміну
швидко, незалежно від
його
концентрації у крові і тканинах.
Стабілізатори, на відміну від них,
не
блокують дію гістаміну, а попереджують
його виділення, тобто "пра-
цюють"
на попередньому етапі. При цьому весь
звільнений гістамін про-
довжує
діяти до того часу, поки не інактивується
ферментами. Ці препа-
рати
застосовують лише для профілактики
нападів ядухи.
Кетотіфен
(задітен)
— один із засобів, який стабілізує
мастоцити і
попереджує
виділення медіаторів (гістамін,
лейкотрієни, тромбоцитоак-
тивуючий
фактор). При тривалому прийманні змінює
конфігурацію Hj-
рецепторів,
а тому ніби проявляє Н1-блокувальний
вплив. Експеримента-
льні
дані свідчать про здатність задітену
знижувати інтенсивність фіксації
алергічних
комплексів до мастоцитів. Задітен
застосовують як базовий
препарат,
особливо у дітей, підлітків і при
нововиниклій астмі у дорослих.
Тривале
лікування задітеном дає можливість
зменшити дозу бронхоліти-
ків,
а при стероїдозалежній формі захворювання
— гормонів. Препарат
приймають
по 1 мг двічі на добу або у пролонгованій
формі по 2 мг один
раз
на добу. У дітей, у зв'язку з високим
кліренсом, застосовують таку ж
дозу
препарату, починаючи з 3-річного віку.
Максимальний ефект про-
являється
через 4-8 тижнів безперервного приймання.
У зв'язку з по-
явою
високоефективних інгаляційних
кортикостероїдів, кетотіфен у до-
рослих
як засіб базисної терапії застосовують
вкрай рідко.
Кромоглікаш
натрію (кромолін,
інтал, ломудал, ломузол) попере-
джує
розвиток ранньої астматичної реакції
і зменшує вираження піз-
ньої
реакції. Він гальмує звільнення
медіаторів з мастоцитів і актива-
цію
гранулоцитів (нейтрофілів і еозинофілів).
Виявлено також здат-
ність
кромоглікату блокувати рефлекторний
бронхоспазм у відповідь
на
хімічні подразники, вплив холодного
повітря, фізичне навантажен-
ня.
Причому цей ефект не пов'язаний із
стабілізацією мастоцитів. Най-
потужніший
вплив виявляється при аспіриновій,
екзогенній і харчовій
астмах,
а також при астмі фізичного зусилля.
Препарат призначають у
період
ремісії за допомогою спеціального
турбоінгалятора (спінхале-
ра).
Ефект, як правило, починає проявлятися
після 1-2 тижнів лікуван-
ня,
а тому при пилковій астмі прийом
препарату розпочинають за 1-2
тижні
до сезону цвітіння рослин, пилок яких
зумовлює напади ядухи, і
продовжують
безперервно аж до завершення цвітіння.
Недокроміл
натрію (тайлед,
недокроміл) у 10 разів потужніше, ніж
кромоглікат,
блокує виділення біологічно активних
речовин, у першу
чергу
— лейкотрієнів, причому не лише з
мастоцитів, але і з еозинофі-
лів,
нейтрофілів, тромбоцитів, клітин
епітелію бронхів. Недокроміл має
властивість
пригнічувати розвиток бронхоспазму,
зумовленого інгаля-
цією
алергену, нейрогенним і медіаторним
впливом. Дію препарату варто
оцінювати
не швидше, ніж через 1 місяць щоденного
прийому. Чоти-
риразові
інгаляції препарату по 4 мг ефективніші,
ніж пероральне за-
стосування
пролонгованих теофілінів і
β-адреноміметиків
для профіла-
ктики
нападів астми, і не поступаються за
силою впливу інгаляційному
беклометазону
в добовій дозі 400 мкг. В останні роки
кромони (кромо-
глікат
і недокроміл} рідко призначають
самостійно як засоби базисної
терапії.
У зв'язку з тим, що вони впливають лише
на окремі компонен-
ти
запалення, їх переважно використовують
як доповнення до інгаля-
ційних
кортикостероїдів.
При
астмі фізичного зусилля, а також при
поєднанні астми з арте-
ріальною
гіпертензією доцільне тривале чи
курсове (протягом 2 тиж-
нів)
призначення антагоністів кальцію. Так,
ніфєдипін
у
дозі 60 мг/
добу
знижує чутливість бронхів до гістаміну
і метахоліну, що проявля-
ється
покращанням функціональних показників
дихання. Певної обе-
режності
слід дотримуватися при супутній
ішемічній хворобі серця,
оскільки
зазначена доза антагоніста кальцію
іноді може посилювати
ішемію
міокарда.
Часто
застосовують фракціоновані гепарини
пролонгованої дії:
фраксипарин,
дальтепарин або
еноксипарин
по
0,3-0,5 мл на добу про-
тягом
10-14 днів. Пригнічуючи активність
комплементу, гістаміну, се-
ротоніну
та збільшуючи елімінацію імунних
комплексів, вони попере-
джують
прогресування захворювання і розвиток
незворотних змін в
судинах
малого кола.
Глюкокортикоїди
пригнічують
пізню астматичну реакцію завдяки
стабілізації
ними клітинних мембран, зменшення
виділення лізосома-
льних
ферментів, судиннорозширювального
впливу гістаміну, гіпер-
реактивності
дихальних шляхів. Крім того, вони
пригнічують запаль-
ний
процес, перерозподіляючи лімфоцити,
моноцити і еозинофіли, при-
гнічуючи
міграцію нейтрофілів із судинного
русла. Після проникнення
в
клітину, молекула глюкокортикоїду
утворює комплекс з цитоплазма-
тичними
рецепторами, який взаємодіє з хроматином
у ядрі, змінюючи
таким
чином функціональну активність клітини.
Оскільки весь процес
займає
близько 6 год, ці засоби не застосовуються
для зняття нападів
ядухи.
Саме через такий час починається
перерозподіл лімфоцитів з
крові
в лімфоїдну тканину, зниження їх
активності, пригнічуються ме-
ханізми
гіперчутливості сповільненого
(клітинного) типу. Глюкокорти-
коїди
застосовують у випадку астматичного
статусу, розвитку загост-
рень
з тяжкими нападами ядухи, які не вдається
усунути іншими засо-
бами,
а також для замісної терапії при
недостатності кори надниркових
залоз.
Гормональна залежність швидко формується
у хворих похилого
віку,
а також при недотриманні режиму
введення глюкокортикоїдів.
Вона
проявляється загостренням захворювання
при спробі відмінити
препарати
або навіть знизити їх дозу.
Для
зменшення побічних ефектів стероїдної
тер'апії необхідно ко-
ристуватися
глкжокортикоїдами короткої дії
[преднізолон,
метилпред-
нізолон).
Найкраще
зарекомендували себе розчинні у воді
еквіваленти
преднізолону
(Solupred).
Всю
добову підтримувальну дозу бажано при-
йняти
одноразово у проміжку з 6ий
до 7ий
ранку. Часто користуються
альтернуючим
способом прийому, змінюючи добову дозу
через день (у
перший
день — призначають на 50 % більшу за
розраховану, наступно-
го
— на 50 % меншу). Якщо добова доза менша
за 15 мг
преднізолоно-
вого
еквіваленту, користуються інтермітуючим
методом (усю дводобо-
ву
дозу, збільшену на 25 %, дають одноразово
зранку в
перший
день,
наступного
дня прийом пропускають). Препарати
тривалої дії не засто-
совують
для базисної терапії астми, оскільки
їх призначення, особливо
парентеральне,
зводить нанівець усі переваги
хронотерапевтичного
розподілу
стероїдів.
Значним
досягненням терапії бронхіальної астми
стало свого часу
використання
інгаляційних форм глюкокортикоїдів,
зокрема бетамета-
зону,
беклометазону, тиксокортолу, а
особливо — будезоніду,
флюти-
казону
і мометазону. Усі
вони мають дуже незначно виражені
системні
побічні
ефекти, зокрема — пригнічення кори
надниркових залоз та іму-
носупресії.
Особливо низькою є така дія у будезоніду
і флютиказону —
засобів,
що погано всмоктуються із слизових
оболонок, проявляючи зде-
більшого
місцевий вплив, а, всмоктавшись, дуже
швидко руйнуються
печінковими
ферментами. Проте залишається можливість
місцевої іму-
носупресії,
оскільки значна частина препарату
залишається на слизовій
оболонці
рота і глотки. Тому для попередження
орального кандидозу
користуватися
інгаляційними глюкокортикоїдами
рекомендують перед
прийомом
їжі, а відразу після інгаляції —
прополіскувати рот водою.
На
сьогодні флютиказон
(фліксотид)
вважається одним з найбільш
безпечних
інгаляційних глюкокортикоїдів. Його
місцева активність і
спорідненість
до стероїдних рецепторів у 18 разів
більша, ніж в декса-
метазону
і в 3 рази — ніж у будезоніду. У той же
час афінність до
власне
глюкокортикоїдних рецепторів у 30-100
разів вища, ніж до ін-
ших
стероїдних рецепторів, що забезпечує
високу селективність впли-
ву
і низький ризик системного і
мінералокортикоїдного ефектів. Мен-
ше
1 % препарату всмоктується зі слизових
оболонок бронхів, причому
практично
весь інактивується при першому ж
проходженні через печі-
нку.
Тому при призначенні засобу перорально
в дозі до 16 мг він взага-
лі
не виявляється у плазмі. Якщо достатньо
виражений протизапаль-
ний
вплив забезпечує інгаляція добової
дози 100 мкг, то системний
вплив
починає проявлятися лише при перевищенні
2000 мкг/добу.
Мометазону
флуорат (астманекс). Особливі
надії покладаються на
мометазону
флуорат —
новий і поки що найефективніший
інгаляцій-
ний
стероїд.
Враховуючи
триетапність перебігу бронхіальної
астми і появу но-
вих
терапевтичних засобів, на сьогодні
переглянута стратегія лікуван-
ня
таких хворих на початковому алергічному
етапі астми. Препарата-
ми
вибору для початкової терапії є
інгаляційні стероїди, які признача-
ються
на тривалий час. У випадках недостатньої
ефективності терапія
доповнюється
р2-міметиками
тривалої дії.
При
застосуванні малих доз {100-400 мкг) немає
суттєвої терапевти-
чної
різниці між беклометазоном, будезонідом
і флютиказоном, проте
економічно
вигідніше призначати два перших засоби.
У випадку більшої
добової
потреби (1200-1600 мкг) перевагу надають
флютиказону через
менший
ризик розвитку системних ефектів.
Навіть при стероїдозалеж-
ній
астмі пероральні глюкокортикоїди
вдається повністю відмінити у 75-
85
% хворих на тлі 4-місячного лікування
флютиказоном у добовій дозі
2000
мг і у 45-60 % — при повністю "безпечній"
дозі 1500 мг.
Показанням
для системної стероїдної терапії є
неефективність ви-
соких
доз інгаляційних глюкокортикоїдів
(ОФБ, покращується менше
ніж
на 15 % після 20 упорскувань беклометазону,
або — тріамциноло-
ну,
або 4 — флунізоліду чи флютиказону за
добу).
Останнім
часом переглянута також стратегія щодо
застосування β2-
агоністів.
Якщо вживання іг
особливо, зловживання інгаляційними
аго-
ністами
короткої дії [сальбутамол,
фенотерол) погіршує
перебіг ас-
тми
і навіть веде до скорочення тривалості
життя, то аналогічні засоби
тривалої
дії [сальметерол,
формотерол, альбутерол) значною
мірою
позбавлені
вказаних недоліків. їх застосування
особливо ефективне
при
нічних нападах ядухи. В таких випадках
виправдане призначення
комбінованих
інгаляційних препаратів, які містять
стероїд (наприклад,
флютиказон)
і β2-3Γ0ΗΪΓΓ
тривалої
дії (сальметерол) — сєретид.
При
тяжкому перебізі бронхіальної астми
або переважанні нічних
нападів
перевагу перед пролонгованими
теофілінами, які прискорю-
ють
формування легеневої гіпертензії, слід
надавати β2-ΜΪΜετΗΚ3Μ
три-
валої
дії.
З
нових засобів передусім варто згадати
антагоністи рецепторів
лейкотрієну
D4
(aLTD4), які
продемонстрували високу клінічну ефек-
тивність,
забезпечуючи захист від бронхоспазму,
зумовленого бронхо-
провокацією
алергенами чи аспірином. Лейкотрієни
при астмі синте-
зуються
в тканині легенів еозинофілами. їх
рівень корелює, з тяжкістю
перебігу
бронхіальної астми і ступенем
бронхоспазму. Є дані про важ-
ливу
роль лейкотрієнових механізмів при
аспіринові астмі. Вважають,
що
при прийомі аспірину (або інших
нестероїдних протизапальних
препаратів)
у таких пацієнтів заблоковується
циклоксигеназний шлях
метаболізму
арахідонової кислоти, який веде до
утворення простаглан-
динів.
Натомість, активується ("шунтується")
циклоксигеназний шлях
із
синтезом лейкотрієнів. Утворення
надмірної кількості лейкотрієнів,
особливо
LTD4,
веде
до бронхоспазму.
Для
антагоністів LTD4
властиве
зростання ефекту зі збільшенням
добової
дози (залежність "доза-ефект") і
пролонгація дії (прийом 1-2
рази
на добу). їх випускають у таблетованій
формі, що зручно в засто-
суванні.
Серед найефективніших антагоністів
слід передусім згадати
монтелукаст
(Singular,
MSD), зафірлукаст
(Accolate,
Zeneca), лраялу-
касяг
(SmithKline-Beecham),
іралукаст
(Ciba-Geigy).
Призначення
зафі-
рлукасту
по 20 мг двічі на добу зменшує денні та
нічні прояви астми,
